Исследование влияния трис- (2-карбамоилэтил) амина на инициирование полимеризации акриламида
ИССЛЕДОВАНИЕ ВЛИЯНИЯ ТРИС- (2-КАРБАМОИЛЭТИЛ)
АМИНА НА ИНИЦИИРОВАНИЕ ПОЛИМЕРИЗАЦИИ АКРИЛАМИДА
При полимеризации акриламида в щелочных растворах в
результате реакции между акриламидом и аммиаком, образующимся при гидролизе
амидных групп, происходит образование трис- (2-карбамоилэтил) амина (ТКА) [1], который дает с персульфатами,
используемыми в качестве инициаторов полимеризации акриламида,
окислительно-восстановительную систему [2], вследствие чего резко меняются
кинетика инициирования и, следовательно, параметры всего процесса и свойства
полимера. Кроме того, система персульфат — ТКА представляет самостоятельный
интерес для инициирования полимеризации в водной среде (ввиду доступности ТКА)
[3] и как модель для изучения реакции между третичными аминами и перекисями. В
связи с этим представляют интерес установление влияния ТКА на гомолитический
распад персульфата в различных условиях и природа веществ, образующихся в
рассматриваемой редокс-системе, а также особенности полимеризации акриламида в
водных растворах, инициируемой персульфатом калия и специально добавленным ТКА.
Для
опытов использовали ТКА с т. пл. 185° (из смеси пропанола-2 и воды),
синтезированный из акриламида и аммиака согласно [4]. Персульфат калия (ч.) (ГОСТ 4146-65), КОН (ч.) (ГОСТ 4203-65) и бисульфат калия
(ч.) (ГОСТ 4223-65) дополнительной очистке не подвергали. Акриламид трижды
перекристаллизовывали из бензола. Во всех опытах применяли бидистиллированную
воду.
Концентрацию
персульфата калия определяли полярографически по ранее описанной методике [2].
Содержание свободного ТКА в водных растворах контролировали путем потенциометрического
титрования ОД н. раствором НС1, используя рН-метр рН-340. О ходе полимеризации
судили по убыли в растворе концентрации акриламида, определяемой
бромид-броматным методом. Характеристическую вязкость полимеров определяли в
10%-ном водном растворе NaCl при
20±0,05°, используя вискозиметр ВПЖ-2 с диаметром капилляра 0,56 мм.
При
установлении природы продуктов взаимодействия персульфата калия и ТКА смешивали
по 25 мл водных растворов исходных веществ (0,434 и 0,868 моль/л
соответственно) и выдерживали смесь в течение 1 ч при 20°. Далее раствор
концентрировали в вакууме при 40-50° до уменьшения объема смеси в ~3 раза по
сравнению с первоначальным. Выделившиеся кристаллы (2,98 г)
перекристаллизовывали из воды и анализировали на содержание азота (по Кьельдалю)
и сульфат-ионов (весовым методом). В маточном растворе бромид-броматным методом
определяли содержание непредельных соединений, и с помощью реакции с
сернокислым гидроксил-амином и последующего титрования выделившейся серной
кислоты определяли концентрацию карбонильных соединений. Качественно
присутствие в реакционной смеси карбонильных соединений обнаруживали с помощью
реакции с 2,4-динитро-фенилгидразином.
Для
исследования кинетики взаимодействия в системе персульфат — ТКА навески
исходных веществ растворяли в отдельных порциях воды (20°), после чего сливали
их и по ходу реакции отбирали пробы для анализов. Полимеризацию акриламида проводили
по методике, описанной в работе [5].
Исходи из данных по предельной степени превращения
персульфата калия (ПСК) под действием различных количеств ТКА было показано, что в отсутствие
каких-либо добавок ПСК реагирует с ТКА в соотношении 1:2. Однако из кинетических кривых (рис. 1), полученных при разных соотношениях реагентов, видно, что в
начальный период ПСК и ТКА расходуются в эквимольном соотношении, а
дополнительное количество ТКА вступает в реакцию лишь после того, как
значительная часть ПСК уже прореагировала. На основании этих данных можно
заключить, что
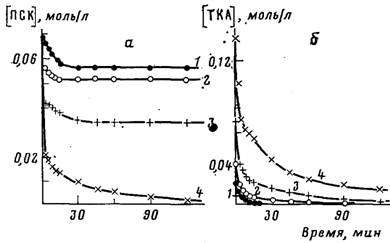
Рис.
1. Кинетические кривые расхода ПСК (а) и ТКА (б) при мольном соотношении
реагентов: 1 — 1:0,36; 2-1:0,5; 3-1:1; 4-1:2. [ПСК]=0,069
моль/л, вода, 20°
ТКА приобретает неактивную форму по накоплении в системе
продуктов реакции ПСК с ТКА. При изучении солеобразного продукта, выпавшего в
осадок после концентрирования реакционной смеси, выявлено отсутствие в нем
калия и наличие сульфат-ионов и азота, содержание которых близко к содержанию
их в соли ТКА и серной кислоты. Выделенное вещество, так же как и полученный
встречным синтезом из ТКА и серной кислоты сульфат ТКА, плавится с разложением
при 192—193°. Кроме того, при обработке полученного сульфата едким кали ТКА был
выделен в виде свободного основания. Выход соли при взаимодействии ТКА и ПСК в
соотношении 2 : 1 в расчете на исходный ТКА составил 49,4%, т. е. половина ТКА
превращается в ходе реакции в соль.
Образование сульфата ТКА в реакции ПСК и ТКА сопровождается
появлением в маточном растворе соединений, содержащих двойные углерод-углеродные
связи и карбонильные группы. Так, в растворе, полученном в результате
взаимодействия ПСК и ТКА при начальных концентрациях 0,092 и 0,184 моль/л,
обнаружено 0,045 г-экв/л непредельных соединений и 0,046 г-экв/л соединений,
содержащих карбонильные группы. Таким образом, на основании приведенных данных
и с учетом схемы окисления третичных аминов перекисями, предложенной в работе
[6], взаимодействие ТКА с ПСК
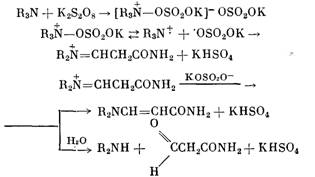
происходит через промежуточное образование катион-радикала R3NT и радикала KOS020 , которые при отсутствии акцепторов радикалов реагируют
с образованием енамина, вторичного амина и альдегида, а также бисульфата калия. Последний нейтрализует третичный амин и переводит его
в неактивную по отношению к ПСК форму. Очевидно, что и продукты реакции (енамин
и вторичный амин) подобно ТКА реагируют с бисульфатом калия и находятся в реакционной смеси в виде солей.
Подтверждением того, что протонированный ТКА не вступает в
окислительно-восстановительную реакцию с ПСК, явился опыт с добавкой к смеси
указанных веществ бисульфата калия в количестве, достаточном для нейтрализации
ТКА, при этом содержание ПСК в
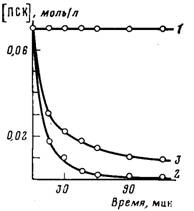
смеси не менялось (рис. 2). Напротив, при проведении реакции в щелочной среде
(с добавкой эквимольного по отношению к ПСК количества КОН) ход кинетической
кривой убыли ПСК (рис. 2) показывает, что до глубоких степеней превращения ПСК
взаимодействует с ТКА в соотношении 1 : 1 вследствие нейтрализации бисульфата
калия более сильным, чем
ТКА, основанием. В буферном растворе с рН 6,85, где, так же
как и в щелочном растворе, нивелируется действие бисульфата калия, реагенты
вступают в реакцию в практически эквимольных количествах (рис. 2).
Из приведенных данных вытекает, что система ПСК — ТКА может
быть использована для инициирования полимеризации лишь в нейтральных и щелочных
средах. Изменяя рН среды, можно регулировать скорость распада ПСК под действием
ТКА и, следовательно, скорость полимеризации и среднюю молекулярную массу
полимера.
В случае распада ПСК под действием ТКА в системе,
содержащей по-лимеризующееся соединение (акриламид), радикал KOSO2 реагирует не только с катион-радикалом R3N*, отрывая от него
атом водорода, но и с молекулой мономера, вызывая его полимеризацию
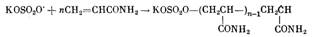
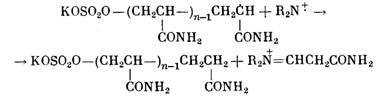
Катион R2N=CHCH2CONH2 по описанной выше
схеме (1) превращается далее в енамин, вторичный амин и альдегид. Образование
карбонильного соединения при полимеризации акриламида в присутствии системы ПСК
— ТКА подтверждено нами экспериментально.
Увеличение скорости распада персульфатного инициатора под
действием ТКА, естественно, приводит к ускорению полимеризации и уменьшению
характеристической вязкости [т]] полимера (уменьшение [г] частично обусловлено также и тем, что ТКА
является агентом передачи цепи при радикальной полимеризации [1]). Так, при 50°
и содержании в воде 4 вес.% акриламида и 0,1 вес.% ПСК в течение 2,5 ч получен
полимер с [Ti]
=7,6 дл/г и выходом 96%; при одновременном
присутствии 0,035 вес.% ТКА за то же время практически получено 100%
полиакриламида с [т]] = =3,7 дл/г. Однако использование системы ПСК — ТКА
позволяет понизить температуру синтеза и получить высокомолекулярный
полиакриламид с приемлемой скоростью: при 20° под действием одного только ПСК
полимеризация акриламида не идет, тогда как при той же температуре в результате
полимеризации в водном растворе, содержащем 7 вес.% акриламида, 0,04 вес.% ПСК
и 0,035 вес.% ТКА, в течение 2 ч получен полимер с [Л] = = 11,0 дл/г при выходе
96%.
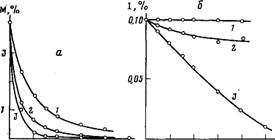
Рис. 3.
Кинетические кривые расхода акриламида (а) и персульфата
калия (б) в ходе
полимеризации без добавок (1), в присутствии
0,035% ТКА (2) и 0,55% аммиака (3). Вода, 50°
ТКА легко образуется in situ при проведении полимеризации акриламида в водно-аммиачных и щелочных
растворах, на что указывают данные, приведенные на рис. 3. Видно, что скорости
полимеризации и разложения инициатора в значительной степени увеличиваются при
введении в систему аммиака. Обращает на себя внимание, что скорость разложения
ПСК в течение полимеризации с добавкой аммиака сохраняет практически постоянное
значение, несмотря на быстрое понижение концентрации ПСК. Этот эффект может
быть объяснен ростом в полимеризационном растворе содержания соединений,
способных эффективно восстанавливать ПСК, т. е. ТКА и сопутствующих ему
первичного и вторичного аминов; [п]
полимера уменьшается от 7,6 дл/г в опыте без аммиака до 1,95 дл/г в его
присутствии.
При использовании в процессе полимеризации гидроокиси
натрия скорости расхода мономера и инициатора также увеличиваются по сравнению
с полимеризацией в нейтральном растворе, причем кинетические кривые изменения
концентраций в течение процесса носят S-образный характер. В начальный период полимеризации, когда в системе
еще нет аммиака, а значит и аминов, разложение инициатора протекает с небольшой
скоростью. По мере накопления аммиака, образующегося при гидролизе амидных
групп, в растворе появляются амины, приводящие к увеличению скорости
инициирования, что находит отражение в уменьшении [п] полимеров.
ЛИТЕРАТУРА
1. Громов В. Ф., Шейнкер А. П., Хомиковский Н. М., Абкин А.
Д. Высокомолек. соед. А, 1974, т. 16, № 2, с. 365.
2. Зильберман Е. Н., Абрамова Л. И., Афонъшин Г. Н.,
Бражкина С. Н. Высокомолек. соед. Б, 1980, т. 22, № 10, с. 774.