Технологія хімічного виробництва вінілацетату
Зміст
Вступ
1. Фізико-хімічна
характеристика процесу
1.1 Існуючі методи
одержання вінілацетату, їх стисла характеристика. Вибір методу
1.2 Теоретичні основи
вибраного методу отримання вінілацетату
2. Технологічна
характеристика процесу
2.1 Основні фізико -
хімічні властивості сировини, допоміжних матеріалів, готової продукції
2.2
Опис технологічної схеми
2.3 Відходи виробництва,
їх використання
2.4 Новизна в проекті
Література
Вступ
Хімія
високомолекулярних сполук за останні роки розвивається винятково швидкими
темпами. Величезне число досліджень у цій області привело до нагромадження
багатого експериментального матеріалу, на основі якого був зроблений ряд
теоретичних узагальнень. Хімія високомолекулярних сполук перетворилася в
самостійний великий розділ хімічної науки. Промисловість синтетичних високомолекулярних
сполук, що охоплює виробництво пластичних мас, плівок, синтетичного каучуку й
синтетичного волокна, що зародилася на початку XX століття, розвивалася в
значному відриві від хімічної науки, тому технічні досягнення часто були
результатом чисто емпіричних досліджень і випереджали наукове вивчення
відповідних процесів. У тридцятих роках відбулися істотні зміни у взаєминах між
хімією й технологією синтетичних високополімерів. Промисловість стала
виготовляти цілий ряд нових технічних високополімерів, синтез яких почав
базуватися на глибокому вивченні реакцій полімеризації й поліконденсації і
перетворень у ланцюгах високополімерів. Бурхливий розвиток промисловості
пластичних мас, синтетичного каучуку й синтетичного волокна у свою чергу
стимулювало подальше розширення об'єму досліджень і поглиблене вивчення
складного механізму процесів утворення високополімерів, їхніх властивостей і
залежності фізичних показників від структури.
Полімери
на основі вінілацетату володіють рядом цінних і специфічних властивостей і,
незважаючи на відносно невелику потребу в них у порівнянні із загальною
потребою в полімерних матеріалах, відіграють важливу роль у розвитку різних
галузей промисловості. Методи їхнього одержання пов'язані з використанням
техніки полімеризації в розчинниках, суспензії й емульсії, статистичної й
щепленої сополімерізації, численних реакцій полімераналогічних перетворень.
Найважливішими особливостями цього класу полімерів є їх універсальні адгезійні
та сполучні властивості, висока міцність волокон і плівкових матеріалів, виготовлених
з їхнім застосуванням. У цей час важко назвати яку-небудь галузь народного
господарства, де б не застосовувалися полімери на основі вінілацетату.
До
полівінілацетатних пластиків відносять полівінілацетат і сополімери вінілацетату,
які випускають у вигляді гранул, розчинів і дисперсій, полівініловий спирт і
полівінілацетати.
Більше
60% колишнього СРСР виробляємого вінілацетату витрачається на виробництво
полівінілацетатної дисперсії. Одержаний емульсійною полімеризацією вінілацетат
в присутності захисних колоїдів або емульгаторів і окислювально-відновних ініціюючих
систем використовується у вигляді 50 % водного продукту такого як клеї, що
зв'язуют, плівкоутворювачів. Перевагами полівінілацетатних дисперсій перед
іншими клеями є їхня низька вартість, негорючість, нешкідливість, стійкість до
старіння, дії жирів, мастил і нафтопродуктів, гарні адгезійні властивості.
Полівінілацетатні
дисперсії широко використаються для склеювання паперу, картону, гофрокартону,
деревини, пінополістиролу, шкіри, тканин, а також у якості сполук у
водоемульсійних фарбах, компоненту композиції для кріплення керамічної плитки і
багатьох інших призначень. Недарма полівінілацетатні дисперсії називають
«матеріалом тисячі можливостей».
Лакофарбові
матеріали на основі дисперсій полівінілацетату є чудовим покриттям для
вбираючих прокладок, наприклад штукатурки, бетону, цегли, асбоцементу. Вони
швидко висихають і мають здатність «дихати», тобто пропускати вологу з
прокладки, при цьому не відбувається ні відлущування покриття, ні утворення в
ньому міхурів.
Водоемульсійні
полівінілацетатні фарби заміняють мастильні, що дозволяє зменшити використання
для технічних цілей харчової сировини. Так, застосування 1 тони
полівінілацетатної дисперсії у вигляді фарби дозволяє заощадити 900 кілограмів
натуральної оліфи, що виготовляється із соняшникової олії.
Розмаїття
областей застосування полівінілацетатної дисперсії зробило необхідним створення
різноманітних сортів цього продукту. У цей час промисловими підприємствами
випускається 25 марок полівінілацетатних дисперсій, що розрізняються в'язкістю,
складом і природою пластифікаторів, розміром часток.
Розроблено
спосіб підвищення морозостійкості (до —40° С) дисперсій, пластифіцированого 15%
дибутілфталату. Підвищення морозостійкості має істотне значення для
транспортування й зберігання дисперсій і фарб на їхній основі в різних
кліматичних умовах.
Однак
застосування пластифікаторів, здатних згодом випаровуватись з покриттів і
мігрувати в субстрати, погіршує споживчі властивості полівінілацетатних
дисперсій. Цих недоліків позбавлені дисперсії сополімерів вінілацетату зі
складними ефірами ненасичених моно- і дікарбонових кислот, іншими складними
вініловими ефірами, етиленом, що є внутрішньо пластифіцированими продуктами.
Крім того, дисперсії сополімерів вінілацетату відрізняються від гомополімерної
полівінілацетатної дисперсії більш високою адгезією до різних матеріалів, а
плівки на їхній основі стійкі до лужного гідролізу.
Особливий
інтерес представляють дисперсії сополімерів вінілацетату з етиленом. Не
поступаючись за властивостями іншим сополімерним дисперсіям, вони мають ту перевагу,
що для їхнього виробництва використовується дешева й легкодоступна сировина -
етилен. Ці дисперсії стійкі при низьких температурах, утворюють високоеластичний
клейовий шов, здатний міцно зклеювати папір і дерево з полівінілхлоридною
плівкою й у майбутньому зможуть майже повністю замінити гомополімерні
полівінілацетатні дисперсії.
Сополімери
вінілового спирту з етиленом поєднують високу еластичність із водостійкістю,
зберігаючи інші властивості полівінілового спирту: газонепроникність, стійкість
до дії мастил, жирів, нафтопродуктів, більшості органічних розчинників. Ці
сополімери можуть знайти застосування в якості плівкових і конструкційних матеріалів.
Потреба
народного господарства в полімерах на основі вінілацетату систематично
випереджає ріст обсягу виробництва. Це обумовлено високою економічною ефективністю
застосування полівінілацетатних пластиків у різних галузях народного господарства.
Для більш повного задоволення потреби в них необхідне створення великих виробництв
із великою потужністю технологічних ліній періодичної й безперервної дії й
подальше розширення марочних асортиментів. [1]
1.
Фізико-хімічна характеристика процесу
1.1
Існуючі методи одержання вінілацетату, їх стисла характеристика.
Вибір методу
Рідкофазний
процес синтезу вінілацетату
У
першому патенті Клат’є опис процесу дається в наступному виді: 250 м безводної оцтової кислоти змішуються з 10 м сірчанокислого закису ртуті. Через суміш при
температурі 60—100°С при перемішуванні пропускається ацетилен. Після припинення
абсорбції ацетилену реакційна суміш переганяється під вакуумом. При цьому
відганяється дуже невелика кількість вінілацетату й у залишку перебуває
непрореагована оцтова кислота й етілідендіацетат. Таким чином, у цьому процесі
реакція йде головним чином у бік етілідендіацетату. Таким методом можуть бути
отримані етіліденові ефіри оцтової, моно-, ді- і тріхлороцтової, пропіонової,
молочної, бензойної й іншої кислот.
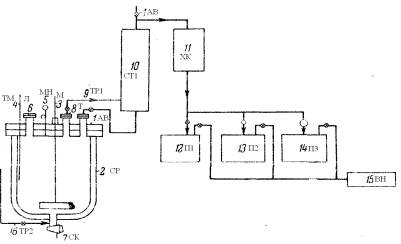
Рисунок
1:1(АВ) – автоклав; 2(СР) – сорочка; 3(М) – мішалка; 4(ТМ) – термометр; 5(МН) –
монометр; 6(Л) – лаз; 7(СК) – спускний кран; 8(Т) – труба;9,16(ТР1,2) –
трубопровід; 10(СТ1) – стовпчик для фракчіонування; 11(ХК) – холодильник;
12-14(П1-3) – приймач; 15(ВН) – вакуум-насос.
Схема
виробництва вінілацетату за рідкофазним процесом із застосуванням підвищеного
тиску рисунок 1.
Основним
апаратом є автоклав (1) (АВ), футерований склом. Автоклав з термометром (4)
(ТМ), манометром (5) (МН), завантажувальним лазом (6) (Л), мішалкою (3) (М),
сорочкою для охолодження й обігріву (2) (СР), відвідною трубою (8)
(Т), спускним краном (7) (СК) і трубопроводами (9, 16) (ТР 1,2).
В
автоклав завантажується 600 частин оцтової кислоти, 30 частин сірчанокислої
ртуті і 100 частин сірчанокислого окису заліза. Після завантаження реакційна
суміш прохолоджується шляхом додавання в сорочку охолодженого розчину, автоклав
продувається азотом і при роботі мішалки нагнітається ацетиленом. Температура
підтримується близько 10°С. Протягом 5-6 годин поглинається 142 частин
ацетилену, після чого до реакційної суміші додається 50 частин безводного оцетокислого
натрію (для нейтралізації сірчаної кислоти), надлишок ацетилену відділяється і
суміш піддається діленню у вакуумі за допомогою вакуум-насосу (1) (ВН). Пара
проходить через мідний стовпчик для фракціонування (10) (СТ1) в алюмінієвий
холодильник (11) (ХК) і конденсуються. У приймачах (12-14) (П1-3) відбираються
фракції, що відповідають вінілацетату, оцтовій кислоті й етилідендіацетату.
Сірчанокислий натрій і ртутні солі, що залишається в автоклаві віддаляються при
промиванні автоклаву, і ртуть піддається регенерації.
У
результаті виходить 100 частин вінілацетату, близько 5 частин етилідендіацетату
і рекуперується 360 частин оцтової кислоти. Вихід вінілацетату на прореаговану
оцтову кислоту становить близько 42 ваг. %.
Основні
методи одержання вінілацетату в газовій фазі зводяться до наступного. Синтез
вінілацетату здійснюється шляхом проходження суміші ацетилену з парою оцтової
кислоти через нагрітий каталізатор. Каталізаторами служать солі цинку й кадмію
(оцтові й фосфорнокислі). Як носій каталізатора застосовуються силікагель або
активоване вугілля. Температура реакції лежить у межах 210–250°.
Газову
суміш рекомендується нагрівати до цієї або трохи вищої температури. Ацетилен
застосовується в надлишку проти теоретичного.
Схема
одержання вінілацетату рисунок 2.
Ацетилен,
що вживався для одержання вінілацетату, промивався спочатку у вежі водою,
насиченої хлором, і потім у другій вежі 3%-м розчином їдкого натру.
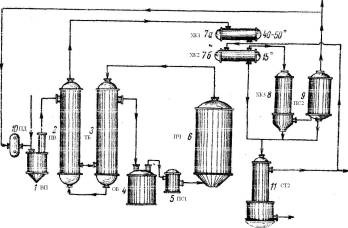
Рисунок
2:
1(ВП)
- випарник; 2(ПВ) – підігрівник; 3(ТБ) – теплообмінник; 4(ОБ) – обігрівач;
5,9(ПС1,2) – пастка; 6(ПЧ) – піч; 7а,б,8(ХК1,2,3) – холодильник; 10(ПД) –
повітродувка; 11(СТ2) – стовпчик.
Після
проходження через карбідні сущії для видалення вологи ацетилен надходив в
очисники, завантажена сухою очисною масою, що складається з кізельгуру, просоченого
хромовою кислотою, і звідси через повітродувку (10) (ПД) у випарник оцтової
кислоти (1) (ВП), у якому підтримувалася температура 120°С. Ацетилен при
температурі 90°С, насичений оцтовою кислотою, нагрівався послідовно в підігрівнику
(2) (ПВ) до 120—140° С, у теплообмінника (3) (ТБ) до 165—190° і, нарешті, в
електричному обігрівачі (4) (ОБ) до 170—220° С. У пастці для купрена (5) (ПС1),
завантаженої використаним каталізатором і розташованої перед контактною піччю,
газ звільняється від продуктів конденсації ацетилену. Суміш ацетилен-оцтова кислота
входила в контактну піч (6) (ПЧ) і проходила через каталізатор, що складається
з активованого вугілля з нанесеним на нього ацетатом цинку (20% Zn), що містяться
у 785 трубках 3,5 м висоти й діаметром 50 мм. Піч ємністю 5 м3 містить 2100 кг каталізатора. Перетворення оцтової кислоти досягає 30—40%. Охолодження
здійснюється ізофороном (з температурою кипіння 213—214°С), що входить у піч
при температурі на 4°С нижче температури печі й залишає її при температурі
печі. Початкова температура реакції 175°С і кінцева близько 220°С.
Контатна
газова суміш проходить з контактної печі (6) (ПЧ) через теплообмінник (3) (ТБ) і
підігрівник (2) (ПВ) до першого холодильника (7а) (ХК1), що залишала при
температурі 45—50°С, і до другого холодильника (7б) (ХК2), що залишила при
температурі 15°С. У наступному холодильнику (8) (ХК3) газ охолоджується до 12°С
і реціклює через пастку (9) (ПС2), яка промивається оцтовою кислотою. Конденсат
із другого холодильника, з газового холодильника (8) (ХК3) і пастки проходить
до верхньої частини стовпчика (11) (СТ2). Ацетальдегід й ацетилен відганяються,
і залишок, що складається з 40% вінілацетату, 0,6 % ацетальдегіду й 59,2%
оцтової кислоти, переганяється послідовно в трьох колонах Рашига.
Перша
дає сирий вінілацетат, що містить ацетальдегід; у другому стовпчику альдегід й
інші домішки відокремлюються: у верхній частині третього стовпчика виходить
чистий вінілацетат (температура кипіння 71°С при 730 мм). Залишок із третього стовпчика, що складає з оцтової кислоти, вінілацетату й альдегіду, який
містить домішки, і другого стовпчика переганяється періодично на двох інших колонах.
Для запобігання утворення полімеру під час перегонки додається розчин гідрохінону.
За 1 годину на 1 л каталізатора виходить близько 50 м3 вінілацетату.
Вихід вінілацетату становив по ацетилену приблизно 92% і по оцтовій кислоті
96-98%.
Парофазний
метод синтезу має істотні переваги перед рідкофазним. При парофазному методі
застосовуються більш дешеві неотруйні каталізатори, що мають більший термін
служби, чим при рідкофазному методі. В самій сутності процесу він є
безперервним і допускає легке одержання будь-якого співвідношення компонентів у
парогазовій суміші, що дає можливість регулювати процес, створювати практично
будь-який надлишок ацетилену й працювати з обраним відсотком конверсії, що
визначається як технічними, так і економічними міркуваннями (практично застосовані
співвідношення оцтової кислоти й ацетилену лежать у межах від 1:2 до 1:10).
Застосування парофазного методу, однак, вимагає використання більше високих
температур і здійснення ряду додаткових заходів пожежної й вибухонебезпечності.
[1]
1.2
Теоретичні основи вибраного методу отримання вінілацетату
Синтез
вінілацетату з ацетилену й оцтової кислоти проводиться в парогазовій фазі по
реакції:
С2Н2
+ СН3СООН → СН2=СНОСОСН3 + Q
через
утворення комплексу ацетилену й оцтової кислоти із цинкацетатом, нанесеним на
активоване вугілля.
Крім
основної реакції протікає ряд побічних, що приводять до утворення
ацетальдегіду, кротонового альдегіду, ацетону, етілідендіацетату, бензолу,
діоксиду вуглецю й інших домішок.
Зворотний гідроліз вінілацетату з утворенням оцтової кислоти й
ацетальдегіду протікає по реакції:
Н2О
+ СН2=СНОСОСН3 → СН3СНО + СН3СООН
Утворення
кротонового альдегіду:
СН3СНО
→ СН3СН=СНСНО + Н2О
Утворення
й розкладення етілідендіацетату:
СН3СООН
+ СН2=СНОСОСН3 → СН3СН=(ОСОСН3)2
СН3СН=(ОСОСН3)2
→ (СН3СО)2О + СН3СНО
(СН3СО)2О
→ СН3СОСН3 + СО 2
(СН3
СО)2О + Н2О → 2СН3СООН
Розкладення
оцтової кислоти на ацетон, воду й діоксид вуглецю:
2СН3СООН
→ СН3СОСН3 + Н2О + СО 2
Ацетилування
ацетальдегіду:
СН3СООН
+ СН3СНО → СН2=СНОСОСН3 + Н2О
Утворення
бензолу:
3С
2Н
2
→ С
6Н
6
3С2Н2 → СН4 + 5С + Н2
+ Q
Утворення
на каталізаторі смолоподібних продуктів відбувається за рахунок полімеризації
ацетальдегіду і кротонового альдегіду, а також полімерів ацетилену і його гомологів
з утворенням купренів.
Купрени
(продукт конденсації молекул ацетилену) - жовта аморфна речовина, що не
змочується водою й не розчиняється у звичайних розчинниках.
Купренизації
ацетилену сприяє присутність міді, а також контакт ацетилену з нагрітими
металевими поверхнями.
Вирішальним
фактором в утворенні купренів є збільшення часу перебування у парогазовій
суміші (ПГС) у зоні контактування.
Протіканню
побічних реакцій сприяє підвищена вологість, місцеві перегріви каталізатора при
невірному веденні технологічного процесу або пропуски води в теплообмінних
апаратах.
Забруднення
вінілацетату-сирцю домішками збільшується при недостатній чистоті змішаної
оцтової кислоти і піролізного ацетилену. [6]
2. Технологічна
характеристика процесу
2.1
Основні фізико - хімічні властивості сировини, допоміжних матеріалів, готової
продукції
Вінілацетат
- безбарвна, прозора рідина з різким ефірним заходом.
|
Молекулярна формула
|
|
СН3СОOСН=СН2
|
|
Структурна формула
|
|
|
|
Молекулярна маса
|
|
86
|
|
Щільність
|
кг/м3
|
934
|
Температура
|
|
|
|
кипіння
|
оС
|
72,7
|
|
плавлення
|
оС
|
мінус 92,8
|
|
Теплота
|
|
|
|
горіння
|
кДж/моль
|
2065,7
|
|
полімеризації
|
кДж/моль
|
89,3
|
|
Розчинність у воді
|
%
|
2,4
|
Ацетилен
при нормальних умовах являє собою безбарвний газ з слабким ефірним заходом, що
має наступні фізичні характеристики:
|
Молекулярна формула
|
|
С2Н2
|
|
|
Структурна формула
|
|
|
|
|
Молекулярна маса
|
|
26
|
|
|
Щільність
|
кг/м3
|
1,175
|
|
Температура
|
|
|
|
|
кипіння
|
оС
|
мінус 83,8
|
|
|
плавлення
|
оС
|
мінус 81
|
|
|
Критична
|
|
|
|
температура
|
оС
|
35,6
|
|
тиск
|
МПа
|
6,16
|
|
кгс/см2
|
61,6
|
|
Теплотворна здатність
|
ккал/м3
|
13387
|
|
кДж/ м3
|
52200
|
Оцтова
кислота - безбарвна рідина з різким заходом оцту, добре розчинна у воді.
|
Молекулярна формула
|
|
СН3СООН
|
|
|
|
Молекулярна маса
|
|
60
|
|
Щільність
|
кг/м3
|
1049
|
Температура
|
|
|
|
кипіння
|
оС
|
118
|
|
плавлення
|
оС
|
16,6
|
Вінілацетат-сирець
фізико-хімічні властивості визначаються наявністю в ньому не менш 40%
вінілацетату й не більше 60% оцтової кислоти.
Ацетальдегід
- безбарвна, прозора рідина з різко вираженим заходом прілих яблук.
Ацетальдегід необмежено розчинний у воді.
|
Молекулярна формула
|
|
СН3—СНО
|
|
Структурна формула
|
|
|
|
Молекулярна маса
|
|
44
|
|
Щільність
|
кг/м3
|
783
|
Температура
|
|
|
|
кипіння
|
оС
|
20,8
|
|
плавлення
|
оС
|
мінус 124
|
Кротоновий
альдегід -рідина із сильним і різким заходом.
|
Молекулярна формула
|
|
СН3-СН=СН―СНО
|
|
Структурна формула
|
|
|
|
Молекулярна маса
|
|
70
|
|
Щільність
|
кг/м3
|
848
|
Температура
|
|
|
|
кипіння
|
оС
|
102,2
|
|
плавлення
|
оС
|
мінус 69
|
Ацетон
- безбарвна, прозора рідина з характерним заходом. Змішується з водою й
органічними розчинниками в будь-яких співвідношеннях.
|
Молекулярна формула
|
|
СН3―СО―СН3
|
|
Структурна формула
|
|
|
|
Молекулярна маса
|
|
58
|
|
Щільність
|
кг/м3
|
790
|
Температура
|
|
|
|
кипіння
|
оС
|
56,2
|
|
плавлення
|
оС
|
мінус 95
|
Карбамід при нормальних умовах
|
Молекулярна формула
|
|
Н2N―CО―NН2
|
|
Структурна формула
|
|
|
|
Молекулярна маса
|
|
48
|
Газоподібний
азот - інертний газ без кольорів, запаху й смаку.
|
Молекулярна формула
|
|
Структурна формула
|
|
|
|
Молекулярна маса
|
|
28
|
|
Щільність
|
кг/м3
|
1,25
|
Температура
|
|
|
|
кипіння
|
оС
|
мінус 195
|
|
плавлення
|
оС
|
мінус 210
|
Розсол
- водяний розчин хлористого кальцію з добавкою біхромату натрію.
|
Щільність
|
кг/м3
|
не менш 1240
|
Температура
|
оС
|
від мінус 10 до мінус
18
|
|
РН середовища
|
|
від 8 до 10
|
Кубовий залишок випарників.
Фізико-хімічні властивості обумовлені наявністю не менш 40%
оцтової кислоти й не більше 60% полівінілацетату, смол неграничних вуглеводнів,
гідрохінону, води.
Фракція кротонового альдегіду з 16 тарілки колони (КЛ1).
Фізико-хімічні властивості обумовлені наявністю від 5% до 15%
кротонового альдегіду розчиненого в оцтовій кислоті. [6]
2.2 Опис технологічної схеми
Ректифікація вінілацетату-сирцю
Процес ректифікації вінілацетату-сирцю
здійснюється на двох агрегатах ректифікації - ректифікаційних колонах КЛ1і КЛ2.
Регенерація оцтової кислоти здійснюється випарюванням оцтової кислоти у
випарниках. Виділення вінілацетату з ацетальдегідної фракції
здійснюється на одній ректифікаційній колоні загальної для двох агрегатів
ректифікації.
Вінілацетат-сирець зі стадії синтезу
надходить у збірник ЗБ 1. Подих збірника ЗБ1 здійснюється через зворотний
холодильник, гідрозатвор.
Затворною рідиною в гідрозатворі служить
вінілацетат-сирець, що подається насосами Н1.
Вінілацетат-сирець зі збірника ЗБ1 насосом
Н1 через холодильник ХК1 і холодильник-конденсатор ХР1 без зупинок подається як
харчування в ректифікаційну колону КЛ1. Колона КЛ1 обігрівається паром, що
подається в кип'ятильники КП1 і КП2. У колоні КЛ1 відбувається відгін
вінілацетату від висококиплячих компонентів. Температура в кубовій частині
колони підтримується в межах 122-130 0С, тиск не більше 0,06МПа.
Висококиплячі компоненти з куба колони КЛ1
відбираються у випарник.
Парогазова суміш із верхньої частини
колони КЛ1 конденсується в дефлегматорі ДФ1 і холодильнику ХК2. Продукти
конденсації зливаються у збірник ЗБ2. Гази, що не сконденсувалися, і пари, з
холодильника ХК 2 скидаються через гідрозатвор і ОПК на смолоскипову установку
цеху ацетилену.
Частина дистиляту зі збірника ЗБ2
подається у верхню частину колони КЛ1 як флегма, інша частина дистиляту
подається як харчування на ректифікаційну колону КЛ2 і для готування розчину
інгібітору в розчинники. Збірник дистиляту ЗБ2 повідомлений з відстійником Е1,
де відбувається розшарування вінілацетату й водного шару. Водний шар періодично
скидається в каналізацію промислових брудних стоків.
Для запобігання полімеризації вінілацетату
в колоні КЛ1, з розчинників гідрохінону насосом подається інгібітор-розчин
гідрохінону.
Для зв'язування кротонового альдегіду й
інших неграничних вуглеводнів на 6-у тарілку колони КЛ1, насосом з розчинника
карбаміду, подається розчин карбаміду в оцтовій кислоті. Утворені при цьому
смолоподібні продукти виводяться з куба колони у випарники. Крім того, фракція
кротонового альдегіду відбирається з 16-ої тарілки колони КЛ1 у дренажний
приймач і в суміші з кубовим залишком випарників відправляється для спалювання
на установку термічного знешкоджування рідких відходів.
Парогазова суміш, що містить пари
вінілацетату з домішками ацетальдегіду й ацетону, з верхньої частини колони КЛ2
конденсується в дефлегматорі ДФ2 і холодильнику ХК3.
Продукти конденсації зливаються в збірник
ЗБ3. Гази, що не сконденсувалися, і пари (ацетилен з домішками ацетальдегіду,
ацетону й вінілацетату) з холодильника ХК3 скидаються через гідрозатвор і ОПК
на смолоскипову установку цеху ацетилену.
Частина дистиляту зі збірників дистиляту
ЗБ2 насосом подається як флегма у верхню частину колони КЛ2. Інша частина
дистиляту колони КЛ2, з метою виходу із системи ректифікації ацетальдегіду й
ацетону, зі збірника флегми ЗБ3 відбирається в збірник.
Для запобігання полімеризації вінілацетату
в колоні КЛ2 у збірник дистиляту СБ 2 з розчинників гідрохінону насосом
подається інгібітор - розчин гідрохінону.
Пари вінілацетату по бічному відбору, що
перебуває між 4 - 5 тарілками колони, через регулюючу заслонку надходять на
конденсацію в конденсатор КР1 і холодильник ХК4. Вінілацетат-ректифікат, що
сконденсувався, через холодильник зливається в збірник ЗБ4, звідки товарний
вінілацетат-ректифікат насосом Н2 відкачується в сховища базисного складу або в
збірник ЗБ1 на переробку.
Кубова частина колони КЛ2 (вінілацетат з
домішками полівінілацетату, оцтової кислоти й води) виводиться в збірник ЗБ4.
[6]
2.3
Відходи виробництва, їх використання
Відходи
виробництва вінілацетату характеризуються таблицею
|
Найменування відходу.
Апарат або стадія, де утвориться
|
Напрямок використання,
метод очищення або знешкодження
|
Норми утворення
відходів, кг. 2007 р.
|
|
1
|
2
|
3
|
|
Тверді відходи
|
|
|
1. Мішки паперові з-під
гідрохінону
|
Відправляється у
хімнакопичувачі твердих відходів
с. Фугаровка
|
0,018
|
|
2. Рукави
гумовотканинні відпрацьовані
|
Відправляється у
хімнакопичувач твердих відходів
с. Фугаровка
|
0,023
|
|
3. Полівінілацетат
після очищення резервуарів ХГС відділення ректифікації
|
Відправляється у
хімнакопичувач твердих відходів
с. Фугаровка
|
0,03
|
|
Рідкі відходи
|
|
|
1. Кубовий залишок
випарників поз. 403/1-2
Масова частка, %
–оцтової кислоти не
менш 40,0;
–полівінілацетата води,
смол неграничних вуглеводнів, гідрохінону, етілідендіацетату не більше 60,0
|
Відправляється у цех
ацетилену на спалювання
|
20,0
|
Відкачується через
станцію перекачування № 3 на ФХО
|
351
|
|
3. Вода при змиві
нульової оцінки етажерки відділення ректифікації, К. 1200 А
|
Відкачується через
станцію перекачування № 3 на ФХО
|
255
|
|
4. Дистилят колони поз.
101
|
На спалювання у цех
ацетилену
|
19,0
|
|
5. Фракція кетонів
колони поз.101
|
На спалювання у цех
ацетилену
|
0,975
|
|
Газоподібні відходи
|
|
|
1.Викідні гази
відділення
ректифікації
|
Направляється на
смолоскипову установку
цеху ацетилену
|
69,064
|
|
2. Викиди через
воздушку ємностей поз. 109/1-3, розчинника поз. 111(6/П-7), К.1200 А
Масова концентрація,
мг/м3
–оцтової кислоти не
більше 10,735
|
Викидаються у атмосферу
|
0,019
|
|
3. Неорганізовані
викиди:
|
|
|
|
3.1 Відділення
ректифікації (22Н/П-7)
–вінілацетат
–оцтова кислота
|
Викидаються у атмосферу
|
0,258
1,4526
|
|
4. Димови гази печі
спалювання рідких відходів:
–оксид вуглецю
–діоксид азоту
–сірчистий ангідрит
|
Викидаються у атмосферу
|
0,00876
0,02183
0,00197
|
2.4 Новизна в проекті
Довідка за результатами впровадження
рацпропозиції «Підвищення ефективності роботи колони поз.101 цеху вінілацетату»
Введення
в експлуатацію додаткових потужностей виробництва вінілацетату в листопаді
2005р. привів до збільшення кількості побічних продуктів, що утворяться на
стадії синтезу, відповідно до росту навантаження на колону ректифікації
ацетальдегідної фракції і до зниження ефективності роботи цієї колони.
Середні
показники роботи колони поз.101 у період із грудня 2005р. до реконструкції
колони відносять:
¾
середня масова концентрація вінілацетату в кетоновій фракції -
25%; середня масова концентрація вінілацетату в дистиляті колони - 5%.
Дистилят
колони і кетонова фракція піддавалися термічному знешкодженню на печі.
Після
впровадження заходів щодо рацпропозиції «Підвищення ефективності роботи колони
цеху вінілацетату» середні показники роботи колони склали:
¾
середня масова концентрація вінілацетату у кетоновій фракції - 1%;
¾
середня масова концентрація вінілацетату у дистиляті колони -
0.1%.
Середньогодинне
утворення кетонової фракції і дистилята колони становить 12.25кг/год. і
62кг/год. відповідно.
Безповоротні
втрати вінілацетату з кетоновою фракцією й дистилятом колони до її
реконструкції відносили:
12.25
* 0.25 + 62 * 0.05 = 6.16кг/год. або
6.16
* 8400 / 1000 = 51.744т/рік.
Безповоротні
втрати вінілацетату з кетоновою фракцією і дистилятом колони поз.101 після її
реконструкції становлять:
12.25
* 0.01 + 62 * 0.001 = 0.185кг/ч або
0.185
* 8400 / 1000 = 1.554т/рік.
Зменшення
втрат вінілацетату після впровадження заходів щодо рацпропозиції склало:
51.744
- 1.554 = 50.19т/рік,
що в
грошовому вираженні, при фактичній собівартості вінілацетату в жовтні 2007р.
4555.95грн/т, становить:
50.19
* 4555.95 = 228663грн/рік
Крім
того, впровадження заходів щодо рацпропозиції дозволило поліпшити показники
якості кетонової фракції з досягненням масової концентрації ацетону від 94 до
97%. З моменту реконструкції колони отримано 33.61т кетоновій фракції, що
відповідає показникам якості по ТУУ В 24.1-33270581-016:2007.
Таким
чином, при збільшенні кількості тарілок збільшилася продуктивність колони. [6]
Література
1.
Ватлаев Ф.П., Вайнштейн В.Б., Лапидус А.С. Бюллетень по обмену
опытом в азотной промышленности, ГХИ, 10, 3 2008
2.
Федоренко Н.П. Методы и экономика получения винилацетата.
Химическая наука и промышленность, в 3 т., т. 1, 1956
3.
Гриненко В.С. Получение винилацетата, изд. АН СССР, 1958 с. 106
4.
Лебедев Н.Н. Химия и технология органического и нерганического
синтеза – М., Химия, 1988 – 592 с.
5.
Адельсон С.В., Вишнякова Т.П., Пацикин Я.М. Технология нефтехимического
синтеза – М., Химия, 1985 – 608 с.
6.
Тимофеев В.С. Принципы технологии основного органического и нефтехимического
синтеза – М., Высшая школа, 2003 – 536 с.