Отримання молібдену
МІНІСТЕРСТВО ОСВІТИ І НАУКИ УКРАЇНИ
СУМСЬКИЙ
ДЕРЖАВНИЙ УНІВЕРСИТЕТ
На
тему: Отримання молібдену
Виконав:
Курдес А. Н.
Проверила: Пастушенко А.Й.
Суми
2009 р.
Зміст
1. Молібденові руди
2. Переробка концентратів
3. Аміачний спосіб
4. Вилуговування МоО3 розчинами аміаку
5. Виробництво триокису молібдену сублімацією
6. Переробка збідненої сировини і відходів
1.
Молібденові руди
Мінерали,
важливі для виробництва, молібденіт MоS2 первинного
походження, інші – повеліт СаМоО4, молібдит Fe2(MoO4)3
і продукти вторинних перетворень сульфіду. Молібденіт, що має першорядне
значення, чорного кольору, м'який, на папері залишає межу подібно до графіту;
щільність мінералу 4700-4800 кг/мЗ.
Руди
містять десяті і соті частки відсотка молібдену, вони поділяються на кварцові,
комплексні за вольфрамітом; скарнові, у яких молібденіти інколи супроводжують
шеєліт, пірит і халькопірит, а порода складається з кременистих вапняків.
Мідно-молібденові руди колчеданового або вкрапленого типу - основний вид
сировини. Молібденіт в них супроводжують пірит і халькопірит. Частіше переважає
мідь, а молібден складає соті частки відсотка, але інколи його більше, ніж
міді.
Збагачення
базується переважно на флотації молібденіту, добування якого в концентрати,
навіть з бідних руд, досягає 90% при вмісті близько 90% MоS2.
Спочатку флотують всі сульфіди. Колективний концентрат після подрібнення
розділяють повторною флотацією, пригнічуючи мінерали міді і заліза сірчистим
або ціаністим натрієм при рН = 8,5. Збирачем для молібденіту служать гас і
мінеральні масла, а як спінювач застосовують соснове масло. Шеєліт, якщо він
наявний, виділяють з хвостів флотації, використовуючи як реагенти жирні кислоти
і силікати натрію.
2.
Переробка концентратів
Продукти,
одержувані з концентратів, різні за призначенням і складом: у чорну металургію
надходять переважно феромолібден - сплав із залізом і молібдат кальцію. У
хімічну промисловість і для отримання ковкого металу йдуть чисті сполуки:
триокис молібдену, парамолібдат амонію, молібдати натрію і кальцію.
Технологічні схеми першим переділом мають окиснення молібденіту випаленням,
рідше азотною кислотою або киснем у автоклавах. На більшості підприємств поки
застосовують випалення. Недогарок спрямовують на виплавку феромолібдену, переробляють
гідрометалургійні, вилуговуючи МоО3 розчинами аміаку, соди або лугу
або переганяють з нього триокис і уловлюють в пиловловлювачах.
Метал
у вигляді порошку відновлюють з чистого триокису водню або вуглецем, подібно вольфраму.
3.
Аміачний спосіб
Горіння
молібденіту за хімізмом і кінетикою схоже з окисненням інших сульфідів у
мідних, цинкових або свинцевих концентратах:
2MoS3
+ 7O2 = 2МоО3 + 4SO2.
(3.62)
При
високих температурах МоО3 помітно випаровується, тиск пари його має
такі величини:
температура,
0С 800 900
тиск,
Н/м2 1679 6838
У
недогарку необхідно залишити не більше 2% сірки, а температуру вище 600°С
піднімати не можна через віднесення МоО3 газами. Випалення можна
прискорити тільки подачею надлишку повітря і перемішуванням концентрату.
4.
Вилуговування МоО3 розчинами аміаку
На
виробництві вилуговування проводять при температурі не вище 50-60°С; у сталевих
чанах з пропелерними мішалками або в барабанних вилуговувавчах в три або чотири
стадії. У міцний луг витягується 80-95% молібдену при концентрації його 140
г/л. У розчині залишається до 30 г/л (≈ 2 міль/л) NH3.
Реакція утворення молібдату амонію
MoO3
+ 2NH4OH = 2NH4+ + MoO42-
+ 2H2O. (3.64)
Молібдати
міді, цинку, заліза, свинцю і кальцію реагують з аміаком по-різному. Перші три
дають аміачні комплекси і при розрахунку рівноваги тут необхідно враховувати
руйнування комплексного іона NH+5:
NH4+
= NH3 + H+;
(3.65)
pK=9,2.
Для
молібдатів міді, цинку і заліза у загальному вигляді
MeMoO4
+ 4NH4OH =  + MoO42- + 4H2O;
(3.66)
+ MoO42- + 4H2O;
(3.66)
-
для кальцію і свинцю
МеМоO4
+ 2NH4OH = Me(OH)2
+ 2NH4+ + MoO42; (3.67)
-
мідь і залізо осаджують сірчистим амонієм з розчину, у якому близько 2 моль/л надлишкового
NH3
і близько 3 моль/л NH4.
Сульфіди міді і заліза осаджуються з суміші аміачних комплексів, серед яких
переважають тетрамінні:
Сu
(NH3)2+ + S2- = CuS + 4 NH3, (3.68)
Fe(NH3)2+
+ S2- = FeS + 4NH3, K = 4·1013. (3.69)
Повнота
осадження домішок повинна бути високою, проте слід уникати забруднень сіркою,
надлишок (NH4)2S
зв'язують, додаючи свіжий розчин, від чого залишкові концентрації міді, заліза
і цинку збільшуються. Очищення проводять у сталевих гумованих чанах з
мішалками.
Для
кристалізації парамолібдату амонію (NH4)6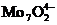 · 4H2O) потрібне
молярне відношення NH3
: МоО4 = 6 : 7, а в очищеному розчині воно більше 2:1 при концентрації
МоО близько 1 моль/л.
· 4H2O) потрібне
молярне відношення NH3
: МоО4 = 6 : 7, а в очищеному розчині воно більше 2:1 при концентрації
МоО близько 1 моль/л.
Нейтралізація
частини аміаку соляною кислотою дає краще витягання, ніж пряме випаровування, і
досить чистий продукт, в якому заліза менше 0,05%, а інших домішок сумарно не
більше 0,015%.
Паромолібдат
прожарюють у човниках з нержавіючої сталі в електричних печах з коробчастим
муфелем при температурі 500°С. Човники поступово просувають в зони високих
температур.
Застосовують
також трубчасті печі, що обертаються, з трубою з нержавіючої сталі, що
обігріваються електрикою.
Техніко-економічні
показники аміачного способу, включаючи переробку відходів, в основному залежать
від ціни сировини, яка становить більше 90% собівартості. Витягання з
концентрату в парамолібдат амонію 93-96% залежить від якості концентратів і
культури виробництва. Найбільші втрати (2-6%) припадають на очищення розчинів і
кристалізацію. Втрати при відновленні близько 1%.
5.
Виробництво триокису молібдену сублімацією
Після
підвищення щільності від 1100 до 1210 кг/м3 коагулюються осади
домішок, які перед подальшим випаровуванням до 1390 кг/м3
фільтрують. Досить випарений розчин знову фільтрують і зливають у кристалізатори
з нержавіючої сталі з мішалками і водним охолоджуванням. Маточний розчин випаровують
і повторно піддають кристалізації, виділяючи після двох стадій до 60% солі
високої чистоти. Залишок розчину випаровують насухо, нагрівають до 400°С для
перетворення в оксиди, які повертають на вилуговування. Осадження
тетрамолібдату (NH4)
 2H2O досягається скріпленням
вільного аміаку добавками соляної кислоти при температурі 60°С і перемішуванні.
У вихідному розчині повинно бути не менше 280 г/л МоО3 і його, якщо
потрібно, концентрують випаровуванням.
2H2O досягається скріпленням
вільного аміаку добавками соляної кислоти при температурі 60°С і перемішуванні.
У вихідному розчині повинно бути не менше 280 г/л МоО3 і його, якщо
потрібно, концентрують випаровуванням.
Після
центрифугування і промивання водою одержують досить чистий продукт, проте часто
забруднений хлором (>0,2%). Повторною кристалізацією, після розчинення в гарячому
5% NH4ОН
доводять до щільності 1420 кг/м3.
Маточний
розчин після десятиразового обертання спрямовують на очищення. Цей спосіб дає
ще вище добування і достатньо чистий продукт, в якому заліза менше 0,05%, а
інших домішок сумарно до 0,015%.
6.
Переробка збідненої сировини і відходів
Хвости
аміачного вилуговування, що містять сумарно до 25% молібдену, знаходилися
спіканням із содою, вилуговуванням розчинами її в автоклавах або розкладалися кислотами.
Спікання
шихти з вологих відходів і соди проводять в череневих печах при температурі
близько 750°С, отримуючи у пекові молібдат натрію. Після вилуговування водою
осаджує молібдат заліза:
3Na2MoO4
+ 2FeCl3 = 6NaCl + Fe2(МоО4)3.
(3.70)
Осад
обробляють аміаком
Fes
(МоО4)3 + 6NH4OH = 3Fe(ВІН)3 + 3(NH4)2MoO4.
(3.71)
Розчини
молібдату амонію, в які добувається до 94% молібдену, повертають в основне
виробництво; у відвальних хвостах його залишається до 1,5%. Вилуговування
хвостів содою в автоклавах можливе, якщо значно переважає окиснений молібден, а
сульфідного мало. Вилуговування соляною кислотою застосовують, якщо, крім молібдену,
наявний вольфрам.
Маточні
розчини після осадження тетрамолібдату амонію (1 г/л Мо, 40 г/л С1, 7 г/л SO4,
домішки заліза і кольорових металів) переробляють сорбцією на аніонітах.
Слабоосновний аніоніт AH-1 у
хлор-формі має динамічну обмінну місткість (ДОМ) за молібденом близько 300
кг/т. Сорбцію проводять при рН-3, пропускаючи розчин через колону із смолою.
Домішки хлору і катіонів не сорбують. Після промивання водою молібден елюїрують
5-10% аміаком і розчин (100 г/л Мо) повертають в основне виробництво.
Промислові
продукти збагачені комплексними, переважно мідно-молібденовими рудами, що
містять сульфіди заліза, міді, молібдену, а також повеліт і молібдит, піддають окиснювальному
випаленню, а потім вилуговують розчинами соди. За відсутності або при малій
кількості сульфідів випалення не потрібне.
Вільний
триокис молібдену переходить при вилуговуванні в добре розчинний Na2MoO4,
а молібдати – мідь, кальцій і залізо - взаємодіють із содою за загальною схемою
Me
MoO4 + Na2CO3
= Na2MoO4
+ MeCO3 (3.72)
Карбонати
міді і заліза далі гідролізуються, переходячи в гідроокиси і основні солі.
Вилуговування
проводять з протитечією в 4-5 стадій 10% розчином соди в залізних чанах з
механічним перемішуванням при підігріванні паровими змійовиками. Після кожної
стадії розчину дають відстоятися і пускають в оборот. Кінцеві хвости
фільтрують, промивають і скидають у відвал, а перший міцний розчин також після
фільтрації надходить на переробку. З концентрованого розчину (60% Мо)
осаджується молібдат кальцію:
Na2MoO4
+ СаС12 = СаМоО4 + 2NaCl. (3.73)
Практично
після осадження при 80°С, щоб уникнути великого надлишку CaCl2 і не
забруднити осад гіпсом, залишають в маточному розчині до 1 г/л молібдену.
Молібдат
кальцію марок МКД і МКД4, в якому не менше 44 або 40% молібденів, а домішок
сірки і фосфору відповідно не більше 0,20-0,23 і 0,1-0,2%, йде в чорну
металургію, на присадки в сталі і виплавку феромолібдену.
Відновлення
триокису молібдену відбувається в дві стадії при 800°С і відповідає реакціям:
MoO2
+ 2H2 = Mo +2H2O. (3.75)
При
протитечійному пропусканні водню реакція завершується в інтервалі температур
400-550°С; проте вимагає повільного нагрівання через можливість утворення
легкоплавкої евтектики MoO3 – МоО2, що уповільнює
відновлення.
На
виробництві застосовують такі самі печі, як для вольфраму. Відновлення
проводять в дві стадії: спочатку в межах температур до 650, а потім до 950°С.
Повільне просування човників в кінці другої стадії сприяє зниженню вмісту
залишкового кисню до 0,1-0,2%. Порошок усереднюють, просівають і зберігають в
герметичній тарі, заповненій аргоном.