Строение атома простыми словами: из чего состоит атом
Понятно и без лишней путаницы разбираем строение атома: что находится в ядре, зачем нужны протоны, нейтроны и электроны, почему атом нейтрален и как работает электронная оболочка. Материал подойдет школьникам, студентам и всем, кто хочет быстро понять тему без сухого учебникового языка.
Содержание
- Из чего состоит атом, если объяснять по-человечески
- Что такое протоны, нейтроны и электроны
- Как устроено ядро атома
- Что такое электронная оболочка и почему без нее атом не понять
- Почему атом считается нейтральным
- Где студенты чаще всего путаются в строении атома
- Как быстро запомнить строение атома
У темы строения атома плохая репутация. Как только человек слышит слова «ядро», «электроны», «протоны», «нейтроны», у него сразу возникает ощущение, что сейчас начнется что-то слишком научное, сухое и почти недоступное без особой подготовки. Кажется,
что это уже территория физиков и химиков, где обычному студенту или школьнику остается только молча запоминать термины и надеяться, что когда-нибудь они сами сложатся в картину.
Обычно этого не происходит.
Проблема здесь не в самой теме, а в том, как ее часто подают. Сначала дают длинное определение, потом перечисляют частицы, потом добавляют заряд, потом вспоминают электронную оболочку — и в итоге у человека остается не понимание, а ощущение набора слов,
которые стоят рядом, но не соединяются в одну систему.
Хотя сама идея на удивление простая.
Атом — это не какая-то абстрактная точка вещества и не загадочный шарик из учебника. У него есть внутренняя структура. И как только эту структуру показать без лишнего тумана, тема перестает казаться пугающей.
На самом базовом уровне все можно свести к очень короткой схеме:
- у атома есть ядро;
- внутри ядра находятся протоны и нейтроны;
- вокруг ядра находятся электроны.
Вот это и есть основа всей темы. Все остальное уже наслаивается сверху.
Поэтому строение атома не нужно пытаться понять через страх перед сложностью. Его намного легче понять через простую и аккуратную внутреннюю логику.
Из чего состоит атом, если объяснять по-человечески
Если говорить совсем просто, атом состоит из двух крупных частей:
- ядра;
- электронной оболочки.
Ядро находится в центре. Электроны находятся вокруг него. Уже на этом этапе у многих становится спокойнее, потому что появляется первая нормальная картинка: атом — это не хаос из частиц, а система, где есть центр и есть то, что расположено вокруг
него.
Внутри ядра находятся две частицы:
А вокруг ядра находятся:
То есть если разложить атом буквально по составу, получится так:
- ядро;
- в ядре — протоны и нейтроны;
- вне ядра — электроны.
На этом уровне никаких дополнительных усложнений пока не нужно.
Еще одна важная вещь, которую полезно понять сразу: почти вся масса атома сосредоточена именно в ядре. Это многих удивляет, потому что на рисунках электроны часто делают заметными, и кажется, будто они дают атомную «наполненность». Но по массе главная
часть атома — это именно ядро.
Электроны при этом не становятся неважными. Наоборот, они играют огромную роль. Просто роль у них не в том, чтобы давать атомную массу, а в том, чтобы определять многие химические свойства и поведение атома во взаимодействиях.
То есть уже на старте полезно развести две вещи:
- ядро — это центр и основная масса;
- электроны — это оболочка и важная часть химического поведения атома.
Так тема начинает собираться не как набор терминов, а как внутренняя конструкция, где у каждой части есть свое место.
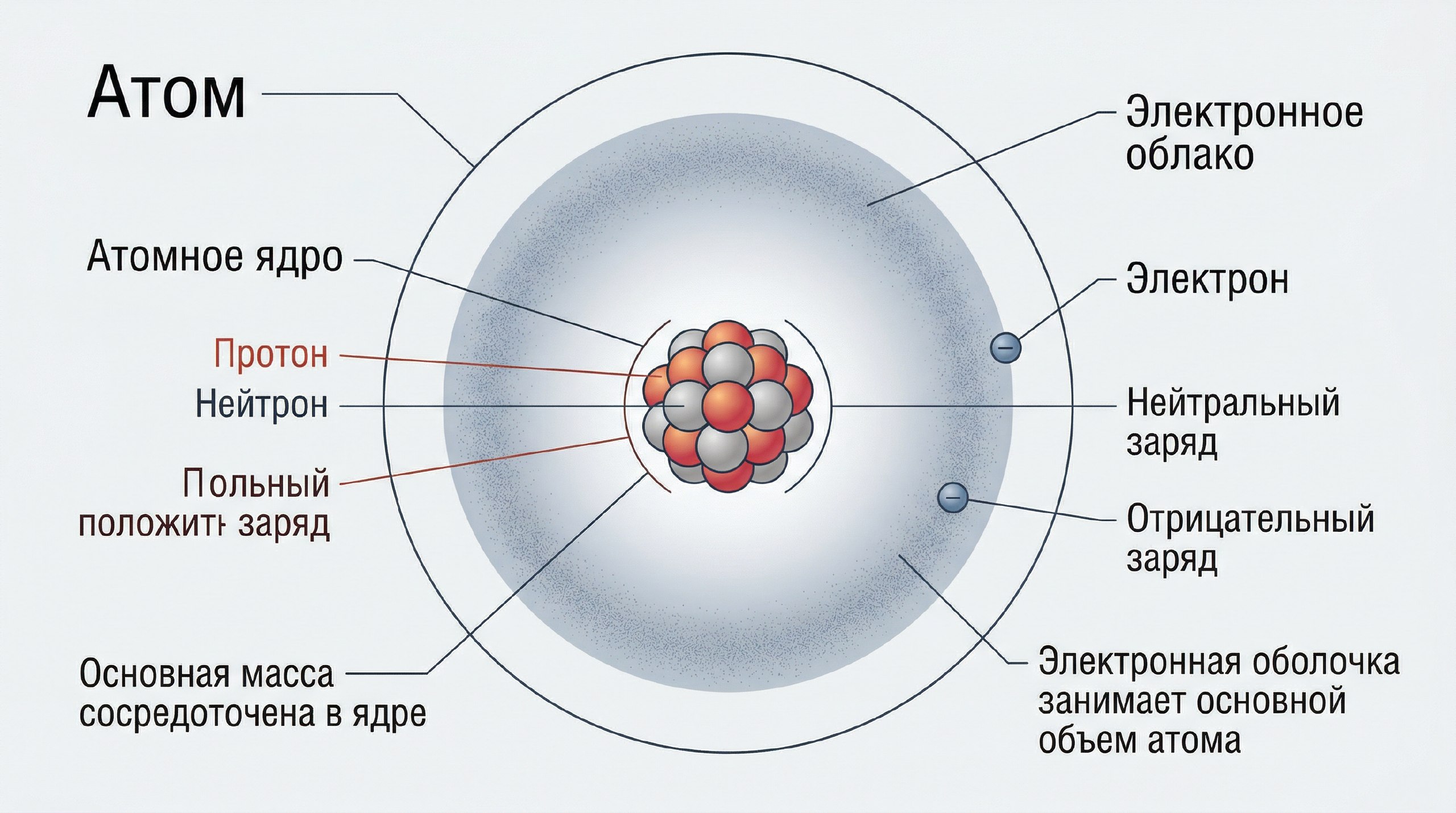
Что такое протоны, нейтроны и электроны
На этом месте тема обычно начинает или проясняться, или окончательно запутываться — в зависимости от того, как объяснить частицы. Самый удобный способ здесь не просто перечислить их, а сразу показать, что каждая из них “делает” в атоме.
Протон
Протон — это частица с положительным зарядом.
Протоны находятся в ядре. Именно они играют очень важную роль: по числу протонов определяется, какой перед нами химический элемент. Не по нейтронам, не по электронам, а именно по протонам.
Это значит, что если меняется число протонов, меняется и сам элемент.
Нейтрон
Нейтрон — это частица без электрического заряда.
Он тоже находится в ядре. Нейтроны не делают атом “другим элементом” в том же смысле, как это делают протоны, но они важны для массы ядра и его устойчивости.
То есть нейтрон — не декоративная частица и не “лишний сосед” протона. Он полноценная часть атомного ядра.
Электрон
Электрон — это частица с отрицательным зарядом.
Электроны находятся не внутри ядра, а вокруг него. Именно это место чаще всего путают. Некоторые по инерции воспринимают атом как сплошной шарик, внутри которого все частицы как будто перемешаны. Но это неверная картинка.
Электроны образуют электронную оболочку и располагаются вокруг ядра.
Если собрать все это в один короткий и удобный блок, получится вот так:
- протон — положительный, в ядре;
- нейтрон — нейтральный, в ядре;
- электрон — отрицательный, вокруг ядра.
Это уже почти весь базовый каркас темы. И если эта схема стала понятной, дальше разбираться будет намного легче.
Как устроено ядро атома
Когда человек впервые слышит слово «ядро», он часто представляет себе просто маленький плотный центр, и в целом это неплохая стартовая картина. Но важно понять, почему ядро вообще считается главной частью атома.
Ядро — это центральная часть атома, где находятся протоны и нейтроны. Оно очень маленькое по сравнению со всем атомом, но при этом именно в нем сосредоточена почти вся масса.
Вот это сочетание и делает тему чуть контринтуитивной. Атом кажется чем-то цельным и объемным, но его самая “тяжелая” часть при этом очень компактна.
Внутри ядра:
- протоны дают положительный заряд;
- нейтроны добавляют массу и участвуют в устойчивости ядра.
Если представить атом как систему, то ядро — это его центр тяжести, центр массы и главный внутренний узел.
Именно поэтому вопрос «что находится внутри атома» в нормальном объяснении почти сразу приводит к ядру. Потому что без понимания ядра все остальное остается слишком расплывчатым.
Полезно запомнить еще одну простую мысль: ядро не содержит электронов. Это кажется банальным, но именно здесь многие поначалу путаются.
То есть ядро — это:
- протоны;
- нейтроны;
- положительный заряд за счет протонов;
- почти вся масса атома.
Если этот блок понятен, тема перестает выглядеть разрозненной.
Что такое электронная оболочка и почему без нее атом не понять
После ядра вторая ключевая часть атома — электронная оболочка. Именно она часто вызывает больше всего бытовых картинок и школьных ассоциаций.
Обычно в учебных схемах электроны рисуют вокруг ядра, иногда почти как планеты вокруг Солнца. Такая картинка полезна для первого знакомства, потому что помогает понять главное: электроны находятся не в ядре, а вокруг ядра.
Но воспринимать эту картину слишком буквально не стоит.
Для начального понимания достаточно помнить несколько вещей.
Электронная оболочка — это
- область, где находятся электроны;
- часть атома, окружающая ядро;
- структура, связанная с химическими свойствами атома.
Именно электроны во многом определяют, как атом будет взаимодействовать с другими атомами. Поэтому, хотя по массе они сильно уступают ядру, по химической значимости они вовсе не “второстепенны”.
Здесь полезно держать баланс между простотой и точностью. Не нужно сразу уходить в сложные квантовые детали, но и представлять электроны как маленькие шарики, которые бегают по идеальным кругам, тоже не слишком полезно.
На базовом уровне достаточно такой формулы:
- ядро — в центре;
- электроны — вокруг;
- именно электроны образуют электронную оболочку.
И если человек это понял, значит, он уже понял строение атома на хорошем начальном уровне.
Почему атом считается нейтральным
Вот здесь у многих возникает вполне нормальный вопрос: если в атоме есть положительно заряженные протоны и отрицательно заряженные электроны, почему сам атом обычно считают нейтральным?
Ответ как раз очень логичный.
У нейтрального атома число протонов равно числу электронов. Протоны дают положительный заряд, электроны — отрицательный. Эти заряды взаимно компенсируются, и в итоге весь атом не имеет общего электрического заряда.
Это один из самых полезных моментов для понимания всей темы, потому что он показывает: атом — не просто набор частиц, а уравновешенная система.
Если коротко, логика такая:
- протоны “дают плюс”;
- электроны “дают минус”;
- когда их число одинаково, заряд в целом уравновешивается.
Именно поэтому в школьных и студенческих заданиях так часто спрашивают про число протонов и электронов. Это не механическая формальность, а способ проверить, понял ли человек сам принцип нейтральности атома.
Здесь важно не перепутать еще одну вещь: нейтроны не участвуют в общем электрическом заряде, потому что они сами по себе нейтральны. Они важны, но не как источник плюса или минуса.
То есть если говорить совсем прямо:
- заряд атома в обычном нейтральном состоянии определяется балансом протонов и электронов;
- нейтроны на этот баланс не добавляют ни плюса, ни минуса.
Как только это становится ясно, тема “заряд атома” перестает быть сложной.
Где студенты чаще всего путаются в строении атома
У этой темы есть несколько типичных точек, где почти все хотя бы раз ошибаются. И это нормально. Лучше их назвать прямо, чем делать вид, будто путаница возникает “сама собой”.
Самые частые ошибки такие
- путать атом и ядро;
- думать, что электроны находятся внутри ядра;
- считать, что элемент определяется нейтронами;
- забывать, что почти вся масса атома сосредоточена в ядре;
- воспринимать учебную картинку с орбитами слишком буквально.
Первая ошибка — смешивать весь атом с его центральной частью. Ядро — это не весь атом. Это только его внутренняя центральная зона.
Вторая ошибка — размещать электроны “внутри”. На самом деле электроны находятся вокруг ядра.
Третья ошибка — путать, какая частица определяет элемент. Здесь важно железно запомнить: элемент определяется числом протонов.
Четвертая ошибка — недооценивать роль ядра в массе атома. Хотя атом выглядит как большая система с оболочкой, почти вся его масса сосредоточена именно в центре.
Пятая ошибка — слишком буквально верить в картинку из школьной схемы. Она полезна как стартовая модель, но не как полное и окончательное описание реальности.
Если хочется совсем короткий ориентир, можно запомнить такую мини-шпаргалку:
- атом = ядро + электроны;
- ядро = протоны + нейтроны;
- электроны находятся вокруг ядра;
- почти вся масса — в ядре;
- число протонов определяет элемент;
- равное число протонов и электронов делает атом нейтральным.
Это очень простая схема, но именно она обычно и удерживает всю тему в порядке.
Как быстро запомнить строение атома
Когда тема уже понятна, возникает второй вопрос: как сделать так, чтобы она еще и запомнилась, а не рассыпалась через час после чтения.
Лучше всего здесь работает не зубрежка определений, а нормальная внутренняя картинка.
Можно представить атом так:
- в центре — плотное ядро;
- в ядре — протоны и нейтроны;
- вокруг — электроны;
- протоны дают положительный заряд;
- электроны дают отрицательный;
- если их поровну, атом нейтрален.
Это уже не просто список, а маленькая логическая модель.
Еще удобно запоминать тему через роли частиц:
- протоны определяют элемент;
- нейтроны добавляют массу и устойчивость;
- электроны участвуют в химическом поведении.
Когда частицы перестают быть “тремя словами подряд” и становятся носителями конкретных функций, запоминать их намного легче.
То есть лучший способ понять строение атома — не учить его как абзац, а собрать как систему, где у каждой части есть свое место и своя задача.