Абсорбция триоксида серы
ОГЛАВЛЕНИЕ
ВВЕДЕНИЕ. 3
ОБЗОР ЛИТЕРАТУРЫ.. 4
1.1 Электрофорез. 4
1.1.1.Техника проведения. 5
1.2. Полимеразная цепная реакция. 7
1.2.1.Специфичность и применение. 7
1.2.2.Проведение ПЦР. 9
МАТЕРИАЛЫ И МЕТОДЫ.. 9
2.1. Метод Электрофореза. 9
2.1.1.Материалы.. 9
2.1.2.Методика. 10
2.2 Метод ПЦР. 11
ЗАКЛЮЧЕНИЕ. 14
СПИСОК ЛИТЕРАТУРЫ.. 15
Завершение полной расшифровки
последовательности генома человека привело к возникновению новой области науки —
системной биологии. В основе системной биологии лежит моделирование поведения
сложных биологических процессов с целью предсказания их дальнейшего поведения.[[1]]
Одним из таких фундаментальных
процессов является функционирование живой клетки. Согласно современным
представлениям, наиболее адекватным описанием таких процессов являются
функциональные сети — модели ансамблей взаимодействующих молекул. Для описания
процесса функционирования различных генов в клетке используют генетические
сети. Упрощенно генную сеть можно представить в виде многочисленных молекул,
которые взаимодействуют друг с другом, обеспечивая, в конечном счете, контроль
активности структурных генов и тем самым формирование признаков организма.[1]
Для описания биохимических
реакций, происходящих в клетке, используют модели метаболических сетей.
Особенностью этих моделей является их сложность, которая может быть описана в
иерархическом виде. На нижних уровнях иерархии находятся генетические
макромолекулы — ДНК, РНК и белки, а взаимодействия между ними определяют
структуру функциональных сетей. Полное и адекватное исследование функций генома
невозможно без детального исследования всех уровней его иерархии. Таким
образом, в постгеномную эру на передний план выдвигаются задачи определения
структур генетических макромолекул, их функций, а также взаимодействий с
другими участниками генных и метаболических сетей.[1]
Такие методы как электрофорез
(ЭФ) и Полимеразная цепная реакция (ПЦР) составляют первые этапы в
исследованиях генетической информации и различных белковых молекул. Т.к. ПЦР - экспериментальный
метод молекулярной биологии, позволяющий добиться значительного увеличения
малых концентраций определённых фрагментов нуклеиновой кислоты (ДНК) в
биологическом материале (пробе), а ЭФ - это аналитический метод, применяемый
для разделения фрагментов ДНК по размеру (длине) и форме (в случае, если ДНК
образует вторичные структуры, например шпильки).[1]
Целью нашего занятия стало – освоение
методов работы с генетическим материалом. Из выше поставленной цели следуют
следующие задачи: 1. Составить обзор литературы
2. Отработка методов
Электрофореза и ПЦР
Электрофорез – метод разделения
макромолекул, различающихся по таким параметрам, как размеры (или молекулярная
масса), пространственная конфигурация, вторичная структура и электрический
заряд.[[2]]
Результатом проведения
электрофореза является электрофореграмма -картина, полученная после разделения
сложной смеси с помощью электрофореза и специфического проявления.
Электрофореграмма белков биологических жидкостей человека (сыворотка крови,
моча, спинномозговая жидкость и др.) позволяет врачам получить значительную
диагностическую информацию.[2]
Например, у здорового человека
относительное содержание белковых фракций при определении их в сыворотке крови
методом электрофореза на бумаге, следующее:
альбумины- 55-65%,
α1-глобулины 3-6%,
α2-глобулины 7-10%,
β-глобулины - 7-12%,
γ-глобулины - 13-19%.
При многих заболеваниях
наблюдается изменение соотношения фракций, тогда как общее количество белка
обычно мало изменяется. Выявление этих изменений с помощью метода электрофореза
широко используется в диагностических целях. [2]
Электрофореграммы
белков-ферментов (зимограммы) позволяют изучать изменения активности и
изоферментного спектра таких белков под действием внешних и внутренних факторов
как у человека, так и у других организмов. [2]
Преимущества:
1. Не требуется сложного
оборудования
2. Низкая стоимость реактивов
Недостатки:
1. Высокий риск контаминации
(загрязнения продуктами предыдущих ПЦР)
2. Требуется дополнительное
помещение и персонал для стадии детекции продукта
3. Трудоемкость
4. Только качественный анализ
(есть/нет)
Электрофорез ДНК — это
аналитический метод, применяемый для разделения фрагментов ДНК по размеру
(длине) и форме (в случае, если ДНК образует вторичные структуры, например
шпильки). Силы электрического поля, прикладываемого к образцам, заставляют
фрагменты ДНК мигрировать через гель. Сахарофосфатный остов молекул ДНК заряжен
отрицательно и поэтому цепи ДНК двигаются от катода, заряженного отрицательно,
к положительному аноду. Более длинные молекулы мигрируют медленнее, так как
задерживаются в геле, более короткие молекулы двигаются быстрее.[[3]]
К образцам обычно добавляют
низкомолекулярный кислый краситель (например, динитрофенол, бромфеноловый
синий), чтобы визуализировать ход электрофореза в процессе. Краситель также
необходим для того, чтобы определить, когда стоит остановить процесс.[3]
Электрофорез проводится в
камере, заполненной буферным раствором. Чаще всего используются буферы,
содержащие ЭДТА, трис и борную кислоту: TAE и TBE. Буфер необходим для повышения
ионной силы раствора, в котором будет происходить разделение молекул ДНК под
действием приложенного электрического поля.[3]
После разделения (иногда
краситель вносят в расплавленную агарозу) фрагменты ДНК разной длины
визуализируют при помощи флюоресцентных красителей, специфично
взаимодействующих с ДНК, например, агарозные гели обычно красят бромистым
этидием, который интеркалирует между азотистыми основаниями дуплекса и
флюоресцирует в УФ-лучах.[3]
Определение размеров производят
путем сравнения коммерчески доступных фрагментов ДНК (DNA ladder, «линейка»),
содержащий линейные фрагменты ДНК известной длины.[3]
Для электрофоретического анализа
ДНК обычно используют агарозные (для относительно длинных молекул ДНК) и
полиакриламидные (для высокого разрешения коротких молекул ДНК, например, в
случае секвенирования) гели.[3]
«Методика электрофореза с
использованием агарозного геля должна учитывать, что «поры» для разделения
макромолекул большого размера, и потому подходят только для молекул,
молекулярная масса которых не меньше 200 кДа. К преимуществам агарозных гелей
можно отнести относительно быстрое перемещение молекул, но полосы имеют
ограниченное разрешение, так как склоны к быстрому размытию границ и
распространению в разные стороны. Процедура электрофореза с гелем проводиться
по следующим этапам:[[4]]
- Во-первых, приготовление водного раствора, вид которого
зависит от выбора электрофоретического буфера (например, трис – ацетатный,
трис – фосфатный, трис – боратный). Конечная рН водного раствора должна
составлять 8,0;
- Одновременно с приготовлением водного раствора выбранный
буфер при помощи нагревания готовит расплав агарозы с концентрацией 0,4 –
2,0 %;
- Полученный расплав агарозы остужают до 50 градусов, после
чего в него добавляют краситель – бромистый этидий в концентрации, которая
требуется для дальнейшей визуализации дифференцированных молекул во время
ультрафиолетового излучения. Длина волны УФ – света должна составлять 254
нм;
- В горизонтальную кювету помещается 50-ти градусный расплав
агарозы, где в последующем за счет гребенки образуются углубления для
внесения препаратов ДНК. В подобном состоянии расплав агарозы оставляется
до момента достижения консистенции геля;
- После застывания гелеобразных лунок с добавленными
препаратами ДНК, кювету помещают в электрофоретическую ванну;
- Одновременно приготавливается навеска гексилрезорцина,
который включается в электрофоретический буфер до момента достижения
высшей концентрации, составляющей 10-3 М (0,194 г/л). Именно
гексилрезорцин или С6 – алкилоксибензол проявляет наиболее выраженные
фотопротекторные свойства;
- Буфер с содержанием указанного выше количества и
концентрации С6 – алкилоксибензола, погружается также на на
электрофоретическую ванну;
- Электрофоретическая ванна соединяется с источником света,
на котором заранее установлены показатели режимов электрофореза;
- Источник тока отключается только после прошествии
некоторого времени от разделения препаратов ДНК, что определяется
получением частиц с разными характеристиками. После разделении молекул ДНК
и отключения источника тока гелеобразную массу агарозы переносят на
трансиллюминатор;
- На поверхности трансиллюминатора под воздействием УФ –
излучения происходит детализации полученного разделения молекул ДНК, и
создание документов при помощи цифровых устройств;
- Последним, заключающим этапом является, вырезание участка
геля из агарозы с разделенным молкулами ДНК, для проведения последующих
генно – инженерных исследований.»[4]
Полимеразная цепная реакция
(ПЦР) - метод, имитирующий естественную репликацию ДНК, "invitro"
аналог биохимической реакции синтеза ДНК в клетке. ПЦР позволяет найти в
исследуемом материале небольшой участок генетической информации, заключенный в
специфической последовательности нуклеотидов ДНК любого организма среди
огромного количества других участков ДНК и многократно размножить его. ПЦР
позволяет получить количество ДНК, достаточное для детекции.
Область применения:
·
диагностика инфекционных заболеваний;
·
диагностика онкологических заболеваний;
·
диагностика генетических заболеваний;
·
идентификация личности;
·
диагностика патогенов в пище;
·
диагностика ГМО и др.
ПЦР - метод молекулярной
диагностики, ставший для ряда инфекций «золотым стандартом», проверен временем
и тщательно апробирован клинически. Метод ПЦР позволяет определить наличие
возбудителя заболевания, даже если в пробе присутствует всего несколько молекул
ДНК возбудителя.[[5]]
ПЦР позволяет диагностировать
наличие долго растущих возбудителей, не прибегая к трудоёмким
микробиологическим методам, что особенно актуально в гинекологии и урологии при
диагностике урогенитальных инфекций, передающихся половым путем (ИППП).[5]
Также, этим методом проводят
диагностику вирусных инфекций, таких как гепатиты, ВИЧ и др. Чувствительность
метода значительно превосходит таковую у иммунохомических и микробиологических
методов, а принцип метода позволяет диагностировать наличие инфекций со
значительной антигенной изменчивостью.[5]
Специфичность ПЦР при
использовании технологии PCR даже для всех вирусных, хламидийных,
микоплазменных, уреаплазменных и большинства других бактериальных инфекций
достигает 100%. Метод ПЦР позволяет выявлять даже единичные клетки бактерий или
вирусов. ПЦР-диагностика обнаруживает наличие возбудителей инфекционных
заболеваний в тех случаях, когда другими методами (иммунологическими,
бактериологическими, микроскопическими) это сделать невозможно.[5]
Особенно эффективен метод ПЦР
для диагностики трудно культивируемых, некультивируемых и скрыто существующих
форм микроорганизмов, с которыми часто приходится сталкиваться при латентных и
хронических инфекциях, поскольку этот метод позволяет избежать сложностей,
связанных с выращиванием таких микроорганизмов в лабораторных условиях.[5]
Применение ПЦР-диагностики также
очень эффективно в отношении возбудителей с высокой антигенной изменчивостью и
внутриклеточных паразитов. Методом ПЦР возможно выявление возбудителей не
только в клиническом материале, полученном от больного, но и в материале,
получаемом из объектов внешней среды (вода, почва и т. д.). В урологической и
гинекологической практике - для выявления хламидиоза, уреаплазмоза, гонореи,
герпеса, гарднереллёза, микоплазменной инфекции, ВПЧ - вирусов папилломы
человека; в пульмонологии - для дифференциальной диагностики вирусных и
бактериальных пневмоний, туберкулёза; в гастроэнтерологии - для выявления
хеликобактериоза; в клинике инфекционных заболеваний - в качестве
экспресс-метода диагностики сальмонеллёза, дифтерии, вирусных гепатитов В, С и
G; в гематологии - для выявления цитомегаловирусной инфекции, онковирусов.
Специфичность ПЦР основана на
образовании комплементарных комплексов между матрицей и праймерами - короткими
синтетическими олигонуклеотидами длиной 18 - 30 букв. Каждый из праймеров
сопоставим (комплементарен) с одной из цепей двуцепочечной матрицы, обрамляя
начало и конец амплифицируемого участка. После соединения (гибридизации)
матрицы с праймером (отжиг), последний служит затравкой для ДНК-полимеразы при
синтезе комплементарной цепи матрицы.[5]
Для проведения ПЦР в простейшем
случае требуются следующие компоненты:
·
ДНК-матрица, содержащая тот участок ДНК, который требуется
амплифицировать;
·
два праймера, комплементарные концам требуемого фрагмента;
·
термостабильная ДНК-полимераза;
·
дезоксинуклеотидтрифосфаты (A, G, C, T);
·
ионы Mg2+, необходимые для работы полимеразы;
·
буферный раствор.
ПЦР проводят в амплификаторе —
приборе, обеспечивающем периодическое охлаждение и нагревание пробирок, обычно
с точностью не менее 0,1°C. Чтобы избежать испарения реакционной смеси, в
пробирку добавляют высококипящее масло, например, вазелиновое. Добавление
специфичеких ферментов может увеличить выход ПЦР-реакции.[5]
·
«образец ДНК - молекулыднккоторые нужно разделить либо определить
их размер, объем 10-20 мкл
·
электрофорезная камера . Камеру можно купить , но можно и
сделать самому.Камера - это просто герметично склеенная коробочка из оргстекла
с 2-я штекерами в которые вставляется питание, самое проблематичное здесь - это
подобрать блок питания.
·
Источник питания на 50 - 150 В
·
Гель - готовый или сделанный самостоятельно Для приготовления
1% геля: 100 мл воды и 1 грамм агарозы
·
буфер TAE(Tris-acetate-EDTA), который в разбавленном виде
заливается в камеру, объем в зависимости от размеров камеры
·
Loadingbuffer - обычно глицерин, объем 1 мкл
При нанесении в лунки днк ,она сама по себе туда не опуститься, всплывет и
рассеится по буферу. Чтобы этого не произошло и нужен глицерин или
чтонибудьдругое тяжелое.
·
Loadingdye - краситель , объем 1 мкл
Не обязателен, но позволяет визуально наблюдать за ходом электрофореза ( днк он
конечно не покажет )
·
DNA ladder - маркер, по объему - столько же сколько и образца
Необходим для определения размера образца.Маркер - фрагменты ДНК ,
определенного размера.
Бывают разныеDnaLadder 100 , 50 , 25. DnaLadder 100 - набор фрагментов от 100
нуклеотидов до 1000 с шагом в 100. Обычно наносятся в первую лунку и получаются
в виде лесенки. Если нужно только узнать наличие\отсутствие днк в образце , то
можно и без маркера. В маркер не нужно добавлять ни Loadingbuffer ни
Loadingdye.
·
Трансиллюминатор или ультрафиолетовая лампа(например бытовая
люминесцентная черная)Для визуализации подкрашенной этидиумом ДНК.»[[6]]
«1. Готовят 1 х ТБЭ в объеме, достаточном для заполнения
камеры для электрофореза и приготовления геля.
2.Добавляют к 1 х ТБЭ агарозу в количестве, необходимом для
получения 0,35—0,45% (в/о) раствора, и нагревают в микроволновой печи до
полного расплавления агарозы.
3. Охлаждают смесь до +/- 50 °С.
4.Добавляют к раствору агарозы бромистый этидий до конечной
концентрации 0,5 мкг/мл и осторожно перемешивают, избегая появления в геле
пузырьков воздуха.
5. Теплую агарозу выливают в кювету для геля и равномерно
распределяют ее по кювете. Вертикально вставляют гребенку так, чтобы ее зубцы
не доставали до дна примерно 1,5 мм.
6. Оставляют кювету с агарозным гелем на 30 мин, затем
осторожно удаляют гребенку и липкую ленту. Кювету с гелем помещают в
электрофорезную камеру, содержащую необходимое количество 1 х ТБЭ с бромистым
этидием в конечной концентрации 0,5 мкг/мл.
7. Подготавливают к электрофорезу образцы исследуемой и
маркерной ДНК, для чего смешивают их с буфером для нанесения (5:1, о/о). Чтобы
получить четкий сигнал при окрашивании бромистым этидием-EtBr, в лунку шириной
5 мм достаточно внести 200 нг маркерной ДНК. Для построения стандартной кривой
необходимо использовать маркерные фрагменты, длина которых примерно равна длине
исследуемой ДНК.
(EtBr при форезе движется от (+) к (-). Если хочется, чтобы
он не уходил из геля, лучше ввести его и в форезный буфер.)
8. Осторожно вносят в лунки исследуемую и маркерную ДНК.для
повышения точности определения размера маркерную ДНК наносят по обе стороны от
исследуемой.
9. Проводят электрофорез при градиенте напряженности 1—3 В
на 1 см геля в течение 1—3 ч.
10. Просматривают гель в УФ-свете на транс иллюминаторе и
фотографируют.»[[7]]
«1. ВЗЯТИЕ, ПРЕДВАРИТЕЛЬНАЯ ОБРАБОТКА, ДОСТАВКА и ХРАНЕНИЕ
МАТЕРИАЛА
1.1. Исследуемый материал (мокрота, плевральная жидкость,
моча, бронхоальвеолярный лаваж, промывные воды бронхов и др.экссудаты) в
количеств 10 мл собрать в пластиковую центрифужную пробирку объемом 50 мл с
плотно завинчивающейся крышкой.
1.1.2. Для разжижения мокроты или плевральной жидкости :
1.1.2.1. Приготовить смесь NALC следующего состава ( на 5
проб мокроты):
0.25 г ацетил-цистеина, 25 мл 4% NaOH, 25 мл 0.1М триNa
цитрата Смесь готовят в день использования (раствор не хранится).
1.1.2.2. К образцу в пробирке добавить равный объем NALC,
перемешать на вортексе в течение 5-20 секунд, инкубировать 15 минут при
комнатной температуре, а затем развести 0.067М фосфатным буфером (рН 6.8) до
50 мл;
1.2. Центрифугировать 15 минут при 3000 об/мин, удалить
надосадочный раствор вакуумным аспиратором в колбу-ловушку с дез.раствором.
Осадок использовать для выделения ДНК.
1.3. К осадку в пробирке добавить 100 мкл дистиллированной
воды, пробирку плотно закрыть, перемешать на вортексе, и перенести весь объем
суспензии в чистую полипропиленовую пробирку типа Эппендорфф объемом 1,5 мл.
Неохлажденные обработанные образцы использовать в течение
2-х часов для выделения ДНК. Допускается хранение при +4…+8оС не более 1 суток,
при –18…-20оС—не более 2-х недель.
Доставка обработанных проб в лабораторию должна проводиться
в термосе со льдом или в термоконтейнере в течение 12 часов.
2. ВЫДЕЛЕНИЕ ДНК ИЗ БИОПРОБ
2.1. Пробы (осадок в 100 мкл воды) прогреть 20 мин при
температуре 95оС.
2.2. К пробе добавить 300 мкл раствора I и 20 мкл суспензии
сорбента. Суспензию сорбента перед использованием необходимо тщательно
перемешать до полной гомогенности.) Пробирки плотно закрыть.
2.3. Пробы инкубировать в течение 10 минут при комнатной
температуре, 1-2 раза перемешивая на вортексе.
2.4. Центрифугировать в течение 15 сек на микроцентрифуге
при 8-12 тыс.об/мин., супернатант удалить вакуумным аспиратором в
колбу-ловушку, с использованием одноразовых наконечников,.
2.5. К осадку добавить 100 мкл раствора II, пробирки плотно
закрыть и встряхнуть на вортексе. Сорбент осадить центрифугированием при 8-12
тыс.об/мин. в течение 15 секунд. Супернатант удалить вакуумным аспиратором в
колбу-ловушку.
2.6. Процедуру отмывки (добавление раствора, встряхивание на
вортексе и осаждение центрифугированием) повторить еще два раза с
использованием 1.0 мл раствора III для промывки.
2.7. Дополнительным центрифугированием при 8-12 тыс.об.мин.,
с последующим отбрасыванием супернатанта убрать остатки раствора III.
2.8. Пробирки поместить в твердотельный термостат и
подсушить пробы 5 мин при температуре 45-55оС, оставляя пробирки открытыми.
Внимание! На всех стадиях обработки клинического материала
удаление супернатанта производят одноразовыми пластиковыми наконечниками при
помощи вакуумного аспиратора в колбу-ловушку, содержащую дезинфицирующий
раствор (3% хлорамин или 5% перекись водорода и т.п.)
2.9. В пробирки с сорбентом добавить 50 мкл ТЕ буфера,
пробирки плотно закрыть, перемешать на вортексе и инкубировать в течение 5
минут при 45-55оС в твердотельном термостате.
2.10. Пробирки центрифугировать 15 сек при 8-12 тыс.об/мин,
водную фазу (супернатант) использовать в качестве исследуемого образца ДНК для
постановки реакции амплификации.
Раствор ДНК (супернатант, перенесенный с осадка сорбента в
чистую пробирку), можно хранить при температуре +4…+8оС в течение недели или
при температуре -20оС в течение 6 месяцев.
3. ПРОВЕДЕНИЕ ПЦР (амплификация)
3.1. Приготовить и пронумеровать пробирки для проведения
амплификации вместимостью 0,5 мл (или 0,2 мл) в соответствии с количеством
анализируемых проб. Подготовить и промаркировать пробирки для положительного
(маркировка «К+») и отрицательного (маркировка «К-») контрольных образцов.
3.2. За 20-30 минут до приготовления рабочей
амплификационной смеси извлечь комплект реагентов для ПЦР (амплификации) из
морозильника, разморозить содержимое (желательно поместить пробирку с
Taq-полимеразой в ледяную баню). Пробирки с реакционной смесью и полностью
размороженным раствором разбавителя тщательно
встряхнуть для перемешивания содержимого.
3.3. Из компонентов набора приготовить смесь реагентов для
амплификации из расчета на 1 пробу:
Рекомендуется готовить смесь реагентов не менее чем на 5
реакций для достоверной дозировки объема фермента17,5 мкл разбавителя, 2,5 мкл
реакционной смеси, 0,2 мклTaq-полимеразы
При приготовлении рабочей амплификационной смеси необходимо
все компоненты добавлять отдельными наконечниками.
3.4. После добавления Taq-полимеразы, которое производится в
последнюю очередь, необходимо тщательно перемешать смесь пипетированием.
3.5. Добавить по 20 мкл рабочей амплификационной смеси во
все пробирки, подготовленные для амплификации.
3.6. Добавить во все пробирки по 1 капле (около 25 мкл)
минерального масла.
3.7. Внести 5 мкл образца из обработанной анализируемой
пробы (см п. выделение ДНК) в соответствующую пробирку с рабочей амплификационной
смесью под слой масла.
3.8. Внести в пробирки для положительных контрольных
образцов по 5 мкл положительного контрольного образца ДНК, а в пробирку для
отрицательного контрольного образца – 5 мкл разбавителя , используя
индивидуальные наконечники с фильтрами.
3.9. Пробирки закрыть и центрифугировать в течение 3-5
секунд при 1,5– 3000 об/мин при
комнатной температуре (+18...+25оС) на
микроцентрифуге-вортексе.
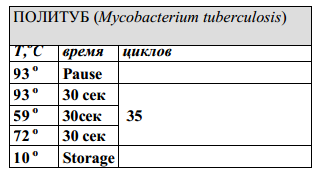
3.10. Перенести пробирки в прогретый до температуры +93оС
(установившаяся температура в режиме Пауза) программируемый термостат
(амплификатор) и провести амплификацию по
следующей программе:»[[8]]
По окончания занятий по большому
практикуму были выполнены следующие задачи:
1. Проанализирована научная
литература.
2. Отработаны методы
Электрофореза и ПЦР
[1] Колчанов Н. Перспективные исследования генетических
макромолекул [Электронный ресурс]. Режим доступа:
#"#_ednref2" name="_edn2" title="">[2]Стручкова И.В.; Кальясова Е.А. Теоретические и
практические основы проведения электрофореза белков в полиакриламидном геле //
И.В. Стручкова Е.А. Кальясова – 2012 С6
[3] Обнаружение единичных нуклеотидных замен в ДНК:
расщепление РНКазой и денатурирующий градиентный гель-электрофорез
[Электронный ресурс]. Режим доступа:
#"#_ednref4" name="_edn4" title="">[4] Электрофорез и генетика [Электронный ресурс]. Режим
доступа: #"#_ednref5" name="_edn5" title="">[5] Полимеразная цепная реакция [Электронный ресурс].
Режим доступа: https://www.invitro.ru/for-clients/mat/1133/(Дата обращения)
18.11.14
[6] Электрофорез ДНК в агарозном геле [Электронный
ресурс]. Режим доступа: #"#_ednref7" name="_edn7" title="">[7] Гель-электрофорез ДНК [Электронный ресурс]. Режим
доступа: #"#_ednref8" name="_edn8" title="">[8] МЕТОДИКА проведения исследования клинического
материала на наличие ДНК микобактерий туберкулезного комплекса методом ПЦР. ОО
НПФ «Литех"