Экстракция редкоземельных элементов
Реферат
Ключевые слова: экстракция, моделирование, азотная кислота, аммиачная
селитра, редкоземельные элементы, тбф.
Изучен процесс совместной экстракции редкоземельных элементов в
экстракционной системе H2O - HNO3 - NH4NO3 - Ln(NO3)3 - ТБФ 100%, определен
состав и стехиометрия экстрагируемых комплексов.
Создана база данных по совместной экстракции лёгких РЗЭ в присутствии NH4NO3, HNO3 и ТБФ.
Построена математическая модель процессов экстракции, определены
константы экстракции и параметры неидеальности.
Содержание
Реферат
Введение
1. Аналитический обзор
1.1 Определение понятия редкоземельных элементов. Их
физические и химические свойства
.2 Электронная конфигурация РЗЭ
.3 Применение редкоземельных элементов
.4 Экстракция редкоземельных элементов
.5 Экстракционное разделение РЗЭ трибутилфосфатом
.6 Метод моделирования процесса экстракции
2. Цели и задачи
. Экспериментальная часть
3.1 Приготовление и анализ растворов
.1.1 Определение плотности ТБФ
.1.2 Определение плотности аммиачной селитры
.1.3 Определение плотности и концентрации раствора суммы
РЗЭ
.2 Проведение экстракции и реэкстракции
.3 Результаты и их обсуждение
.3.1 Серия 1 с концентрацией суммы РЗЭ в водной фазе 0,0195
- 1,93 М и концентрацией аммиачной селитры 8,08 - 0 М
.3.2 Серия 2 с концентрацией суммы РЗЭ в водной фазе 0,030
- 2,52 М и концентрацией аммиачной селитры 5,75 - 0 М
.3.3 Серия 3 с концентрацией суммы РЗЭ в водной фазе 0,010
- 1,61 М и концентрацией аммиачной селитры 5,79 - 0 М
.3.4 Серия 4 с концентрацией суммы РЗЭ в водной фазе 0,0542
- 2,52 М и концентрацией аммиачной селитры 2,29 - 0 М
.3.5 База данных по совместной экстракции РЗЭ в системе H2O
- HNO3 - NH4NO3 - Ln(NO3)3
- ТБФ 100%
Заключение и выводы
Список использованных источников
Приложения
Введение
Научно-технический процесс, достигнутый за последние годы в химии во
многом обязан успешному применению материалов, в основе которых лежат редкие
элементы. Они играют огромную роль в металлургии, машиностроении, атомной
промышленности, авиастроении и других отраслях промышленности. РЗЭ обладают
многими уникальными свойствами, отличающими их от других металлов.
Успешное решение проблемы охраны биосферы, снижение отрицательного
влияния индустриализации на состояние природной среды и многие другие
глобальные проблемы непосредственно связаны с разработкой эффективных методов
анализа. Состояние методов избирательного определения металлов не всегда
удовлетворяет требованиям к нижним границам определяемых содержаний. Постоянно
ощущается необходимость в простых по выполнению, точных, чувствительных
методиках, которые позволяли бы определять компонент в сложной по составу
смеси. Для решения этой проблемы ученые привлекли методы концентрирования,
которые позволили в значительной степени устранить сложные ситуации. Более
того, в некоторых случаях концентрирование расширило пределы применимости
инструментальных методов (атомно-абсорбционной спектрометрии, хроматографии,
спектрофотометрии, вольтамперометрии).
Одним из перспективных методов разделения и концентрирования является
экстракция.
Экстракция - это процесс распределения вещества между двумя
несмешивающимися растворителями. Одним из них обычно является вода, вторым -
органический растворитель. Будучи гетерогенным процессом, экстракция
подчиняется правилу фаз Гиббса. Выполнение экстракционного разделения и
концентрирования обычно не требует сложного и дорогостоящего оборудования,
однако, это сложный физико-химический процесс.
Теория экстракции находится на стыке различных разделов химии: химической
термодинамики, теории растворов, химической кинетики, органической химии и
координационной химии. Для описания экстракционных процессов необходимо также
использовать теорию массопереноса. Задача экстракции состоит в том, чтобы полно
и селективно перевести компонент из водной фазы в органическую. Для этого
необходимо подобрать условия образования подходящих соединений (например,
комплексов металлов), в виде которых компонент может находиться в органической
фазе.[1]
Современные экстракционные методы достаточно универсальны. Трудно найти
типы соединений, которые нельзя было бы экстрагировать. С помощью экстракции
можно разделять многокомпонентные системы, причем эффективнее и быстрее, чем
это достигается другими методами. Экстракционные методы пригодны для
абсолютного и относительного концентрирования, извлечения в экстракт
микроэлементов или матрицы, индивидуального и группового выделения элементов.
Приведенные в настоящей работе экспериментальные данные,
физико-химические и математические модели, параметры фазовых экстракционных
равновесий могут быть использованы при разработке новых технологий
экстракционного разделения и очистки РЗМ, а также представляют собой справочный
материал.
1. Аналитический обзор
1.1 Определение
понятия редкоземельных элементов. Их физические и химические свойства
Редкие элементы - это относительно малораспространенные в природе
химические элементы (ориентировочно с кларками ниже 0,01 % по массе). Перечень
редких элементов точно не установлен и различен у разных авторов.
На основании особенностей геохимии и технологии выделения редкие элементы
делят на группы :
легкие
- Li, Cs, Be, Sr ;
редкоземельные элементы - Y, La и лантаноиды, к ним относят и Sc ;
тугоплавкие - Zr, Nb, Та, Mo, W и др. ;
рассеянные элементы - Cd, Ga, In, Tl, Ge, Se, Те и др. (к рассеянным
часто относят также легкий редкий элемент Rb, редкоземельный Sc и тугоплавкие
Hf и Re) ;
платиновые металлы (Ru, Rh, Pd, Os, Ir,Pt),
радиоактивные элементы (U, Th и др.) ;
благородные газы.
Традиционно относят к редким элементам Ti, хотя для этого нет достаточных
оснований - природные запасы его значительны и добывается он в больших
количествах. Иногда из числа редких исключают Mo, W, V, Li и включают Bi и
другие.
Таким образом, редкоземельные элементы - это группа из 17 элементов,
включающая лантан, скандий, иттрий и лантаноиды, относящаяся к редким
элементам. Рассмотрим физические свойства представителей данной группы
элементов.
Лантаноиды - металлы серебристо-белого цвета. Некоторые из них имеют
слегка желтоватый цвет (например, празеодим, неодим). Большая часть металлов
кристаллизуется в плотной гексагональной или гранецентрированной кубической
решетке. Исключение составляют самарий (ромбоэдрическая структура) и европий
(объёмно-центрированная кубическая структура).
У церия, лантана, празеодима, скандия, а также, вероятно, у неодима,
самария, эрбия и иттербия имеются аллотропические модификации. Вследствие
замедленного протекания модификационных превращений в слитках церия, лантана и
празеодима часто наблюдаются две фазы, отвечающие различным типам структур.
Необходимо отметить весьма высокие сечения захвата тепловых нейтронов у
некоторых элементов: гадолиния, самария, европия. По сечению захвата гадолиний
превосходит почти все элементы. Для сопоставления укажем, что применяемые для
регулирования работы ядерных реакторов кадмий и бор имеют сечения захвата
тепловых нейтронов соответственно 2500 и 715 барн.
Обращает на себя внимание, что у элементов Sm, Eu и Yb, проявляющих
валентность (2 +), точки кипения значительно ниже, чем у всех других элементов
группы.
Редкоземельные металлы высокой чистоты пластичны и имеют твердость
порядка 20-30 единиц по Бринелю. Твердость возрастает по мере увеличения
атомного номера. Наиболее пластичными являются иттербий и самарий.
Механические свойства весьма сильно зависят от содержания примесей.
Редкоземельные металлы имеют сравнительно низкую электропроводность. У лантана,
при температуре 4,7 К наблюдается сверхпроводимость. Все редкоземельные металлы
парамагнитны, но некоторые из них проявляют ферромагнитные свойства (гадолиний,
диспрозий, гольмий).
Известно более 200 изотопов редкоземельных элементов. Из них 54
встречаются в природной смеси элементов, остальные изотопы получены
искусственно и являются радиоактивными.
Скандий, иттрий и лантаноиды имеют высокую реакционную способность.
Рассмотрим химические свойства РЗЭ и их соединений.
Редкоземельные металлы и иттрий химически активны : во влажном воздухе
тускнеют, покрываясь пленкой окисла. Элементы иттриевой подгруппы значительно
устойчивее на воздухе, чем элементы цериевой подгруппы.
Редкоземельные металлы - хорошие восстановители ; восстанавливают многие
окиси до металла (окись железа, окись марганца и др.). CO и CO2 восстанавливаются церием при красном
калении до углерода. РЗЭ и Y со
многими металлами и неметаллами образуют сплавы и интерметаллические
соединения. Лантан, церий и другие металлы уже при обычной температуре
реагируют с водой и кислотами - не окислителями, выделяя водород. Из-за высокой
активности к атмосферному кислороду и воде куски лантана, церия, иттрия и др.
следует хранить в парафине.
Химическая активность редкоземельных металлов неодинакова. От скандия до
лантана химическая активность возрастает, а в ряду лантан - лютеций -
снижается. Отсюда следует, что наиболее активным металлом является лантан. Это
обуславливается уменьшением радиусов атомов элементов от лантана до лютеция с
одной стороны, и от лантана до скандия - с другой.
Окислы
Окислы РЗЭ получают, прокаливая гидроокиси, карбонаты, оксалаты, соли
некоторых других кислот при (800 - 1200) °C. Если реакция идет на воздухе, то получаются окислы Ln2O3, и только соединения церия, празеодима, тербия в этих
условиях образуют высшие окислы CeO2, Pr6O11, Tb4O7. Все окислы РЗЭ - очень прочные соединения. Имеют
высокие теплоты образования, что отличает их от окислов других металлов. Окислы
могут быть получены в виде аморфного порошка или с хорошо выраженной
кристаллической структурой. Некоторые из них кристаллизуются в решетке
гексагонального типа, некоторые имеют кубическую решетку.
Гидроокиси
Гидроокиси типа Y(OH)3 и Ln(OH)3 выпадают в виде аморфных осадков от действия
солей иттрия и РЗЭ на водные растворы аммиака или щелочей. Гидроокиси хорошо
растворяются в соляной, азотной и серной кислотах, образуя соли.
Основные свойства гидроокисей заметно понижаются с уменьшением объема
атомов РЗЭ ; чем меньше радиус иона Ln3+, тем прочнее он удерживает ионы OH-. Гидроокиси РЗЭ в некоторой степени амфотерны.
Сульфаты
Гидратированные сульфаты иттрия, лантана и лантаноидов состава Ln2(SO4)3·nН2O
могут быть получены растворением оксидов, гидроксидов или карбонатов в
разбавленной серной кислоте с последующим упариванием растворов. Сульфаты
выделяются с различным содержанием кристаллизационной воды. Безводные сульфаты
можно получить, нагревая гидратированные сульфаты до (600 - 650) єС, иттрия -
до 400 єС. Сульфаты растворяются в воде. Растворимость уменьшается с повышением
температуры. Сульфаты РЗЭ склонны к образованию пересыщенных растворов. В этом
они сходны с сульфатами кальция и натрия. Двойные сульфаты РЗЭ иттриевой
подгруппы значительно растворяются, сульфаты тербия занимают промежуточное
положение. Различие в растворимости двойных сульфатов используется для
предварительного разделения лантаноидов на две подгруппы.
Нитраты(NO3)3 получают, действуя на оксиды иттрия и
лантаноидов жидким оксидом азота. В виде кристаллогидратов нитраты получают,
растворяя оксиды, гидроксиды, карбонаты в азотной кислоте и затем упаривая
растворы :
Ln2O3 + 6HNO3 = 2Ln(NO3)3
+ 3H2O, (1)2(CO3)3 + 6HNO3
= 2Ln(NO3)3 + 3H2O + 3CO2. (2)
Выделяются они с различным числом молекул кристаллизационной воды. Лучше
кристаллизуются нитраты цериевой подгруппы, труднее - иттриевой. Растворимость
нитратов в воде и азотной кислоте от лантана до гадолиния уменьшается, а затем
снова возрастает. Имеется некоторая закономерность в окраске ионов. Нитраты
иттрия способны образовывать двойные соединения с нитратами аммония, щелочных,
щелочноземельных и других металлов. Двойные нитраты применялись при разделении
РЗЭ фракционной кристаллизацией, до появления современных методов.
Фосфаты
Метафосфаты иттрия и лантаноидов Ln(PO3)3 получают,
растворяя сульфаты в расплавленной метафосфорной кислоте. Они не растворяются в
воде и в разбавленных минеральных кислотах.
Безводные ортофосфаты LnPO4 получают, сплавляя оксиды с
метафосфатом щелочного металла и затем обрабатывая охлажденный сплав водой.
Безводный ортофосфат иттрия встречается в природе в виде минерала ксенотима.
Ортофосфаты не растворяются в воде и разбавленных минеральных кислотах.
Гидратированные ортофосфаты образуются, если действовать на водные
растворы солей иттрия, лантана и лантаноидов фосфорной кислотой. Полученные
соединения LnPO4 · nH2O хорошо растворяются в разбавленных
минеральных кислотах.
Все соли LnPO4 · nH2O термически устойчивы.
Устойчивость закономерно повышается от солей празеодима к солям иттербия.
Также РЗЭ образуют пирофосфаты - LnHP2O7,
диметилфосфаты - Ln[(CH3)2PO4]3.
Карбонаты
Средние карбонаты иттрия и лантаноидов Ln2(CO3)3
получают в виде аморфных или кристаллических осадков, действуя на водные
растворы их солей разбавленными растворами карбонатов натрия, калия и аммония,
взятых в стехиометрическом количестве. При нагревании выпадают смеси средних и
основных карбонатов. Средние карбонаты при нагревании в присутствии воды
гидролизуются, переходя в основные карбонаты :
Ln2(CO3)3 + 2H2O
Ln(OH)CO3 + H2CO3. (3)
Поведение карбонатов при медленном нагревании аналогично поведению
сульфатов и нитратов. Сначала они теряют кристаллизационную воду, затем CO2.
При дальнейшем нагревании образуются окиси. Карбонаты могут служить исходным
материалом для получения окисей и других соединений РЗЭ.
Помимо всех вышеперечисленных соединений, РЗЭ образуют хроматы, силикаты,
молибдаты, вольфраматы, галогениды, соли органических кислот, а также
комплексные соединения.
1.2 Электронная
конфигурация РЗЭ
К группе редкоземельных элементов или лантаноидов относятся
элементов с порядковыми номерами от 58 (церия) до 71 (лютеция),
расположенных в периодической системе за лантаном и сходных с ним по свойствам.
Поэтому в эту группу обычно включают и лантан. Кроме того, к редкоземельным
элементам примыкают химические аналоги лантана - скандий и иттрий, которые
почти всегда содержатся вместе с лантаноидами в минеральном сырье.
По физико-химическим свойствам лантаноиды весьма близки между собой. Это
объясняется особенностями строения их электронных оболочек. Как известно,
химические и ряд физических свойств элементов определяются преимущественно
строением внешних электронных уровней. Электронные конфигурации атомов
лантаноидов могут быть представлены формулой 1s22s2p63s23p63d104s24p64d104fn5s25p65dm6s2, где n
изменяется от 0 до 14, а m
равно 0 или 1. Энергии электронных уровней 5d и 4f близки, однако 5d-электроны имеются только у четырех элементов - лантана, церия, гадолиния
и лютеция. У ионизированных атомов f-электроны связаны с ядром более прочно,
чем d-электроны. По этой причине трижды
ионизированные атомы РЗМ имеют только 4f-электроны, а 5d и 6s электроны удаляются.[2]
По мере увеличения заряда ядра (увеличение порядкового номера) структура
двух внешних электронных уровней (оболочки О и Р) у атомов лантаноидов почти не
изменяется, так как дополнительные электроны заполняют более глубоко лежащий 4f -уровень.
У цезия и бария - элементов, предшествующих лантану, электроны заполняют
внешний 6s уровень, в то время как слои 4f, 5d и 5f
остаются незаполненными. У следующего за барием лантана дальнейшее заполнение
шестого уровня (Р-оболочка) прерывается, так как энергетически более выгодным
оказывается положение электрона на 5d-уровне.
Степень окисления +3 лантана обусловлена участием в валентных связях двух
6s-электронов и одного 5d-электрона.
При этом ион La3+ приобретает электронную конфигурацию ксенона (8
электронов на О -оболочке). После лантана происходит заполнение электронами
слоя 4f, которое начинается у церия и
заканчивается у лютеция (максимальное количество электронов на f-уровне - четырнадцать). При этом в
нормальном состоянии у всех лантаноидов (за исключением гадолиния и лютеция)
нет 5d-электронов.
Электроны 4f-уровня
относительно свободны от действия внешних влияний, например от действия полей
соседних атомов, так как они экранированы электронами внешних оболочек. Это
обусловливает сходство большинства редкоземельных элементов в химическом
отношении и резкие полосы поглощения в инфракрасной, видимой и ультрафиолетовой
частях спектра, характерные для лантаноидов.
Электроны 4f не принимают
участия в образовании химических связей. Однако для перехода одного электрона
из слоя 4f в слой 5d требуется небольшая затрата энергии.
Характерная для всей группы редкоземельных элементов валентность (3+)
основана на возбужденных достояниях 5d1 6S2 или 5d2
6s1, возникающих в результате перехода одного электрона с уровня 4f
на уровень 5d. Некоторые лантаноиды проявляют, кроме валентности (3+), также
валентность (4+) и (2+). Эти «аномальные» валентности объясняются различиями в
структуре электронных оболочек. Известно, что прочность связи электрона
возрастает по мере заполнения электронного f - уровня наполовину (при
заполнении его до семи электронов) или при полном его заполнении до 14
электронов. Поэтому валентность (4 +) проявляется у церия и празеодима (первые
f - электроны слабей удерживаются) и у тербия и диспрозия, следующих за
гадолинием, у которого f-оболочка заполнена наполовину. Валентность (2+)
наблюдается у самария (оболочка f почти заполнена наполовину), европия (7
электронов на f - уровне) и у тербия (14 электронов на f-уровне). Вследствие
сравнительной устойчивости электронов на f-оболочке у этих элементов переход f
- электронов на d-уровень требует большей затраты энергии. Поэтому в валентной
связи в ряде случаев могут принять участие только внешние два электрона
6s-уровня.
Заполнение электронами 4f - уровня по мере увеличения заряда ядра
сопровождается уменьшением радиуса атомов и ионов лантаноидов. Это явление,
известное под названием «лантаноидного сжатия», также приводит к небольшим
различиям в свойствах этих элементов, в частности объясняет некоторое понижение
основного характера элементов в направлении от церия к лютецию, обусловливает различия
в растворимости солей и устойчивости комплексных соединений.
Редкоземельные элементы обычно подразделяют на две группы: цериевую (La, Ce, Pr, Nd, Pm, Sm, Eu) и иттриевую (Gd, Tb, Dy, Ho, Er, Yb, Lu,
Y). Это деление, которое
первоначально было основано на различии растворимости двойных сульфатов,
образуемых сульфатами лантаноидов с сульфатами натрия или калия, согласуется и
с некоторыми различиями в физических свойствах металлов обеих групп. Однако
между двумя группами нет отчетливых границ, и европий часто включают в группу
иттрия.
В последнее время в литературе принят термин легкие лантаноиды (элементы
от лантана до гадолиния) и тяжелые лантаноиды (от тербия до лютеция).
Деление РЗЭ на две подгруппы можно объяснить электронной структурой
оболочки 4f.
По правилу Хунда, в пределах данного значения побочного квантового числа
электроны стремятся расположиться так, чтобы число неспаренных электронов с
параллельными спинами и суммарный спинмомент были максимальны. В согласии с
этим правилом у первых семи элементов (от церия до гадолиния) спины электронов
на 4f - уровне параллельны, а у последующих элементов (от тербия до лютеция)
происходит заполнение электронами с антипараллельными спинами.
Среди свойств лантаноидов, объясняющихся их электронной структурой,
следует отметить парамагнетизм и высокие значения парамагнитной восприимчивости
(парамагнитная восприимчивость обусловлена наличием неспаренных электронов на f
- оболочке). Это обусловлено экранированием магнитноактивного 4f - уровня
электронами внешних оболочек.
1.3 Применение
редкоземельных элементов
Практическое использование РЗМ началось во второй половине XIX века. Однако соединения РЗМ
применялись лишь в производстве газокалильных сеток или колпачков для
осветительных газовых и керосиновых фонарей.
Расширение областей использования РЗЭ связано с развитием
аэрокосмической, электронной, нефтехимической, атомной и других отраслей
промышленности.
Рассмотрим некоторые области применения РЗЭ и их соединений.
Металлургия
Использование РЗМ в металлургии основано на их высоком химическом
сродстве к кислороду, сере, азоту и водороду, примеси которых ухудшают свойства
сталей, сплавов и цветных металлов. При взаимодействии РЗМ с этими элементами
происходит очистка расплава за счет образования прочных тугоплавких соединений,
что вызывает в свою очередь резкое повышение механических свойств легируемых
металлов у сплавов.
Успешному применению РЗМ в металлургии способствуют также невысокое
давление насыщенного пара при температуре плавления чугунов и сталей, высокие
температуры кипения и плотность, близкая к плотности железа. Сочетание этих
факторов позволяет вводить лантаноиды в различные тугоплавкие металлы
значительно проще по сравнению с такими известными модификаторами, как кальций
и магний.
Таким образом, РЗМ в настоящее время широко используют для получения
высокопрочных чугунов, улучшения свойств низколегированных, коррозионностойких
и других сортов сталей, увеличения жаропрочности магниевых и алюминиевых
сплавов, а также для повышения свойств целого ряда других металлов и сплавов.
По объему потребления РЗМ металлургия занимает ведущее место.
Технология силикатов и керамики
Широкое применение РЗМ в стекольной и керамической отраслях
промышленности основано на целом комплексе физико-химических свойств этих элементов
и их соединений, прежде всего большой термической прочности, твердости и
высокой температуре плавления оксидов РЗМ, окислительных свойствах некоторых из
них, например, диоксида церия, высокой абсорбционной способности в разных
частях спектра.
В настоящее время в стекольной промышленности Р3М используют для окраски
и обесцвечивания стекол. Стеклам специального назначения РЗМ придает
способность к пропусканию инфракрасных лучей, поглощению ультрафиолетовых,
стойкость против различного рода излучений.
Оксиды лантана используют в оптических стеклах, о6ладающих высокими
показателями преломления и низкой дисперсией.
Р3М и в первую очередь иттрий применяют для изготовления огнеупоров и
других изделий на основе диоксида циркония, а также для получения искусственных
драгоценных камней.
Особое место занимают оксиды РЗМ в полировке стекла.
Производство люминофоров
Люминофоры применяют в различных областях народного хозяйства. Наиболее
широко их используют в люминесцентных лампах - самых экономичных источников света.
Люминесцентные составы на основе Р3М отличает насыщенный цвет излучения,
узкий спектральный максимум и короткое экспоненциальное затухание.
В качестве фотолюминофоров Р3М используют в люминесцентных лампах
высокого давления.
Электронно-вычислительные машины и квантовые генераторы
Монокристаллы оксидов Р3М с оксидами некоторых других элементов,
получившие название материалов гранатовой структуры, приобретают все большее
значение в современной технике.
Железно-иттриевые гранаты используют в твердотельных лазерах, среди
которых наряду с рубиновыми лазерами и лазерами на неодимовом стекле главную
роль играют лазеры на алюмо-иттриевом гранате. На алюмо-иттриевом гранате,
легированном неодимом, в частности создан один из первых лазеров, работающих
при комнатной температуре.
Осветительная техника
В начале 20-х годов фториды РЗЭ стали вводить в состав фитилей угольных
электродов дуговых ламп и прожекторов. Добавки РЗМ значительно повышают
интенсивность света и улучшают световой спектр. В настоящее время для этой цели
расходуют значительное количество РЗМ.
Также РЗМ применяются в медицине, для создания постоянных магнитов и
магнитострикторов и других областях науки и техники.[2]
1.4 Экстракция
редкоземельных элементов
Экстракционные методы широко применяют как для получения редкоземельных
элементов (РЗЭ), так и для выделения индивидуальных элементов. В качестве
экстрагентов обычно используют фосфорорганические соединения или карбоновые
кислоты. Среди фосфорорганических экстрагентов в промышленности РЗЭ наибольшее
применение нашли три - н - бутилфосфат (ТБФ). ТБФ широко используют для
экстракции. Редкоземельные элементы, обладающие переменной валентностью,
например Ce4+, могут быть отделены от остальной массы РЗЭ с очень
большими факторами разделения.
Экстракция нитратов редкоземельных металлов(III) (РЗМ(III)) ТБФ или
другими нейтральными фосфорорганическими соединениями (НФОС) широко
используется в технологии разделения и тонкой очистки РЗМ. Нитраты РЗМ(III)
экстрагируются ТБФ по сольватному механизму, образуя в органической фазе
недиссоциированные трисольваты состава [Me(NO3)3(ТБФ)3].
В органической фазе возможно также образование и тетрасольватов состава [Me(NO3)3(ТБФ)4].
Процесс экстракции
нитратов РЗМ (III) ТБФ может быть представлен уравнением гетерогенной реакции :
Me3+(в) + 3NO3-(в) + 3 ТБФ(о)
= [Me(NO3)3(ТБФ)3](о). (4)
В случае экстракционного разделения РЗМ(III) из растворов с достаточно
низкой их концентрацией и без высаливателя факторы разделения близлежащих
элементов невысоки. Введение в водную фазу высаливателей позволяет значительно
увеличить коэффициенты распределения и, в большинстве случаев, факторы
разделения РЗМ(III) .
Экстракционное разделение РЗЭ трибутилфосфатом осложнено зависимостью
коэффициента распределения редкоземельных элементов от его порядкового номера,
от концентрации, от состава и кислотности водной фазы и т. д.
Экстракцию ТБФ используют для коллективного выделения всех РЗЭ из
различных промышленных растворов, для разделения РЗЭ на подгруппы и для
получения индивидуальных РЗЭ. Полное извлечение РЗЭ из растворов сложного
солевого состава также может быть осуществлено с использованием ТБФ.
При экстракции ТБФ, рекомендуется сначала выделить из суммы РЗЭ элементы
с переменной валентностью.
1.5 Экстракционное
разделение РЗЭ трибутилфосфатом
Трибутилфосфат (три - н - бутиловый эфир ортофосфорной кислоты, (C4H9O)3P=O)
в настоящее время имеет очень широкое применение для экстракционного разделения
элементов. Исключительная склонность ТБФ к сольватации - результат его высокой
донорной способности, связанной с наличием фосфорильной группы Р = О, в состав
которой входит основной атом кислорода, отличающийся хорошей стерической
доступностью. Сольватация солей ТБФ осуществляется путем присоединения молекул
ТБФ к катионам соли.
Наиболее широкое применение он получил для экстракционного отделения
урана. Такое широкое применение трибутилфосфата обусловлено рядом ценных
качеств, среди которых, в первую очередь, следует назвать весьма высокие
коэффициенты распределения, позволяющие в подавляющем большинстве случаев
достигнуть практически полного извлечения за одну экстракцию. Так, например,
при экстрагировании урана из 2 М раствора азотной кислоты, содержащего 5 мг
урана в 1 мл, коэффициент распределения составляет 33, а в присутствии нитрата
натрия (66 г в 100 мл) он повышается до 1800. Вторым ценным качеством
трибутилфосфата является то, что он не летуч в очень широком интервале
температур (температура кипения 289 єС), и вследствие этого работа с ним
совершенно безопасна. Кроме того, трибутилфосфат обладает чрезвычайно малой
растворимостью в воде, а также мало чувствителен к радиоактивным излучениям.
Данные по растворимости ТБФ в воде представлены в табл. 1.
Таблица 1 - Растворимость ТБФ в воде
|
Температура, єС
|
16
|
7
|
19
|
22
|
|
Растворимость, г/л
|
0,42
|
0,41
|
0,397
|
0,38
|
В химическом отношении трибутилфосфат также очень стабилен. Его гидролиз
водой практически исключается. Он также устойчив по отношению к
концентрированной азотной кислоте и только при ее концентрации 16 М и более
имеет место заметное разложение трибутилфосфата с образованием ди - и
монобутилфосфорной кислот. Трибутилфосфат устойчив к действию многих
окислителей, в том числе таких сильных, как церий(IV) и других.
Кроме урана, трибутилфосфатом из нитратных растворов могут
экстрагироваться также Ce(IV), Zr, Hf, Th, Pu(IV), Ru(VI),Y, La и
редкоземельные элементы, а также Np(IV) и Np(VI), Am(VI), Au(III), Fe(III),
Sc(III), Pa(IV) и Te(III).
Так как вязкость трибутилфосфата очень велика (3,41 сантипуаза при 25
°С), вследствие чего разделение фаз значительно затрудняется, применяют, как
правило, не сам трибутилфосфат, а его растворы в различных инертных
растворителях (керосин, тетрадекан, октан, ксилол, синтин, толуол, хлороформ,
четыреххлористый углерод, дихлорэтан и др.). При этом с понижением вязкости
снижается и коэффициент распределения, но одновременно увеличивается
селективность.
Для повышения селективности экстракционного отделения урана, кроме выбора
соответствующих условий (концентрация трибутилфосфата в инертном растворителе,
концентрация высаливателя и азотной кислоты), большое значение имеет применение
различных маскирующих комплексообразующих. Вследствие большой экстракционной
способности трибутилфосфата полное извлечение урана в органическую фазу, как
уже указывалось, достигается за одну экстракцию; но с другой стороны, это
свойство трибутилфосфата оказывает значительное препятствие выделению урана из
органической фазы. Трехкратное реэкстрагирование равным объемом воды не всегда
обеспечивает полное выделение урана. Для полного извлечения урана из
экстрактов, содержащих большие количества урана и азотной кислоты (вследствие
эффекта самовысаливания), требуется до 9 последовательных реэкстракции равным
объемом 25 % раствора ацетата аммония.
Для реэкстрагирования урана из органической фазы, кроме ацетата аммония,
рекомендуются также растворы сульфатов натрия или аммония.
1.6 Метод
моделирования процесса экстракции
В основе разработанной нами модели лежат результаты физико-химических
исследований, проведенных в СПбГТИ (ТУ), а также результаты моделирования
экстракционного равновесия в системе на основе кислого экстрагента
хлорированного дикарболлида кобальта (ХДК).
В водной фазе экстракционной системы имеются ионы экстрагируемого
металла, протоны и нитрат - ионы. Имеют место следующие реакции :
(5)
(6)
где К - константа образования соответствующего комплекса.
В присутствии ТБФ могут протекать следующие реакции :
Система уравнений (5) - (8), записывается в виде матрицы A. В столбцах
матрицы представлены наименования базовых химических форм и стехиометрические
коэффициенты, с которыми они входят в образующиеся химические формы,
представленные в строках этой же матрицы. В столбцах приведены значения
логарифма термодинамической константы реакции и параметра А уравнений,
учитывающих зависимость концентрационных констант от физико-химических свойств
водной и органической фазы. Приводится параметр Р, отражающий присутствие
данной образующейся химической формы в водной фазе (P=1) или в органической
фазе (P = 0), для соответствующих химических форм.
Если ионная сила водной фазы меньше 0,5, то расчет концентрационной
константы проводится по уравнению Дебая-Хюккеля.
 . (9)
. (9)
Если ионная сила водной фазы больше 0,5, то расчет концентрационной
константы проводится по уравнению Васильева
 , (10)
, (10)
где m - ионная сила
водной фазы экстракционной системы ; и Ko - концентрационная
и термодинамическая константа образования комплекса соответственно;
 - алгебраическая сумма квадратов зарядов продуктов и
исходных компонентов реакции; - параметр неидеальности, отображающий ионные
взаимодействия в водной фазе.
- алгебраическая сумма квадратов зарядов продуктов и
исходных компонентов реакции; - параметр неидеальности, отображающий ионные
взаимодействия в водной фазе.
Закон действующих масс в матричной форме примет вид
, (11)
где  - вектор логарифмов равновесных концентраций ;
- вектор логарифмов равновесных концентраций ;
 - вектор логарифмов концентраций базовых форм.
- вектор логарифмов концентраций базовых форм.
Тогда уравнение материального баланса можно записать в виде
, (12)
где C - вектор аналитических концентраций базовых форм.
Для данного набора констант экстракции существует единственное решение
уравнения (9), как это показано в работе. В каждой точке концентрационной
зависимости коэффициентов распределения решают систему уравнений и рассчитывают
коэффициент распределения металла или кислоты как отношение равновесных
концентраций металла в органической и водной фазах. Для определения
концентрационных констант экстракции методом поиска экстремума функции многих
переменных Флетчера - Пауэлла минимизируют целевую функцию (10), при этом для
всех точек, где коэффициент распределения больше 200, уменьшаем массу
 , (13)
, (13)
где  ,
,  -коэффициент распределения металла или кислоты
экспериментальный и вычисленный соответственно ; - число экспериментальных
точек концентрационной зависимости коэффициентов распределения.
-коэффициент распределения металла или кислоты
экспериментальный и вычисленный соответственно ; - число экспериментальных
точек концентрационной зависимости коэффициентов распределения.
Описанный алгоритм и ФОРТРАН-программа MULCONJ реализованы для
операционной системы WINDOWS.
2. Цели и задачи
Целью дипломной работы является создание базы данных по коэффициентам
распределения и факторов разделения пар редкоземельных элементов.
Для реализации данной цели были поставлены следующие задачи :
Проведение экстракции суммы РЗЭ и азотной кислоты в системе H2O - HNO3 - NH4NO3 - Ln(NO3)3 - ТБФ 100% ;
Расчет констант экстракции индивидуальных РЗЭ при их совместной
экстракции в разных интервалах концентраций реагентов.
экстракция редкоземельный селитра трибутилфосфат
3. Экспериментальная часть
Экспериментальная часть выполнялась в лаборатории кафедры технологии
редких элементов и наноматериалов на их основе СПбГТИ (ТУ).
В ходе работы было приготовлено 4 серии образцов, в каждой из которых
получены 12 растворов с различными концентрациями Ln(NO3)3,
NH4NO3 и HNO3.
3.1 Приготовление и анализ растворов
В работе использовались следующие реактивы : кислый и нейтральный
растворы карбонатов РЗЭ, ацетатно-аммиачный буфер с рН=5,6, ТБФ, аммиачная
селитра, соляная кислота, гидроксид натрия, трилон Б, уксусная кислота, хлорид
калия, ксиленовый оранжевый.
В ходе работы была проведена промывка трибутилфосфата 10 % раствором соды
3 раза по 30 минут, промывка дистиллированной водой в течение двух минут и 0,1
М азотной кислотой в течение 30 минут.
Для приготовления ацетатно-аммиачного буфера понадобится 6 мл
концентрированной уксусной кислоты и 11 мл нитрата аммония. Смешиваем растворы,
помещаем их в мерную колбу объемом 1л и доводим раствор до метки
дистиллированной водой.
Раствор аммиачной селитры был приготовлен путем постепенного добавления
соли в горячую дистиллированную воду, масса навески соли определялась в
зависимости от необходимой концентрации аммиачной селитры.
Чтобы приготовить раствор NaOH
необходимо взять навеску массой 40 г и поместить ее в мерную колбу объемом 1
литр. Гидроксид натрия разбавили дистиллированной водой до метки.
Ксиленоловый оранжевый был растерт в ступке с KCl в соотношении 1:100.
Для приготовления 0,05 М раствора трилона Б использовался стандарт-титр.
Для приготовления слабокислого раствора Ln(NO3)3
необходимо взять 50 мл крепкой азотной кислоты, поместить ее в термостойкий
стакан и нагревать, постепенно добавляя в раствор карбонаты РЗЭ. Добавление
происходит до тех пор, пока не прекратится его растворение в кислоте, то есть
выделение углекислого газа. Таким образом, было добавлено 96 г карбонатов РЗЭ.
Цвет раствора - зеленый. Объем раствора = 84 мл, его pH=2,093. Отфильтровываем
раствор с помощью фильтра «синяя лента».
3.1.1 Определение
плотности ТБФ
В данной работе плотность растворов определялась пикнометрическим
методом. Этот метод заключается в определении массы испытуемого материала,
помещенного в пикнометр с известным объемом при определенной температуре.
Для определения плотности раствора понадобится 3 пикнометра объемом 5 мл,
предварительно высушенных в сушильном шкафу. Вымытые и просушенные пикнометры
взвешиваем на аналитических весах, затем заполняем их дистиллированной водой до
метки, закрываем пробкой и снова взвешиваем каждый из пикнометров 3 раза при
температуре 20°С. По данным о массе воды определяем объём пикнометров по
формуле :
V=m/p, (14)
где V - объём пикнометра, см3 ;
m -
масса воды, г ;
р - плотность воды, г/ см3.
Освобождаем пикнометры от воды, сушим и заполняем их раствором ТБФ при 20
°С. Взвешиваем каждый из пикнометров три раза. Полученные данные сведены в
таблицу 2.
Таблица 2 - Плотность ТБФ
|
Номер пикнометра
|
Номер взвешивания
|
Масса сухого пикнометра, г
|
Масса пикнометра с водой, г
|
Объем пикнометра, мл
|
Масса пикнометра с ТБФ, сред., г
|
Масса среды (ТБФ), сред., г
|
Плотность, г / см3
|
|
1
|
1
|
8,0164
|
13,47210
|
5,4652
|
13,3798
|
5,3634
|
0,9501
|
|
2
|
8,0164
|
13,47180
|
|
|
|
|
|
3
|
8,0164
|
13,47160
|
|
|
|
|
|
2
|
1
|
8,2612
|
14,40440
|
6,1538
|
14,3004
|
6,0389
|
0,9813
|
|
2
|
8,2616
|
14,40440
|
|
|
|
|
|
3
|
8,2618
|
14,40440
|
|
|
|
|
|
3
|
1
|
8,2872
|
13,8369
|
5,5596
|
13,7393
|
5,4520
|
0,9806
|
|
2
|
8,2873
|
13,8369
|
|
|
|
|
|
3
|
8,2873
|
13,8368
|
|
|
|
|
Плотность раствора ТБФ равна 0,9707 г / см3.
3.1.2 Определение
плотности аммиачной селитры
Аналогичным образом определяем плотность раствора нитрата аммония.
Концентрация аммиачной селитры будет варьироваться в зависимости от серии
растворов. Данные по измерению плотности для первой серии растворов приведены в
таблицу 3.
Таблице 3-Плотность аммиачной селитры
|
Номер пикнометра
|
Масса сухого пикнометра, г
|
Масса пикнометра с аммиачной селитрой, сред., г
|
Масса среды, г
|
Плотность, г / см3
|
|
1
|
8,0164 8,0164 8,0164
|
14,8347
|
6,8183
|
1,2476
|
|
5
|
8,2612 8,2616 8,2618
|
15,9395
|
7,6780
|
1,2477
|
|
6
|
8,2872 8,2873 8,2873
|
15,2268
|
6,9395
|
1,2482
|
Таким образом, плотность аммиачной селитры равна 1,2478 г/см3,
что при 20 °С соответствует 8,55 моль/л. [3]
3.1.3 Определение
плотности и концентрации раствора суммы РЗЭ
Определяем плотность раствора уже известным пикнометрическим методом.
Данные по определению плотности приведены в таблице 4.
Таблица 4- Плотность раствора Ln(NO3)3
|
Номер пикнометра
|
Масса сухого пикнометра, г
|
Масса пикнометра с Ln(NO3)3, сред., г
|
Масса среды Ln(NO3)3, г
|
Плотность, г / см3
|
|
1
|
8,0164 8,0164 8,0164
|
17,3464
|
9,32997
|
1,7072
|
|
5
|
8,2612 8,2616 8,2618
|
19,0917
|
10,72297
|
1,7014
|
|
6
|
8,2872 8,2873 8,2873
|
19,5342
|
11,18000
|
1,7025
|
Плотность раствора определяем по формуле 14. Таким образом, плотность
раствора равна 1,7037 г/см3.
В ходе работы определение концентраций суммы РЗЭ проводили с помощью
комплексонометрического метода. Комплексонометрический метод основан на реакции
комплексообразования катионов металлов с комплексонами. При этом образуются
очень прочные, хорошо растворимые в воде внутрикомплексные соединения -
комплексонаты. Метод отличается быстротой и высокой точностью.
Для определения концентрации раствора Ln(NO3)3 в
колбу помещали 30 мл ацетатного буфера с pH=5,6, добавляли пару кристалликов
ксиленолового оранжевого, раствор приобретал желтый цвет, далее добавляли
аликовоту раствора, при этом цвет изменялся на фиолетовый. Нагревали раствор на
горелке до 60 0C и титровали 0,05 M трилоном Б до появления желтой
окраски и рассчитывали концентрацию РЗМ по формуле :
 , (15)
, (15)
где VT - объём титранта, израсходованный на
титрование, мл ;
Стрил - концентрация титранта, моль/л ;
Vпр
- объём пробы, мл.
Концентрация раствора = 2, 9375 моль/л.
3.2 Проведение
экстракции и реэкстракции
После приготовления растворов идет подготовка серий к экстракции. Для
этого понадобилось 12 чистых стеклянных конических пробирок объемом 10 мл.
В каждую из них поместили определенный объем раствора РЗЭ и аммиачной
селитры. Суммарный объем каждого полученного образца равен 10 мл. Проводился
анализ каждой из проб, а именно, определялась плотность и концентрация РЗЭ
каждого раствора.
Далее переносим раствор в коническую колбу для титрования на 50 мл.
Процесс экстракции проводили в системе раствор РЗЭ - ТБФ при соотношении
объёмов водной и органической фаз (1:1). Межфазное равновесие устанавливалось
при интенсивном встряхивании конических колб объёмом 50 мл в шейкере ТИП - «memmert», содержащих водную и органическую
фазы в течение 3 часов при постоянной температуре 25 єС. Разделяли водную и
органическую фазы пипеткой Пастера, органическую фазу реэкстрагировали 0,1 М
раствором HNO3 с соотношением фаз 1:1 в течение 3 часов при
температуре 60 єС и разделяли фазы. Водные фазы после экстракции и реэкстракции
титровали комплексонометрическим методом и методом потенциометрического
титрования.
Методом потенциометрического титрования определялась концентрация кислоты
в пробе. Для измерения pH
использовали pH - метр Thermo Orion 720A Plus со стеклянным комбинированным
электродом ЭСЛК-01.7. Перед началом титрования проводилась калибровка прибора
по трем буферным растворам с pH =
4,01, pH = 1,68 и 1 М HNO3 c pH=1,1.
Далее в стакан помещали 40 мл дистиллированной воды и аликвоту
исследуемого раствора. Титрование вели путем постепенного добавления в раствор NaOH и фиксирования значений pH, пока не произойдет его скачок до 7.
Определяли точку эквивалентности и рассчитывали концентрацию кислоты с помощью
концентрации гидроксида натрия. Концентрация гидроксида натрия определялась
также потенциометрически с использованием 0,1 М кислоты HCl, полученной разбавлением фиксанала.
Проводили ICP - OES анализ образцов экстракта и
реэкстракта для получения данных о коэффициентах распределения РЗЭ.
3.3 Результаты
и их обсуждение
3.3.1 Серия
1 с концентрацией суммы РЗЭ в водной фазе 0,0195 - 1,93 М и концентрацией
аммиачной селитры 8,08 - 0 М
Экстракция РЗЭ была проведена для следующих элементов - La, Ce, Pr, Nd, Sm, Eu, Gd, Y. В таблице 5 представлены данные об анализе образцов 1 серии
до экстракции, после экстракции и реэкстракции.
Таблица 5- Результаты анализа проб 1 серии
|
Плотность раствора каждой пробы, г/см3
|
С ∑РЗЭ в исходном растворе, М
|
С HNO3
в исходном растворе, М
|
C NH4NO3
в исходном растворе, М
|
С ∑РЗЭ после экстракции, М
|
С HNO3
после экстракции, М
|
С ∑РЗЭ после реэкстракции, М
|
С HNO3
после реэкстракции, М
|
|
1,2704
|
0,167
|
1E-2
|
8,06
|
0,0195
|
н/о
|
0,104
|
н/о
|
|
1,2803
|
0,400
|
1E-2
|
7,60
|
0,0250
|
н/о
|
0,175
|
н/о
|
|
1,3149
|
0,483
|
1E-2
|
7,13
|
0,0830
|
н/о
|
0,275
|
н/о
|
|
1,3256
|
0,611
|
1E-2
|
6,65
|
0,113
|
н/о
|
0,292
|
н/о
|
|
1,3727
|
0,800
|
6,18
|
0,225
|
н/о
|
0,375
|
н/о
|
|
1,3752
|
1,06
|
1E-2
|
5,70
|
0,225
|
н/о
|
0,400
|
н/о
|
|
1,4436
|
1,26
|
1E-2
|
4,75
|
0,550
|
н/о
|
0,458
|
н/о
|
|
1,4875
|
1,56
|
1E-2
|
3,80
|
0,767
|
н/о
|
0,525
|
н/о
|
|
1,5459
|
1,97
|
1E-2
|
2,85
|
1,10
|
н/о
|
0,567
|
н/о
|
|
1,5992
|
2,12
|
1E-2
|
1,90
|
1,36
|
н/о
|
0,508
|
н/о
|
|
1,6763
|
2,73
|
1E-2
|
0,475
|
1,88
|
н/о
|
0,583
|
н/о
|
|
1,7078
|
2,94
|
1E-2
|
0
|
1,93
|
н/о
|
0,550
|
н/о
|
Приводим график зависимости концентрации РЗЭ в каждом образце от его
плотности (Рисунок 1).
Рисунок 1- Зависимость концентрации РЗЭ в каждом образце от его плотности
Полученные на ICP - OES экспериментальные данные представили
в виде зависимости коэффициента распределения суммы РЗЭ в органической фазе от
концентрации суммы РЗЭ в водной фазе.
Различия между коэффициентом распределения определённым методом
комплексонометрии и методом ISP-OES составляют 20,6 %. Большие ошибки
при малых концентрациях обусловлены высокой ошибкой комплексонометрического
метода.
- определено методом комплексонометрии ; 2- методом ISP-OES
Рисунок 2- Зависимость коэффициента распределения суммы РЗЭ в
органической фазе от концентрации суммы РЗЭ в водной фазе
Экспериментальные данные также представлены в виде зависимости
коэффициента распределения индивидуальных РЗЭ в органической фазе от
концентрации индивидуальных РЗЭ в водной фазе (рисунок 3).
Рисунок 3 - Зависимость коэффициента распределения индивидуальных РЗЭ в
органической фазе от концентрации индивидуальных РЗЭ в водной фазе
Различия между коэффициентом распределения определённым методом
комплексонометрии и методом ISP-OES составляют 35,7 %.
По экспериментальным данным, приведенным в таблице Ж.1 и таблице Ж.2 в
приложении Ж, при помощи программы mulcon вычислены значения констант и параметров неидеальности в экстракционной
системе H2O - HNO3 - NH4NO3 - Ln(NO3)3 - ТБФ 100% для первой
серии, которые приведены в табл. 6.
Таблица 6 - Набор термодинамических констант и параметров неиделаьности
|
Образующаяся форма
|
Термодинамические константы, Lg K
|
Параметр А
|
|
(La)(NO3)3(TBP)3
|
-1,98E+00
|
0,5028
|
|
(La)(NO3)3(TBP)4
|
2,66E+00
|
-1,12E-01
|
|
(Ce)(NO3)3(TBP)3
|
-1,13E+00
|
0,4018
|
|
(Ce)(NO3)3(TBP)4
|
3,08E-01
|
2,42E-01
|
|
(Pr)(NO3)3(TBP)3
|
-8,15E-01
|
0,4387
|
|
(Nd)(NO3)3(TBP)3
|
2,75E-01
|
0,264
|
|
(Sm)(NO3)3(TBP)3
|
1,02E+01
|
-2,61E-01
|
|
(Eu)(NO3)3(TBP)3
|
1,57E+00
|
1,44E-01
|
|
(Gd)(NO3)3(TBP)3
|
-3,84E+00
|
0,8085
|
|
(Gd)(NO3)3(TBP)4
|
2,26E+01
|
-2,74E+00
|
|
(Y)(NO3)3(TBP)4
|
6,19E-01
|
2,49E-01
|
Экстракция лантана
Рисунок 4 - Зависимость доли форм экстрагируемых комплексов La3+ от суммарной концентрации La3+ в водной фазе
Из рисунка 4 видно, что доля экстрагируемых форм типа (La)(NO3)3(TBP)3
выше, чем (La)(NO3)3(TBP)4. НаРисунок 5
рисунке 5 показаны коэффициенты распределения лантана в зависимости от концентрации
нитрата аммония и от равновесной концентрации лантана в водной фазе. Видно, что
модель адекватно описывает экспериментальные данные.
Рисунок 5- Зависимость коэффициента распределения лантана (D La3+) от содержания нитрата аммония в водной фазе
Рисунок 6 - Зависимость коэффициента распределения лантана (D La3+) от содержания лантана в экстракте
Среднее отклонение расчёта от экспериментальных данных составляет 6,13 %.
Экстракция церия
Рисунок 7- Зависимость доли форм экстрагируемых комплексов Се от
суммарной концентрации Се3+ в водной фазе
Из рисунка 7 видно, что доля в ходе экстракции образуется как
экстрагируемая форма типа (La)(NO3)3(TBP)3 ,
так и (La)(NO3)3(TBP)4. Причем в точке, в
которой концентрация Се3+ равна 0,4 моль/л, доли форм образуемых
комплексов совпадают. На рисунке 8 и рисунке 9 показаны коэффициенты
распределения церия в зависимости от концентрации нитрата аммония и от
равновесной концентрации церия в водной фазе. Видно, что модель адекватно
описывает экспериментальные данные.
Среднее отклонение расчёта от экспериментальных данных составляет 5,58 %.
Рисунок 8- Зависимость коэффициента распределения церия (D Се3+) от
содержания нитрата аммония в водной фазе
Рисунок 9 - Зависимость коэффициента распределения церия (D Се3+) от
содержания церия в экстракте
Экстракция празеодима
Из рисунка 10 видно, что в случае с празеодимом в ходе экстракции
образуется лишь одна экстрагируемая форма - (Pr)(NO3)3(TBP)3.
Среднее отклонение расчёта от экспериментальных данных составляет 10,8 %. На
Рисунок 11 показаны коэффициенты распределения празеодима в зависимости от
равновесной концентрации лантана в водной фазе. Видно, что модель адекватно
описывает экспериментальные данные.
Рисунок 10 - Зависимость доли форм экстрагируемых комплексов Pr3+ от суммарной концентрации Pr3+ в водной фазе
Рисунок 11- Зависимость коэффициента распределения празеодима (D Pr3+) от содержания
празеодима в экстракте
Экстракция неодима
Из рисунка 12 видно, что образуется лишь одна экстрагируемая форма - (Nd)(NO3)3(TBP)3.
На рисунке 13 и рисунке 14 показаны коэффициенты распределения неодима в
зависимости от концентрации нитрата аммония и от равновесной концентрации
неодима в водной фазе. Видно, что модель адекватно описывает экспериментальные
данные.
Рисунок 12- Зависимость доли форм экстрагируемых комплексов Nd3+ от суммарной концентрации Nd3+ в водной фазе
Рисунок 13- Зависимость коэффициента распределения неодима (D Nd3+) от содержания нитрата аммония в водной фазе
Рисунок 14 - Зависимость коэффициента распределения неодима (D Nd3+) от содержания неодима в экстракте
Среднее отклонение расчёта от экспериментальных данных составляет 8,91 %.
Экстракция самария
Из рисунка 15 видно, что образуется лишь одна экстрагируемая форма - (Sm)(NO3)3(TBP)3.
Рисунок 15 - Зависимость доли форм экстрагируемых комплексов Sm3+ от суммарной концентрации Sm 3+ в водной фазе
На рисунке 16 и рисунке 17 показаны коэффициенты распределения самария в
зависимости от концентрации нитрата аммония и от равновесной концентрации
самария в водной фазе.
Рисунок 16- Зависимость коэффициента распределения самария (D Sm3+) от содержания нитрата аммония в водной фазе
Рисунок 17- Зависимость коэффициента распределения самария (D Sm3+) от содержания самария в экстракте
Среднее отклонение расчёта от экспериментальных данных составляет 11,7 %.
Экстракция европия
Рисунок 18- Зависимость доли форм экстрагируемых комплексов Eu3+ от суммарной концентрации Eu 3+ в водной фазе
Рисунок 19- Зависимость коэффициента распределения европия (D Eu3+) от содержания нитрата аммония в водной фазе
Из рисунка 18 видно, что для европия образуется лишь одна экстрагируемая
форма - (Eu)(NO3)3(TBP)3.
На рисунке 19 и рисунке 20 показаны коэффициенты распределения европия в
зависимости от концентрации нитрата аммония и от равновесной концентрации
европия в водной фазе. Видно, что модель адекватно описывает экспериментальные
данные.
Рисунок 20- Зависимость коэффициента распределения европия (D Eu3+) от содержания европия в экстракте
Среднее отклонение расчёта от экспериментальных данных составляет 17,2 %.
Экстракция гадолиния
Из рисунка 21 видно, что гадолиний образует две экстрагируемых формы : (Gd)(NO3)3(TBP)3
и (Gd)(NO3)3(TBP)3.
На рисунке 22 и рисунке 23 показаны коэффициенты распределения гадолиния
в зависимости от концентрации нитрата аммония и от равновесной концентрации
гадолиния в водной фазе. Видно, что модель адекватно описывает
экспериментальные данные.
Рисунок 21- Зависимость доли форм экстрагируемых комплексов Gd3+ от суммарной концентрации Gd 3+ в водной фазе
Рисунок 22 - Зависимость коэффициента распределения гадолиния (D Gd3+) от содержания нитрата аммония в водной фазе
Среднее отклонение расчёта от экспериментальных данных составляет 10,6 %.
Рисунок 23- Зависимость коэффициента распределения гадолиния (D Gd3+) от содержания гадолиния в экстракте
Экстракция иттрия
Из рисунка 24 видно, что иттрий образует одну экстрагируемую форму: (Y)(NO3)3(TBP)3.
На рисунке 25 и рисунке 26 показаны коэффициенты распределения иттрия в
зависимости от концентрации нитрата аммония и от равновесной концентрации
иттрия в водной фазе.
Рисунок 24- Зависимость доли форм экстрагируемых комплексов Y3+ от суммарной концентрации Y 3+ в водной фазе
Рисунок 25- Зависимость коэффициента распределения иттрия (D Y3+) от содержания нитрата аммония в водной фазе
Рисунок 26- Зависимость коэффициента распределения иттрия (D Y3+) от содержания иттрия в экстракте
Среднее отклонение расчёта от экспериментальных данных составляет 14,4 %.
3.3.2
Серия 2 с концентрацией суммы РЗЭ в водной фазе 0,030 - 2,52 М и концентрацией
аммиачной селитры 5,75 - 0 М
Экстракция РЗЭ была проведена для элементов - La, Ce, Pr, Nd, Sm, Eu, Gd,
Y. В таблице 7 представлены данные об анализе образцов 2 серии до экстракции,
после экстракции и реэкстракции.
Таблица 7- Результаты анализа проб 2 серии
|
Плотность раствора каждой пробы, г/см3
|
С ∑РЗЭ в исходном растворе, М
|
С HNO3
в исходном растворе, М
|
C NH4NO3
в исходном растворе, М
|
С ∑РЗЭ после экстракции, М
|
С HNO3
после экстракции, М
|
С ∑РЗЭ после реэкстракции, М
|
С HNO3
после реэкстракции, М
|
|
1,21094
|
0,144
|
1E-2
|
5,75
|
0,0300
|
н/о
|
0,120
|
н/о
|
|
1,24653
|
0,375
|
1E-2
|
5,41
|
0,0500
|
н/о
|
0,225
|
н/о
|
|
1,28895
|
0,650
|
1E-2
|
5,08
|
0,123
|
н/о
|
0,303
|
н/о
|
|
1,32313
|
0,821
|
1E-2
|
4,74
|
0,250
|
н/о
|
0,375
|
н/о
|
|
1,34335
|
0,875
|
1E-2
|
4,398
|
0,333
|
н/о
|
0,404
|
н/о
|
|
1,39170
|
1,07
|
1E-2
|
4,06
|
0,450
|
н/о
|
0,408
|
н/о
|
|
1,46616
|
1,78
|
1E-2
|
3,38
|
0,783
|
н/о
|
0,500
|
н/о
|
|
1,53741
|
2,00
|
1E-2
|
2,71
|
1,03
|
н/о
|
0,525
|
н/о
|
|
1,61124
|
2,22
|
1E-2
|
2,03
|
1,33
|
н/о
|
0,575
|
н/о
|
|
1,68131
|
3,17
|
1E-2
|
1,35
|
1,67
|
н/о
|
0,592
|
н/о
|
|
1,78845
|
3,33
|
1E-2
|
0,338
|
2,37
|
н/о
|
0,600
|
н/о
|
|
1,82341
|
3,27
|
1E-2
|
0
|
2,52
|
н/о
|
0,717
|
н/о
|
Приводим зависимость концентрации РЗЭ в каждом образце от его плотности
(рисунок 27).
Полученные на ICP - OES экспериментальные данные представили
в виде зависимости коэффициента распределения суммы РЗЭ в органической фазе от
концентрации суммы РЗЭ в водной фазе (рисунок 28).
Экспериментальные данные также представлены в виде зависимости
коэффициента распределения индивидуальных РЗЭ в органической фазе от
концентрации оксидов индивидуальных РЗЭ в исходной водной фазе (рисунок 29).
Рисунок 27- Зависимость концентрации РЗЭ в каждом образце от его
плотности
- определено методом комплексонометрии ; 2- методом ISP-OES
Рисунок 28 - Зависимость коэффициента распределения суммы РЗЭ в
органической фазе от концентрации суммы РЗЭ в водной фазе
Рисунок 29- Зависимость коэффициента распределения индивидуальных РЗЭ в
органической фазе от концентрации оксидов РЗЭ в исходной водной фазе
Ниже представлены аналогичные зависимости для гадолиния (Рисунок 30) и
европия (Рисунок 31).
Рисунок 30- Зависимость коэффициента распределения гадолиния в
органической фазе от концентрации оксидов РЗЭ в исходной водной фазе
Рисунок 31- Зависимость коэффициента распределения европия в органической
фазе от концентрации оксидов РЗЭ в исходной водной фазе
Различия между коэффициентом распределения определённым методом
комплексонометрии и методом ISP-OES
составляют 62,8 %.
По экспериментальным данным, приведенным в таблице Ж.3 и в таблице Ж.4 в
приложении Ж, при помощи программы mulcon вычислены значения констант и параметров неидеальности в экстракционной
системе H2O - HNO3 - NH4NO3 - Ln(NO3)3 - ТБФ 100% для второй
серии, которые приведены в таблице 8.
Таблица 8- Набор термодинамических констант и параметров неидеальности
|
Образующаяся форма
|
Термодинамические константы, Lg K
|
Параметр А
|
|
(La)(NO3)3(TBP)3
|
1,62E+00
|
6,45E-02
|
|
(Ce)(NO3)3(TBP)3
|
1,56E+00
|
8,21E-02
|
|
(Pr)(NO3)3(TBP)3
|
1,48E+00
|
0,1124
|
|
(Nd)(NO3)3(TBP)3
|
-6,74E-01
|
3,96E-01
|
|
(Nd)(NO3)3(TBP)4
|
1,61E+00
|
1,79E-01
|
|
(Sm)(NO3)3(TBP)3
|
1,14E+01
|
-5,56E-01
|
|
(Sm)(NO3)3(TBP)4
|
8,44E+00
|
-6,86E-03
|
|
(Eu)(NO3)3(TBP)3
|
1,57E+00
|
1,44E-01
|
|
(Gd)(NO3)3(TBP)3
|
1,46E+00
|
0,2037
|
Экстракция лантана
Рисунок 32 - Зависимость доли форм экстрагируемых комплексов La3+ от суммарной концентрации La3+ в водной фазе
Рисунок 33- Зависимость коэффициента распределения лантана (D La3+) от содержания нитрата аммония в водной фазе
Из рисунка 32 видно, что образуется только один экстрагируемый комплекс
лантана (La)(NO3)3(TBP)3, доля этого комплекса
уменьшается с увеличением La3+ в водной фазе. На рисунке 33 и
рисунке 34 показаны коэффициенты распределения лантана в зависимости от
концентрации нитрата аммония и от равновесной концентрации лантана в водной
фазе. Видно, что модель адекватно описывает экспериментальные данные.
Рисунок 34- Зависимость коэффициента распределения лантана (D La3+) от содержания лантана в экстракте
Среднее отклонение расчёта от экспериментальных данных составляет 16,9 %.
Экстракция церия
Из рисунка 35 видно, что образуется только один экстрагируемый комплекс
церия (Се)(NO3)3(TBP)3, доля этого комплекса
уменьшается с увеличением Се3+ в водной фазе.
На рисунке 36, рисунке 37 показаны коэффициенты распределения церия в
зависимости от концентрации нитрата аммония и от равновесной концентрации церия
в водной фазе. Видно, что модель адекватно описывает экспериментальные данные.
Рисунок 35- Зависимость доли форм экстрагируемых комплексов Се от
суммарной концентрации Се3+ в водной фазе
Рисунок 36- Зависимость коэффициента распределения церия (D Се3+) от содержания
нитрата аммония в водной фазе
Рисунок 37- Зависимость коэффициента распределения церия (D Се3+) от содержания церия
в экстракте
Среднее отклонение расчёта от экспериментальных данных составляет 13,3 %.
Экстракция празеодима
Рисунок 38 - Зависимость доли форм экстрагируемых комплексов Pr3+ от суммарной концентрации Pr3+ в водной фазе
Из рисунка 38 видно, что образуется только один экстрагируемый комплекс
церия (Pr3+)(NO3)3(TBP)3,
доля этого комплекса уменьшается с увеличением Pr3+ в водной фазе. На рисунке 39 показаны коэффициенты
распределения празеодима в зависимости от равновесной концентрации празеодима в
водной фазе. Видно, что модель адекватно описывает экспериментальные данные.
Среднее отклонение расчёта от экспериментальных данных составляет 10,9 %.
Рисунок 39- Зависимость коэффициента распределения празеодима (D Pr3+) от содержания празеодима в экстракте
Экстракция неодима
Из рисунка 40 видно, что образуются два экстрагируемых комплекса неодима,
однако, доля комплекса (Nd)(NO3)3(TBP)3
выше доли комплекса (Nd)(NO3)3(TBP)4.
На рисунке 41 и рисунке 42 показаны коэффициенты распределения неодима в
зависимости от концентрации нитрата аммония и от равновесной концентрации
неодима в водной фазе. Видно, что модель адекватно описывает экспериментальные
данные.
Рисунок 40 - Зависимость доли форм экстрагируемых комплексов Nd3+ от суммарной концентрации Nd3+ в водной фазе
Рисунок 41- Зависимость коэффициента распределения неодима (D Nd3+) от содержания нитрата аммония в водной фазе
Среднее отклонение расчёта от экспериментальных данных составляет 9,15 %.
Рисунок 42- Зависимость коэффициента распределения неодима (D Nd3+) от содержания неодима в экстракте
Экстракция самария
Из рисунка 43 видно, что образуются два экстрагируемых комплекса самария,
однако, доля комплекса (Sm)(NO3)3(TBP)4
выше доли комплекса (Sm)(NO3)3(TBP)3.
Рисунок 43 - Зависимость доли форм экстрагируемых комплексов Sm3+ от суммарной концентрации Sm 3+ в водной фазе
На рисунке 44 и рисунке 45 показаны коэффициенты распределения самария в
зависимости от концентрации нитрата аммония и от равновесной концентрации
самария в водной фазе.
Рисунок 44- Зависимость коэффициента распределения самария (D Sm3+) от содержания нитрата аммония в водной фазе
Рисунок 45- Зависимость коэффициента распределения самария (D Sm3+) от содержания самария в экстракте
Среднее отклонение расчёта от экспериментальных данных составляет 7,79 %.
Экстракция европия
Из рисунка 46 видно, что для европия образуется лишь одна экстрагируемая
форма - (Eu)(NO3)3(TBP)3.
Рисунок 46 - Зависимость доли форм экстрагируемых комплексов Eu3+ от суммарной концентрации Eu 3+ в водной фазе
Рисунок 47 - Зависимость коэффициента распределения европия (D Eu3+) от содержания нитрата аммония в водной фазе
На рисунке 47 и рисунке 48 показаны коэффициенты распределения европия в
зависимости от концентрации нитрата аммония и от равновесной концентрации
европия в водной фазе. Видно, что модель адекватно описывает экспериментальные
данные.
Рисунок 48- Зависимость коэффициента распределения европия (D Eu3+) от содержания европия в экстракте
Среднее отклонение расчёта от экспериментальных данных составляет 11,7 %.
Экстракция гадолиния
Рисунок 49- Зависимость доли форм экстрагируемых комплексов Gd3+ от суммарной концентрации Gd 3+ в водной фазе
Из рисунка 49 видно, что для гадолиния образуется лишь одна
экстрагируемая форма - (Gd)(NO3)3(TBP)3.
На рисунке 50 и рисунке 51 показаны коэффициенты распределения гадолиния
в зависимости от концентрации нитрата аммония и от равновесной концентрации
гадолиния в водной фазе.
Рисунок 50- Зависимость коэффициента распределения гадолиния (D Gd3+) от содержания нитрата аммония в водной фазе
Рисунок 51- Зависимость коэффициента распределения гадолиния (D Gd3+) от содержания гадолиния в экстракте
Среднее отклонение расчёта от экспериментальных данных составляет 18,0 %.
3.3.3 Серия
3 с концентрацией суммы РЗЭ в водной фазе 0,010 - 1,61 М и концентрацией
аммиачной селитры 5,79 - 0 М
Экстракция РЗЭ была проведена для элементов - La, Ce, Pr, Nd, Sm, Eu, Gd,
Y. В таблице 9 представлены данные об анализе образцов 3 серии до экстракции,
после экстракции и реэкстракции.
|
Плотность раствора каждой пробы, г/см3
|
С ∑РЗЭ в исходном растворе, М
|
С HNO3
в исходном растворе, М
|
C NH4NO3
в исходном растворе, М
|
С ∑РЗЭ после экстракции, М
|
С HNO3
после экстракции, М
|
Плотность раствора экстракта г/см3
|
С ∑РЗЭ после реэкстракции, М
|
С HNO3
после реэкстракции, М
|
|
1,2675
|
0,0800
|
0,472
|
5,79
|
0,0100
|
н/о
|
1,24
|
0,0850
|
н/о
|
|
1,2836
|
0,217
|
0,786
|
5,48
|
0,0250
|
н/о
|
1,23
|
0,128
|
н/о
|
|
1,2526
|
0,247
|
1,10
|
5,18
|
0,0733
|
н/о
|
1,24
|
0,155
|
н/о
|
|
1,3182
|
0,350
|
1,57
|
4,87
|
0,150
|
н/о
|
1,25
|
0,183
|
н/о
|
|
1,3309
|
0,400
|
1,89
|
4,57
|
0,250
|
н/о
|
1,27
|
0,192
|
н/о
|
|
1,3608
|
0,550
|
2,20
|
4,26
|
0,333
|
н/о
|
1,28
|
0,183
|
н/о
|
|
1,4059
|
0,700
|
2,99
|
3,65
|
0,550
|
н/о
|
1,32
|
0,175
|
н/о
|
|
1,4394
|
0,850
|
4,09
|
3,045
|
0,708
|
н/о
|
1,35
|
0,200
|
н/о
|
|
1,4801
|
1,12
|
4,87
|
2,44
|
0,917
|
н/о
|
1,39
|
0,158
|
н/о
|
|
1,5176
|
1,30
|
7,00
|
1,83
|
1,09
|
н/о
|
1,43
|
0,192
|
н/о
|
|
1,5701
|
1,51
|
7,54
|
0,914
|
1,32
|
н/о
|
1,63
|
0,200
|
н/о
|
|
1,6224
|
1,77
|
8,02
|
0
|
1,61
|
н/о
|
1,51
|
0,225
|
н/о
|
Приводим Зависимость концентрации РЗЭ в каждом образце от его плотности
(рисунок 52).
Полученные на ICP - OES экспериментальные данные представили
в виде зависимости коэффициента распределения суммы РЗЭ в органической фазе от
концентрации суммы РЗЭ в водной фазе (Рисунок 53).
Рисунок 52 - Зависимость концентрации РЗЭ в каждом образце от его
плотности
1- определено методом комплексонометрии ; 2- методом ISP-OES
Рисунок 53- Зависимость коэффициента распределения суммы РЗЭ в
органической фазе от концентрации суммы РЗЭ в водной фазе
Экспериментальные данные также представлены в виде зависимости
коэффициента распределения индивидуальных РЗЭ в органической фазе от
концентрации индивидуальных РЗЭ в водной фазе (Рисунок 54).
Рисунок 54- Зависимость коэффициента распределения индивидуальных РЗЭ в
органической фазе от концентрации индивидуальных РЗЭ в водной фазе
Различия между коэффициентом распределения определённым методом
комплексонометрии и методом ISP-OES составляют 16,6 %.
По экспериментальным данным, приведенным в таблице Ж.5 и таблице Ж.6 в
приложении Ж, при помощи программы mulcon вычислены значения констант и параметров неидеальности в экстракционной
системе H2O - HNO3 - NH4NO3 - Ln(NO3)3 - ТБФ 100% для третьей
серии, которые приведены в таблицу 10.
Таблица 10 - Набор термодинамических констант и параметров неидеальности
|
Образующаяся форма
|
Термодинамические константы, Lg K
|
Параметр А
|
|
(La)(NO3)3(TBP)3
|
2,85E+01
|
-4,13E+00
|
|
(La)(NO3)3(TBP)4
|
8,21E-01
|
1,16E-01
|
|
(Ce)(NO3)3(TBP)3
|
1,10E+00
|
1,07E-01
|
|
(Pr)(NO3)3(TBP)3
|
2,03E+00
|
6,19E-02
|
|
(Nd)(NO3)3(TBP)3
|
-1,24E+00
|
3,75E-01
|
|
(Nd)(NO3)3(TBP)4
|
1,27E+00
|
1,91E-01
|
|
(Sm)(NO3)3(TBP)3
|
1,01E+01
|
-1,82E-01
|
|
(Sm)(NO3)3(TBP)4
|
8,05E+00
|
-1,16E-02
|
|
(Eu)(NO3)3(TBP)3
|
1,58E+00
|
1,28E-01
|
|
(Gd)(NO3)3(TBP)3
|
1,72E+00
|
0,1252
|
|
(Y)(NO3)3(TBP)4
|
1,29E+00
|
1,63E-01
|
Экстракция лантана
Из рисунка 55 видно, что доля экстрагируемых форм типа (La)(NO3)3(TBP)4
выше, чем (La)(NO3)3(TBP)3.
Рисунок 55- Зависимость доли форм экстрагируемых комплексов La3+ от суммарной концентрации La3+ в водной фазе
На рисунке 56, рисунке 57 и рисунке 58 показаны коэффициенты
распределения лантана в зависимости от концентрации нитрата аммония, от ионной
силы и от равновесной концентрации лантана в водной фазе. Видно, что модель
адекватно описывает экспериментальные данные.
Среднее отклонение расчёта от экспериментальных данных составляет 13,6 %
Рисунок 56- Зависимость коэффициента распределения лантана (D La3+) от содержания нитрата аммония в водной фазе
Рисунок 57- Зависимость коэффициента распределения лантана (D La3+) от равновесной ионной силы
Рисунок 58- Зависимость коэффициента распределения лантана (D La3+) от содержания лантана в экстракте
Экстракция церия
Из рисунка 59 видно, что для церия образуется лишь одна экстрагируемая
форма - (Се)(NO3)3(TBP)3.
Рисунок 59 - Зависимость доли форм экстрагируемых комплексов Се от
суммарной концентрации Се3+ в водной фазе
На рисунке 59, рисунке 60 и рисунке 61 показаны коэффициенты
распределения церия в зависимости от концентрации нитрата аммония и от
равновесной концентрации церия в водной фазе. Видно, что модель адекватно
описывает экспериментальные данные.
Рисунок 60- Зависимость коэффициента распределения церия (D Се3+) от содержания
нитрата аммония в водной фазе
Рисунок 61- Зависимость коэффициента распределения церия (D Се3+) от содержания церия
в экстракте
Среднее отклонение расчёта от экспериментальных данных составляет 15,2 %.
Экстракция празеодима
Из рисунка 62 видно, что для празеодима образуется лишь одна
экстрагируемая форма - (Pr)(NO3)3(TBP)3.
Рисунок 62- Зависимость доли форм экстрагируемых комплексов Pr3+ от суммарной концентрации Pr3+ в водной фазе
Рисунок 63- Зависимость коэффициента распределения празеодима (D Pr3+) от содержания нитрата аммония в водной фазе
На рисунке 63 и рисунке 64 показаны коэффициенты распределения церия в
зависимости от концентрации нитрата аммония и от равновесной концентрации церия
в водной фазе. Видно, что модель адекватно описывает экспериментальные данные.
Рисунок 64- Зависимость коэффициента распределения празеодима (D Pr3+) от содержания празеодима в экстракте
Среднее отклонение расчёта от экспериментальных данных составляет 50, 3
%.
Экстракция неодима
Рисунок 65- Зависимость доли форм экстрагируемых комплексов Nd3+ от суммарной концентрации Nd3+ в водной фазе
Из рисунка 65 видно, что для неодима образуются две экстрагируемые формы,
но доля формы (Nd)(NO3)3(TBP)4
больше, чем доля (Nd)(NO3)3(TBP)3.
На рисунке 66 и рисунке 67 показаны коэффициенты распределения неодима в
зависимости от концентрации нитрата аммония и от равновесной концентрации
неодима в водной фазе. Видно, что модель адекватно описывает экспериментальные
данные.
Рисунок 66- Зависимость коэффициента распределения неодима (D Nd3+) от содержания нитрата аммония в водной фазе
Рисунок 67- Зависимость коэффициента распределения неодима (D Nd3+) от содержания неодима в экстракте
Среднее отклонение расчёта от экспериментальных данных составляет 7,38 %.
Экстракция самария
Из рисунка 68 видно, что для самария образуются две экстрагируемые формы.
Рисунок 68- Зависимость доли форм экстрагируемых комплексов Sm3+ от суммарной концентрации Sm 3+ в водной фазе
Рисунок 69- Зависимость коэффициента распределения самария (D Sm3+) от
содержания нитрата аммония в водной фазе
На рисунке 69 и рисунке 70 показаны коэффициенты распределения самария в
зависимости от концентрации нитрата аммония и от равновесной концентрации
самария в водной фазе.
Рисунок 70- Зависимость коэффициента распределения самария (D Sm3+) от
содержания самария в экстракте
Среднее отклонение расчёта от экспериментальных данных составляет 9,89 %.
Экстракция европия
Из Рисунок 72 видно, что для европия образуется лишь одна экстрагируемая
форма - (Eu)(NO3)3(TBP)3.
На Рисунок 72 и Рисунок 73 показаны коэффициенты распределения европия в
зависимости от концентрации нитрата аммония и от равновесной концентрации
европия в водной фазе.
Среднее отклонение расчёта от экспериментальных данных составляет 11,7 %.
Рисунок 71- Зависимость доли форм экстрагируемых комплексов Eu3+ от суммарной концентрации Eu 3+ в водной фазе
Рисунок 72- Зависимость коэффициента распределения европия (D Eu3+) от содержания нитрата аммония в водной фазе
Рисунок 73 - Зависимость коэффициента распределения европия (D Eu3+) от содержания европия в экстракте
Экстракция гадолиния
Из рисунка 74 видно, что гадолиний образуются две экстрагируемых формы (Gd)(NO3)3(TBP)3
и (Gd)(NO3)3(TBP)4.
Доля первой формы значительно выше. На рисунке 75 и рисунке 76
показаны коэффициенты распределения гадолиния в зависимости от концентрации
нитрата аммония и от равновесной концентрации гадолиния в водной фазе.
Рисунок 74- Зависимость доли форм экстрагируемых комплексов Gd3+ от суммарной концентрации Gd 3+ в водной фазе
Рисунок 75- Зависимость коэффициента распределения гадолиния (D Gd3+) от содержания нитрата аммония в водной фазе
Рисунок 76- Зависимость коэффициента распределения гадолиния (D Gd3+) от содержания гадолиния в экстракте
Среднее отклонение расчёта от экспериментальных данных составляет 13,8 %.
Экстракция иттрия
Из рисунка 77 видно, что иттрий образуются одну экстрагируемую форму (Y)(NO3)3(TBP)4.
Рисунок 77- Зависимость доли форм экстрагируемых комплексов Y3+ от суммарной концентрации Y 3+ в водной фазе
На рисунке 78 и рисунке 79 показаны коэффициенты распределения иттрия в
зависимости от концентрации нитрата аммония и от равновесной концентрации
иттрия в водной фазе. Видно, что модель адекватно описывает экспериментальные
данные.
Рисунок 78- Зависимость коэффициента распределения иттрия (D Y3+) от содержания нитрата аммония в водной фазе
Рисунок 79- Зависимость коэффициента распределения иттрия (D Y3+) от содержания иттрия в экстракте
Среднее отклонение расчёта от экспериментальных данных составляет 12,86
%.
3.3.4 Серия
4 с концентрацией суммы РЗЭ в водной фазе 0,0542 - 2,52 М и концентрацией
аммиачной селитры 2,29 - 0 М
Экстракция РЗЭ была проведена для элементов - La, Ce, Pr, Nd, Sm, Eu, Gd,
Y. В таблице 11 представлены данные об анализе образцов 4 серии до экстракции,
после экстракции и реэкстракции.
Таблица 11- Результаты анализа проб 4 серии
|
Плотность раствора каждой пробы, г/см3
|
С ∑РЗЭ в исходном растворе, М
|
С HNO3
в исходном растворе, М
|
C NH4NO3
в исходном растворе, М
|
С ∑РЗЭ после экстракции, М
|
С HNO3
после экстракции, М
|
Плотность раствора экстракта г/см3
|
С ∑РЗЭ после реэкстракции, М
|
С HNO3
после реэкстракции, М
|
|
1,1050
|
0,0900
|
0,314
|
2,29
|
0,0542
|
2,83
|
1,08
|
2,83
|
1,73
|
|
1,1380
|
0,200
|
0,629
|
2,17
|
0,100
|
2,36
|
1,10
|
2,36
|
1,18
|
|
1,1652
|
0,400
|
0,943
|
2,05
|
0,165
|
2,12
|
1,14
|
2,12
|
1,18
|
|
1,1943
|
0,450
|
1,18
|
1,93
|
0,250
|
1,89
|
1,13
|
1,89
|
0,943
|
|
1,2255
|
0,500
|
1,73
|
1,81
|
0,333
|
1,42
|
1,16
|
1,42
|
0,943
|
|
1,2563
|
0,600
|
1,89
|
1,69
|
0,450
|
0,943
|
1,18
|
0,943
|
0,707
|
|
1,3155
|
1,00
|
2,36
|
1,45
|
0,783
|
0,707
|
1,23
|
0,707
|
0,707
|
|
1,3636
|
1,33
|
2,83
|
1,21
|
1,03
|
0,589
|
1,27
|
0,589
|
0,589
|
|
1,4241
|
1,53
|
3,77
|
0,966
|
1,33
|
0,472
|
1,33
|
0,472
|
0,472
|
|
1,4738
|
1,68
|
4,24
|
0,725
|
1,67
|
0,472
|
1,37
|
0,472
|
0,472
|
|
1,5487
|
1,93
|
4,95
|
0,362
|
2,37
|
0,314
|
1,45
|
0,314
|
0,314
|
|
1,6341
|
2,25
|
5,42
|
0
|
2,52
|
0,314
|
1,53
|
0,314
|
0,314
|
Приводим Зависимость концентрации РЗЭ в каждом образце от его плотности
(рисунок 80).
Рисунок 80- Зависимость концентрации РЗЭ в каждом образце от его
плотности
Полученные на ICP - OES экспериментальные данные представили
в виде зависимости коэффициента распределения суммы РЗЭ в органической фазе от
концентрации суммы РЗЭ в водной фазе (рисунок 81).
Экспериментальные данные также представлены в виде зависимости
коэффициента распределения индивидуальных РЗЭ в органической фазе от
концентрации индивидуальных РЗЭ в водной фазе (рисунок 82).
- определено методом комплексонометрии ; 2- методом ISP-OES
Рисунок 81- Зависимость коэффициента распределения суммы РЗЭ в
органической фазе от концентрации суммы РЗЭ в водной фазе
Рисунок 82 - Зависимость коэффициента распределения индивидуальных РЗЭ в
органической фазе от концентрации индивидуальных РЗЭ в водной фазе
Различия между коэффициентом распределения определённым методом
комплексонометрии и методом ISP-OES составляют 24,6 %.
По экспериментальным данным, приведенным в таблице Ж.7 и таблице Ж.8 в
приложении Ж, при помощи программы mulcon вычислены значения констант и параметров неидеальности в экстракционной
системе H2O - HNO3 - NH4NO3 - Ln(NO3)3 - ТБФ 100% для четвертой
серии, которые приведены в таблице 12.
Таблица 12 - Набор термодинамических констант и параметров неидеальности
|
Образующаяся форма
|
Термодинамические константы, Lg K
|
|
(La)(NO3)3(TBP)3
|
1,02E+00
|
1,29E-01
|
|
(Ce)(NO3)3(TBP)3
|
1,11E+00
|
1,26E-01
|
|
(Pr)(NO3)3(TBP)3
|
1,15E+00
|
1,38E-01
|
|
(Nd)(NO3)3(TBP)3
|
1,09E+00
|
1,61E-01
|
|
(Nd)(NO3)3(TBP)4
|
-9,16E+00
|
1,08E+00
|
|
(Sm)(NO3)3(TBP)4
|
1,13E+01
|
-1,81E-02
|
|
(Eu)(NO3)3(TBP)3
|
1,28E+00
|
1,61E-01
|
|
(Gd)(NO3)3(TBP)3
|
1,26E+00
|
0,1648
|
Экстракция лантана
Из рисунка 83 видно, что лантан образуются одну экстрагируемую форму (La)(NO3)3(TBP)3.
Рисунок 83- Зависимость доли форм экстрагируемых комплексов La3+ от суммарной концентрации La3+ в водной фазе
На рисунке 86, рисунке 85 и рисунке 84 показаны коэффициенты
распределения лантана в зависимости от концентрации нитрата аммония, от ионной
силы и от равновесной концентрации лантана в водной фазе. Видно, что модель
адекватно описывает экспериментальные данные.
Рисунок 84- Зависимость коэффициента распределения лантана (D La3+) от содержания нитрата аммония в водной фазе
Рисунок 85- Зависимость коэффициента распределения лантана (D La3+) от равновесной ионной силы
Рисунок 86- Зависимость коэффициента распределения лантана (D La3+) от содержания лантана в экстракте
Среднее отклонение расчёта от экспериментальных данных составляет 6,41 %
Экстракция церия
Из рисунка 87 видно, что церий образуются одну экстрагируемую форму
(Се)(NO3)3(TBP)3.
Рисунок 87- Зависимость доли форм экстрагируемых комплексов Се от
суммарной концентрации Се3+ в водной фазе
На рисунке 88 и рисунке 89 показаны коэффициенты распределения церия в
зависимости от концентрации нитрата аммония и от равновесной концентрации церия
в водной фазе. Видно, что модель адекватно описывает экспериментальные данные.
Рисунок 88 - Зависимость коэффициента распределения церия (D Се3+) от содержания
нитрата аммония в водной фазе
Рисунок 89- Зависимость коэффициента распределения церия (D Се3+) от содержания церия
в экстракте
Среднее отклонение расчёта от экспериментальных данных составляет 4,71 %.
Экстракция празеодима
Из рисунка 90 видно, что празеодим образует одну экстрагируемую форму (Pr)(NO3)3(TBP)3.
Рисунок 90- Зависимость доли форм экстрагируемых комплексов Pr3+ от суммарной концентрации Pr3+ в водной фазе
Рисунок 91- Зависимость коэффициента распределения празеодима (D Pr3+) от содержания нитрата аммония в водной фазе
На рисунке 91, рисунке 92 и рисунке 93 показаны коэффициенты
распределения церия в зависимости от концентрации нитрата аммония, ионной силы
и от равновесной концентрации церия в водной фазе. Видно, что модель адекватно
описывает экспериментальные данные.
Рисунок 92- Зависимость коэффициента распределения празеодима (D Pr3+) от равновесной ионной силы
Рисунок 93- Зависимость коэффициента распределения празеодима (D Pr3+) от содержания празеодима в экстракте
Среднее отклонение расчёта от экспериментальных данных составляет 6,79 %.
Экстракция неодима
Из рисунка 94 видно, что неодим образует две экстрагируемых формы.
Однако, доля формы (Nd)(NO3)3(TBP)4
значительно меньше, чем (Nd)(NO3)3(TBP)3.
Рисунок 94 - Зависимость доли форм экстрагируемых комплексов Nd3+ от суммарной концентрации Nd3+ в водной фазе
Рисунок 95- Зависимость коэффициента распределения неодима (D Nd3+) от содержания нитрата аммония в водной фазе
На рисунке 95 и рисунке 96 показаны коэффициенты распределения неодима в
зависимости от концентрации нитрата аммония и от равновесной концентрации
неодима в водной фазе.
Рисунок 96- Зависимость коэффициента распределения неодима (D Nd3+) от содержания неодима в экстракте
Среднее отклонение расчёта от экспериментальных данных составляет 2,1 %.
Экстракция самария
Рисунок 97- Зависимость доли форм экстрагируемых комплексов Sm3+ от суммарной концентрации Sm 3+ в водной фазе
Из рисунка 97 видно, что самарий образует одну экстрагируемую форму (Sm)(NO3)3(TBP)4.
На рисунке 98 и рисунке 99 показаны коэффициенты распределения самария в
зависимости от концентрации нитрата аммония и от равновесной концентрации
самария в водной фазе.
Рисунок 98 - Зависимость коэффициента распределения самария (D Sm3+) от содержания нитрата аммония в водной фазе
Рисунок 99- Зависимость коэффициента распределения самария (D Sm3+) от содержания самария в экстракте
Среднее отклонение расчёта от экспериментальных данных составляет 9,1 %.
Экстракция европия
Из рисунка 100 видно, что европий образует одну экстрагируемую форму (Eu)(NO3)3(TBP)3.
Рисунок 100 - Зависимость доли форм экстрагируемых комплексов Eu3+ от суммарной концентрации Eu 3+ в водной фазе
Рисунок 101- Зависимость коэффициента распределения европия (D Eu3+) от содержания нитрата аммония в водной фазе
На рисунке 101 и рисунке 102 показаны коэффициенты распределения европия
в зависимости от концентрации нитрата аммония и от равновесной ионной силы.
Видно, что модель адекватно описывает экспериментальные данные.
Рисунок 102 - Зависимость коэффициента распределения европия (Eu3+) от равновесной ионной силы
Среднее отклонение расчёта от экспериментальных данных составляет 4,1 %.
Экстракция гадолиния
Из Рисунок 103 видно, что гадолиний образует одну экстрагируемую форму (Gd)(NO3)3(TBP)3.
На рисунке 104 и Рисунок 1055 показаны коэффициенты распределения гадолиния в
зависимости от концентрации нитрата аммония и от равновесной концентрации
гадолиния в водной фазе.
Среднее отклонение расчёта от экспериментальных данных составляет 10,9 %.
Рисунок 103- Зависимость доли форм экстрагируемых комплексов Gd3+ от суммарной концентрации Gd 3+ в водной фазе
Рисунок 104- Зависимость коэффициента распределения гадолиния (D Gd3+) от содержания нитрата аммония в водной фазе
Рисунок 105- Зависимость коэффициента распределения гадолиния (D Gd3+) от содержания гадолиния в экстракте
3.3.5 База
данных по совместной экстракции РЗЭ в системе H2O - HNO3 - NH4NO3
- Ln(NO3)3 - ТБФ 100%
В таблице 13 приведены исходные концентрации суммы РЗЭ в водной фазе,
исходные расчетные концентрации азотной кислоты в водной фазе, равновесная
ионная сила и коэффициенты распределения индивидуальных РЗЭ (La, Ce, Pr, Nd, Sm, Eu, Gd, Y), полученные на приборе ICPE - 9000 Shimadzu после анализа серии 1, серии 2, серии 3 и серии 4.
Таблица 13- Коэффициенты распределения индивидуальных РЗЭ в системе H2O
- HNO3 - NH4NO3 - Ln(NO3)3
- ТБФ 100% при их совместной экстракции (исходные данные результатов анализа ICP-OES)
|
№ точки
|
C NH4NO3, M, в.ф.
|
С ∑РЗЭ, г/л, ICP-OES
в.ф.
|
C HNO3 в.ф., исход. расчетное
|
Ионная сила
|
Коэффициент распределения
|
|
|
|
|
|
La
|
Ce
|
Pr
|
Nd
|
Sm
|
Eu
|
Gd
|
Y
|
|
СЕРИЯ 1
|
|
1
|
8,08
|
1,10
|
0,01
|
8,08
|
19,4
|
24,8
|
31,1
|
29,3
|
69,7
|
63,5
|
31,5
|
н/о
|
|
2
|
7,60
|
3,80
|
0,01
|
7,56
|
1,77
|
2,15
|
2,20
|
2,56
|
4,85
|
5,4
|
10,7
|
н/о
|
|
3
|
7,13
|
10,2
|
0,01
|
7,53
|
3,51
|
6,38
|
5,32
|
5,30
|
9,92
|
14,5
|
10,3
|
8,17
|
|
4
|
6,65
|
19,2
|
0,01
|
7,30
|
2,95
|
3,80
|
4,57
|
4,56
|
8,35
|
10,0
|
8,65
|
12,4
|
|
5
|
6,18
|
39,2
|
0,01
|
7,71
|
1,84
|
2,49
|
3,12
|
3,04
|
7,50
|
7,40
|
6,53
|
6,46
|
|
6
|
5,70
|
53,4
|
0,01
|
7,41
|
1,22
|
1,63
|
1,93
|
1,99
|
4,247
|
4,61
|
4,19
|
3,22
|
|
7
|
4,75
|
93,5
|
0,01
|
8,065
|
0,813
|
1,12
|
1,38
|
1,37
|
2,65
|
3,13
|
3,05
|
2,12
|
|
8
|
3,80
|
140
|
0,01
|
8,85
|
0,615
|
0,840
|
1,02
|
1,02
|
1,94
|
2,36
|
2,65
|
1,77
|
|
9
|
2,85
|
188
|
0,01
|
9,66
|
0,492
|
0,696
|
0,844
|
0,851
|
1,66
|
1,78
|
2,64
|
1,37
|
|
10
|
1,90
|
229
|
0,01
|
9,77
|
0,344
|
0,545
|
0,689
|
0,698
|
1,43
|
1,55
|
1,93
|
1,02
|
|
11
|
0,475
|
296
|
0,01
|
11,3
|
0,314
|
0,519
|
0,680
|
0,667
|
1,36
|
1,41
|
2,18
|
1,02
|
|
12
|
0
|
305
|
0,01
|
10,8
|
0,291
|
0,461
|
0,591
|
0,582
|
1,10
|
1,18
|
1,59
|
0,783
|
|
СЕРИЯ 2
|
|
1
|
5,75
|
1,94
|
0,01
|
5,83
|
9,43
|
12,6
|
12,8
|
15,1
|
17,2
|
н/о
|
30,6
|
н/о
|
|
2
|
5,415
|
8,49
|
0,01
|
5,67
|
4,07
|
4,81
|
5,07
|
6,732
|
8,14
|
н/о
|
н/о
|
н/о
|
|
3
|
5,08
|
20,3
|
0,01
|
5,63
|
2,27
|
2,73
|
2,76
|
3,71
|
4,64
|
н/о
|
6,17
|
н/о
|
|
4
|
4,74
|
16,1
|
0,01
|
5,30
|
3,00
|
3,84
|
4,13
|
5,72
|
7,43
|
н/о
|
н/о
|
н/о
|
|
5
|
4,40
|
22,5
|
0,01
|
5,15
|
2,31
|
2,10
|
3,20
|
4,63
|
6,11
|
н/о
|
7,91
|
н/о
|
|
6
|
4,06
|
37,6
|
0,01
|
5,14
|
1,34
|
1,76
|
1,97
|
2,10
|
3,98
|
4,87
|
5,02
|
н/о
|
|
7
|
3,38
|
64,3
|
0,01
|
5,38
|
0,910
|
1,20
|
1,29
|
2,040
|
2,73
|
3,47
|
4,18
|
н/о
|
|
8
|
2,71
|
150,0
|
0,01
|
7,52
|
0,383
|
0,574
|
0,636
|
0,932
|
1,26
|
1,54
|
2,73
|
|
9
|
2,03
|
202,9
|
0,01
|
8,79
|
0,275
|
0,457
|
0,512
|
0,863
|
1,20
|
1,41
|
2,05
|
н/о
|
|
10
|
1,35
|
315,2
|
0,01
|
12,3
|
0,207
|
0,355
|
0,390
|
0,679
|
0,942
|
1,11
|
1,49
|
н/о
|
|
11
|
0,338
|
353,4
|
0,01
|
13,4
|
0,206
|
0,381
|
0,437
|
0,831
|
1,16
|
1,40
|
1,72
|
н/о
|
|
12
|
0
|
343,3
|
0,01
|
12,5
|
0,199
|
0,362
|
0,407
|
0,724
|
1,01
|
1,18
|
1,29
|
н/о
|
|
СЕРИЯ 3
|
|
1
|
5,79
|
0,781
|
0,401
|
5,95
|
17,5
|
22,9
|
28,4
|
37,0
|
н/о
|
н/о
|
н/о
|
н/о
|
|
2
|
5,48
|
3,50
|
0,802
|
5,87
|
4,68
|
6,54
|
8,60
|
11,6
|
н/о
|
н/о
|
н/о
|
н/о
|
|
3
|
5,18
|
10,9
|
1,20
|
6,06
|
1,79
|
2,52
|
3,52
|
4,87
|
8,78
|
н/о
|
н/о
|
н/о
|
|
4
|
4,87
|
23,5
|
1,60
|
6,43
|
0,868
|
1,25
|
1,71
|
2,38
|
4,52
|
н/о
|
н/о
|
н/о
|
|
5
|
4,57
|
39,0
|
2,00
|
6,79
|
0,509
|
0,765
|
1,06
|
1,53
|
3,21
|
3,28
|
4,63
|
4,00
|
|
6
|
4,26
|
53,86
|
2,41
|
7,40
|
0,462
|
0,731
|
1,01
|
1,47
|
2,89
|
3,16
|
4,17
|
3,94
|
|
СЕРИЯ 3
|
|
7
|
3,65
|
90,2
|
3,21
|
8,49
|
0,230
|
0,358
|
0,497
|
0,705
|
1,53
|
1,62
|
2,23
|
2,09
|
|
8
|
3,05
|
119
|
4,01
|
9,68
|
0,137
|
0,214
|
0,308
|
0,446
|
0,893
|
0,983
|
1,25
|
1,46
|
|
9
|
2,44
|
154
|
4,81
|
11,0
|
0,0957
|
0,149
|
0,215
|
0,307
|
0,580
|
0,662
|
0,818
|
1,02
|
|
10
|
1,83
|
187
|
5,61
|
13,8
|
0,119
|
0,186
|
0,262
|
0,372
|
0,747
|
0,839
|
0,977
|
1,45
|
|
11
|
0,914
|
223
|
6,81
|
14,8
|
0,112
|
0,160
|
0,222
|
0,307
|
0,593
|
0,673
|
0,842
|
1,32
|
|
12
|
0,00
|
271
|
8,02
|
16,1
|
0,0898
|
0,141
|
0,200
|
0,283
|
0,605
|
0,667
|
0,901
|
1,78
|
|
СЕРИЯ 4
|
|
1
|
2,29
|
8,43
|
0,314
|
2,69
|
1,08
|
1,24
|
1,34
|
1,475
|
1,980
|
н/о
|
н/о
|
н/о
|
|
2
|
2,18
|
17,1
|
0,629
|
3,02
|
0,823
|
0,942
|
1,05
|
1,157
|
1,53
|
1,55
|
1,44
|
1,103
|
|
3
|
2,05
|
29,9
|
0,943
|
3,48
|
0,574
|
0,693
|
0,778
|
0,879
|
1,17
|
1,21
|
1,15
|
н/о
|
|
4
|
1,93
|
41,2
|
1,18
|
3,92
|
0,472
|
0,573
|
0,670
|
0,770
|
1,05
|
1,08
|
1,01
|
0,609
|
|
5
|
1,81
|
56,1
|
1,73
|
4,51
|
0,383
|
0,484
|
0,572
|
0,676
|
0,909
|
0,964
|
0,873
|
0,564
|
|
6
|
1,69
|
69,6
|
1,89
|
5,10
|
0,347
|
0,443
|
0,533
|
0,641
|
0,907
|
0,941
|
0,879
|
0,583
|
|
7
|
1,45
|
93,7
|
2,36
|
6,17
|
0,292
|
0,379
|
0,464
|
0,557
|
0,765
|
0,832
|
0,901
|
1,03
|
|
8
|
1,21
|
128
|
2,83
|
7,54
|
0,211
|
0,292
|
0,376
|
0,471
|
0,720
|
0,756
|
0,803
|
1,00
|
|
9
|
0,966
|
159
|
3,77
|
8,87
|
0,175
|
0,252
|
0,332
|
0,428
|
0,646
|
0,715
|
0,777
|
1,10
|
|
10
|
0,725
|
207
|
4,24
|
10,7
|
0,136
|
0,202
|
0,279
|
0,373
|
0,598
|
0,666
|
0,711
|
0,665
|
|
11
|
0,362
|
252
|
4,95
|
12,7
|
0,127
|
0,183
|
0,249
|
0,334
|
0,615
|
0,738
|
1,12
|
|
12
|
0,00
|
310
|
5,42
|
15,4
|
0,152
|
0,198
|
0,249
|
0,315
|
0,498
|
0,568
|
0,705
|
1,40
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Для удобства технологов была проведена сортировка данной таблицы по
различным параметрам водной фазы экстракционной системы (C NH4NO3,
С ∑РЗЭ, C HNO3), а также по полученным в ходе расчетов
коэффициентам распределения индивидуальных РЗЭ. Результаты сортировки
представлены в таблицах Ж.9 - Ж.12 приложения Ж.
В таблице 14 приведены исходные концентрации суммы РЗЭ в водной фазе,
исходные расчетные концентрации азотной кислоты в водной фазе, равновесная
ионная сила и факторы разделения пар РЗЭ, полученные на приборе ICPE - 9000 Shimadzu после анализа серии 1, серии 2,
серии 3 и серии 4.
Таблица 14- Факторы разделения пар РЗЭ в системе H2O - HNO3 - NH4NO3 -
Ln(NO3)3 - ТБФ 100% при их совместной экстракции
|
№ точки
|
C NH4NO3, M, в.ф.
|
С ∑РЗЭ, г/л, ICP-OES
в.ф.
|
C HNO3 в.ф., исход. расчетное
|
Ионная сила
|
Фактор разделения в
|
|
|
|
|
|
Ce/La
|
Pr/Ce
|
Nd/Pr
|
Sm/Nd
|
Eu/Sm
|
Gd/Eu
|
Y/Gd
|
|
СЕРИЯ 1
|
|
1
|
8,08
|
1,10
|
0,01
|
8,08
|
1,28
|
1,26
|
0,941
|
2,38
|
0,910
|
0,496
|
н/о
|
|
2
|
7,60
|
3,80
|
0,01
|
7,56
|
1,21
|
1,02
|
1,17
|
1,89
|
1,11
|
1,99
|
н/о
|
|
3
|
7,13
|
10,2
|
0,01
|
7,53
|
1,82
|
0,834
|
0,996
|
1,87
|
1,46
|
0,706
|
0,797
|
|
4
|
6,65
|
19,2
|
0,01
|
7,30
|
1,29
|
1,20
|
0,997
|
1,83
|
1,20
|
0,864
|
1,43
|
|
5
|
6,18
|
39,2
|
0,01
|
7,71
|
1,35
|
1,25
|
0,976
|
2,47
|
0,987
|
0,882
|
0,989
|
|
6
|
5,70
|
53,4
|
0,01
|
7,41
|
1,34
|
1,19
|
1,03
|
2,14
|
1,09
|
0,909
|
0,768
|
|
7
|
4,75
|
93,5
|
0,01
|
8,065
|
1,38
|
1,23
|
0,995
|
1,94
|
1,18
|
0,974
|
0,697
|
|
8
|
3,80
|
140
|
0,01
|
8,85
|
1,37
|
1,21
|
1,00
|
1,90
|
1,22
|
1,12
|
0,667
|
|
9
|
2,85
|
188
|
0,01
|
9,66
|
1,42
|
1,21
|
1,01
|
1,95
|
1,07
|
1,49
|
0,520
|
|
10
|
1,90
|
229
|
0,01
|
9,77
|
1,59
|
1,26
|
1,01
|
2,06
|
1,08
|
1,25
|
0,525
|
|
11
|
0,475
|
296
|
0,01
|
11,3
|
1,65
|
1,31
|
0,982
|
2,04
|
1,04
|
1,54
|
0,469
|
|
12
|
0
|
305
|
0,01
|
10,8
|
1,58
|
1,28
|
0,985
|
1,89
|
1,08
|
1,35
|
0,491
|
|
СЕРИЯ 2
|
|
1
|
5,75
|
1,94
|
0,01
|
5,83
|
1,33
|
1,02
|
1,18
|
1,14
|
н/о
|
н/о
|
н/о
|
|
2
|
5,415
|
8,49
|
0,01
|
5,67
|
1,18
|
1,05
|
1,33
|
1,21
|
н/о
|
н/о
|
н/о
|
|
3
|
5,08
|
20,3
|
0,01
|
5,63
|
1,20
|
1,01
|
1,34
|
1,25
|
н/о
|
н/о
|
н/о
|
|
4
|
4,74
|
16,1
|
0,01
|
5,30
|
1,28
|
1,07
|
1,39
|
1,30
|
н/о
|
н/о
|
н/о
|
|
5
|
4,40
|
22,5
|
0,01
|
5,15
|
1,30
|
1,07
|
1,44
|
1,32
|
н/о
|
н/о
|
н/о
|
|
6
|
4,06
|
37,6
|
0,01
|
5,14
|
1,32
|
1,11
|
1,52
|
1,33
|
1,23
|
1,03
|
н/о
|
|
7
|
3,38
|
64,3
|
0,01
|
5,38
|
1,32
|
1,08
|
1,58
|
1,34
|
1,27
|
1,20
|
н/о
|
|
8
|
2,71
|
150,0
|
0,01
|
7,52
|
1,50
|
1,11
|
1,46
|
1,35
|
1,23
|
1,77
|
н/о
|
|
9
|
2,03
|
202,9
|
0,01
|
8,79
|
1,66
|
1,12
|
1,69
|
1,39
|
1,17
|
1,46
|
н/о
|
|
10
|
1,35
|
315,2
|
0,01
|
12,3
|
1,71
|
1,10
|
1,74
|
1,39
|
1,18
|
1,33
|
н/о
|
|
11
|
0,338
|
353,4
|
0,01
|
13,4
|
1,85
|
1,15
|
1,90
|
1,39
|
1,21
|
1,23
|
н/о
|
|
12
|
0
|
343,3
|
0,01
|
12,5
|
1,82
|
1,12
|
1,78
|
1,39
|
1,17
|
1,09
|
н/о
|
|
СЕРИЯ 3
|
|
1
|
5,79
|
0,781
|
0,401
|
5,95
|
1,30
|
1,24
|
1,30
|
н/о
|
н/о
|
н/о
|
н/о
|
|
2
|
5,48
|
3,50
|
0,802
|
5,87
|
1,40
|
1,32
|
1,35
|
н/о
|
н/о
|
н/о
|
н/о
|
|
3
|
5,18
|
10,9
|
6,06
|
1,41
|
1,40
|
1,39
|
1,802
|
н/о
|
н/о
|
н/о
|
|
4
|
4,87
|
23,5
|
1,60
|
6,43
|
1,44
|
1,37
|
1,40
|
1,90
|
н/о
|
н/о
|
н/о
|
|
5
|
4,57
|
39,0
|
2,00
|
6,79
|
1,50
|
1,38
|
1,44
|
2,10
|
1,02
|
1,41
|
0,865
|
|
6
|
4,26
|
53,86
|
2,41
|
7,40
|
1,58
|
1,38
|
1,46
|
1,97
|
1,10
|
1,32
|
0,944
|
|
7
|
3,65
|
90,2
|
3,21
|
8,49
|
1,56
|
1,39
|
1,42
|
2,17
|
1,06
|
1,38
|
0,938
|
|
8
|
3,05
|
119
|
4,01
|
9,68
|
1,57
|
1,44
|
1,45
|
2,00
|
1,10
|
1,27
|
1,17
|
|
9
|
2,44
|
154
|
4,81
|
11,0
|
1,56
|
1,44
|
1,43
|
1,88
|
1,14
|
1,24
|
1,25
|
|
10
|
1,83
|
187
|
5,61
|
13,8
|
1,57
|
1,41
|
1,42
|
2,01
|
1,12
|
1,17
|
1,48
|
|
11
|
0,914
|
223
|
6,81
|
14,8
|
1,42
|
1,38
|
1,38
|
1,93
|
1,14
|
1,25
|
1,57
|
|
12
|
0
|
271
|
8,02
|
16,1
|
1,57
|
1,42
|
1,41
|
2,14
|
1,10
|
1,35
|
1,98
|
|
СЕРИЯ 4
|
|
1
|
2,29
|
8,43
|
0,314
|
2,69
|
1,14
|
1,09
|
1,10
|
1,34
|
н/о
|
н/о
|
н/о
|
|
2
|
2,18
|
17,1
|
0,629
|
3,02
|
1,15
|
1,11
|
1,1
|
1,32
|
1,02
|
0,928
|
0,765
|
|
3
|
2,05
|
29,9
|
0,943
|
3,48
|
1,21
|
1,12
|
1,13
|
1,33
|
1,03
|
0,956
|
н/о
|
|
4
|
1,93
|
41,2
|
1,18
|
3,92
|
1,21
|
1,17
|
1,1
|
1,36
|
1,03
|
0,932
|
0,604
|
|
5
|
1,81
|
56,1
|
1,73
|
4,51
|
1,27
|
1,18
|
1,18
|
1,34
|
1,06
|
0,905
|
0,646
|
|
6
|
1,69
|
69,6
|
1,89
|
5,10
|
1,28
|
1,20
|
1,20
|
1,41
|
1,04
|
0,934
|
0,663
|
|
7
|
1,45
|
93,7
|
2,36
|
6,17
|
1,30
|
1,22
|
1,20
|
1,38
|
1,09
|
1,08
|
1,14
|
|
8
|
1,21
|
128
|
2,83
|
7,54
|
1,38
|
1,29
|
1,25
|
1,53
|
1,05
|
1,06
|
1,25
|
|
9
|
0,966
|
159
|
3,77
|
8,87
|
1,44
|
1,32
|
1,29
|
1,51
|
1,11
|
1,09
|
1,42
|
|
10
|
0,725
|
207
|
4,24
|
10,7
|
1,49
|
1,38
|
1,34
|
1,60
|
1,11
|
1,07
|
0,935
|
|
11
|
0,362
|
252
|
4,95
|
12,7
|
1,44
|
1,36
|
1,34
|
1,65
|
1,12
|
1,20
|
1,52
|
|
12
|
0,00
|
310
|
5,42
|
15,4
|
1,31
|
1,26
|
1,27
|
1,58
|
1,14
|
1,24
|
1,99
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Для таблицы 14 также была проведена сортировка по различным параметрам
водной фазы экстракционной системы (C NH4NO3, С ∑РЗЭ,
C HNO3), а также по полученным в ходе расчетов факторам разделения
пар РЗЭ. Результаты сортировки представлены в таблицах Ж.13 -- Таблица 14 Таблица 15 Таблица 16 Таблица 17 Ж18
приложения Ж.
Заключение и выводы
В ходе дипломной работы было определено изменение объёма и плотности ТБФ
при экстракции нитратов редкоземельных элементов.
Были приготовлены и проанализированы 4 серии растворов с разными
концентрациями компонентов экстракционной системы (C ∑РЗЭ, С HNO3, С NH4NO3).
На основании экспериментальных опытов и расчетов ICP - OES
создана база данных по совместной экстракции лёгких редкоземельных элементов в
присутствии HNO3, NH4NO3 и ТБФ, приспособленная
для использования в заводской лаборатории с целью облегчения проведения
технологического процесса.
На основе имеющихся экспериментальных данных были определены
термодинамические константы и параметры неидеальности экстрагируемых комплексов
для экстракционной системы H2O - HNO3 - NH4NO3
- Ln(NO3)3 - ТБФ 100%.
Список
использованных источников
1 Золотов Ю.А. Экстракция внутрикомплексных соединений / Ю.А.
Золотов. - М. : Наука, 1968. - С. 288
Михайличенко А.И. Редкоземельные металлы / А.И. Михайличенко,
Е.Б. Михлин Ю.Б. Патрикеев. - М. : Металлургия, 1987. - С. 5, 210-221
Лурье Ю.Ю. Справочник по аналитической химии / Ю.Ю. Лурье. -
М.: Химия, 1989. - С. 388
Беляев А.И. Физико-химические основы очистки металлов и
полупроводниковых материалов / А.И, Беляев. - М.: Металлургия, 1973. - 224 с.
Большаков К.А. Химия и технология редких и рассеянных
элементов / К.А. Большаков. - М.: Высшая школа, 1976. - Ч.1. - 360 с.
Лазарев Н.В. Вредные вещества в промышленности: справочник
для химиков, инженеров и врачей / Н.В. Лазарев, Э.И. Левина. - Л.: Химия, -1977
- Т.1,2,3.
Равдель А.А. Краткий справочник физико-химических величин /
А.А. Равдель, А.М. Пономарев. - Изд. 10-е, перераб. и доп.- СПб.: Иван Федоров,
2003. - 624 с.
ГОСТ 8.417-2002 Единицы величин. Взамен ГОСТ 8.417-81; введ.
2003-09-01. - Минск: Межгос. совет по стандартизации, метрологии и сертификации;
M.: Изд-во стандартов, 2003. - 27 с. - (Государственная система обеспечения
единства измерений).
Р01-2007. Библиографическое описание документа. Примеры
оформления. - Взамен Р01-97 ; введ. 2008-01-01. - СПб. : ИК «Синтез», 2007. -
10 с.
СТП СПбГТИ 006 - 2009. Подготовка и оформление текстовых
авторских оригиналов для издания. - Взамен СТП СПбГТИ 006 - 2005; введен 2009 -
07 - 01. - СПб.: ИК «Синтез», 2009. - 32 с. - (Комплексная система управления
качеством деятельности вуза).
СанПин 2.1.1.1200-03. Санитарно-защитные зоны и санитарная
классификация предприятий, сооружений и иных объектов: утв. Гл. гос. Санит.
Врачом Российской Федерации 18.04.03: ввод в действие 15.06.03. - М.:
Федеральный центр Госсанэпиднадзора Минздрава России, 2003. - 11 с.
Приложение А
Сертификат качества карбонатов РЗЭ
Приложение Б
Экономическая оценка результатов исследования
Научно-технический процесс, достигнутый за последние годы в химии во
многом обязан успешному применению материалов, в основе которых лежат редкие
элементы.
Состояние методов избирательного выделения металлов из растворов не
всегда удовлетворяет требованиям к нижним границам содержания извлекаемого
металла. Постоянно ощущается необходимость в простых по выполнению, точных,
чувствительных методиках, которые позволяли бы выделить компонент в сложной по
составу смеси. Для решения этой проблемы ученые привлекли методы
концентрирования, которые позволили в значительной степени устранить эти
трудности.
Одним из перспективных методов разделения и концентрирования является
экстракция. Экстракционные методы пригодны для абсолютного и относительного
концентрирования, извлечения в экстракт микроэлементов или матрицы,
индивидуального и группового выделения элементов.
Экстракционный метод разделения РЗЭ вытеснил метод осаждения, который
оказался менее эффективным и менее быстрым.
Цели и задачи дипломной работы :
• Проведение совместной экстракции РЗЭ
и азотной кислоты в экстракционной системе 100 % ТБФ - NH4NO3 - HNO3 ;
• Моделирование процессов экстракции
РЗЭ и азотной кислоты в экстракционной системе 100 % ТБФ - NH4NO3 - HNO3 ;
• Создание базы данных по совместной
экстракции лёгких РЗЭ в присутствии HNO3
и NH4NO3 три-н-бутилфосфатом.
Экстракция РЗЭ применяется на предприятиях, в технологический процесс
которых входит разделение РЗЭ, очистка каких-либо соединений или концентратов
от примесей РЗЭ. Также метод экстракции РЗЭ используется при получении
фосфорной кислоты из фосфатов (апатит), а так как потребление удобрений в мире
неуклонно растет, то растет и число предприятий, занимающихся производством
данной кислоты.
Примером такого предприятия может послужить «Акрон» - один из ведущих
вертикально интегрированных производителей минеральных
удобрений в России и мире. Здесь получают фосфорную кислоту, как одну из составляющих
удобрений. После получения фосфорной кислоты из апатитов, необходимо очистить
ее от РЗЭ, содержащихся в апатитах. Для этого методом осаждения получают осадок
двойных солей РЗЭ, содержащих фосфаты, которые впоследствии можно использовать
для получения чистых
РЗЭ. Осадок фильтруют азотной кислотой и очищают с помощью ТБФ в
предназначенной для этого колонне.
Наша база данных (а также база, созданная в том году на нашей кафедре
Бычковой Марией) позволит автоматизировать систему каскадов и сделать ее более
усовершенствованной и менее затратной. Этого можно достичь, зная коэффициенты
распределения и массовые коэффициенты распределения РЗЭ, рассчитанные в ходе
моего исследования для системы : 100 % ТБФ - NH4NO3 - HNO3.
Приведенные в настоящей работе экспериментальные данные,
физико-химические и математические модели, параметры фазовых экстракционных
равновесий могут быть использованы при разработке новых технологий
экстракционного разделения и очистки РЗМ, а также представляют собой справочный
материал.
Результаты данной работы могут представлять интерес в качестве
справочно-расчетного инструмента при проектировании установок по разделению и
выделению РЗЭ экстракционным методом, так как в настоящее время на производстве
экстракционный метод стал основным в схеме разделения РЗЭ.
В данной работе была проведена экономическая оценка результатов
исследования.
В таблице Б.1 представлена оценка конкурентноспособности экстракционного
метода.
Таблица Б.1 - Сравнение конкурентоспособности товара
|
Перечень требований идеальной модели
|
Коэффициент веса
|
Экспертная оценка
|
Оценка с учетом веса
|
Выигрыш (+) или проигрыш (-) относительно :
|
|
|
Идеальная модель
|
Совместная экстракция из растворов нитрата аммония
|
Дробное осаждение
|
Экстракция из азотнокислых растворов
|
Идеальная модель
|
Совместная экстракция из растворов нитрата аммония
|
Дробное осаждение
|
Экстракция из азотнокислых растворов
|
Идеальная модель
|
Дробное осаждение растворов
|
Экстракция из азотнокислых растворов
|
|
Производительность (кг/год)
|
2
|
5
|
3
|
1
|
4
|
10
|
6
|
2
|
8
|
-4
|
4
|
-2
|
|
Стоимость (руб./кг)
|
2
|
5
|
3
|
1
|
4
|
10
|
6
|
2
|
8
|
-4
|
4
|
-2
|
|
Эффективность разделения РЗЭ (выход продукта, %)
|
2
|
5
|
4
|
1
|
3
|
10
|
8
|
6
|
-2
|
6
|
2
|
|
Энергоемкость процесса извлечения (кВт*ч)
|
2
|
5
|
4
|
3
|
4
|
10
|
8
|
6
|
8
|
-2
|
2
|
0
|
|
Экологическая безопасность
|
2
|
5
|
3
|
4
|
4
|
10
|
6
|
8
|
8
|
-4
|
-2
|
-2
|
|
Итого:
|
10
|
25
|
|
|
|
50
|
34
|
20
|
38
|
-16
|
14
|
-4
|
Расчет договорной цены
.1 Расчет суммы затрат на сырье, материалы, реактивы, покупные изделия и
полуфабрикаты
Затраты на сырье, материалы и реактивы (Зм), израсходованные
на проведение исследования, определяются исходя из цены каждого вида ресурса (Цi)
и его расхода (Рi) в натуральных единицах :
 , (Б.1)
, (Б.1)
где i = 1, 2, 3…n - виды материальных
ресурсов.
Общая сумма затрат по данной статье расходов представлена в таблице Б.2
Таблица Б.2 - Расчет суммы затрат на сырье, материалы и реактивы
|
Наименование материала
|
Техническая характеристика
|
Ед. изм.
|
Израсходованное количество
|
Цена, руб.
|
Сумма затрат, руб.
|
|
NH4NO3
|
ХЧ, ГОСТ 22867 - 77
|
кг
|
0,8
|
38
|
30,4
|
|
HNO3
|
ОСЧ, ГОСТ 11125-84
|
л
|
0,4
|
162
|
64,8
|
|
NaOH
|
ЧДА, ГОСТ 4328 -77
|
кг
|
0,2
|
103
|
20,6
|
|
Трилон Б
|
Ч, ГОСТ 10652-73
|
л
|
0,5
|
344
|
172
|
|
HСl
|
ХЧ, ГОСТ 3118-77
|
л
|
0,1
|
286
|
28,6
|
|
CH3COOH
|
ХЧ, ГОСТ 61-75
|
л
|
0,2
|
121
|
24,2
|
|
La2O3
|
Ч
|
кг
|
0,007
|
5000
|
35
|
|
CeO2
|
Ч
|
кг
|
0,014
|
500
|
7
|
|
Pr6O11
|
Ч
|
кг
|
0,002
|
15000
|
30
|
|
Nd2O3
|
Ч
|
кг
|
0,004
|
8000
|
32
|
|
Sm2O3
|
Ч
|
кг
|
0,0003
|
10000
|
3
|
|
Трибутилфосфат
|
Ч, ТУ 6-09-3536-74
|
л
|
0,3
|
280
|
84
|
|
Итого
|
|
|
|
|
531,6
|
|
Прочие материалы (фильтровальная бумага, индикатор, прочие
реактивы)
|
|
|
5% от основных расходов на реактивы
|
|
27
|
|
Итого
|
|
|
|
|
559
|
.2 Расчет суммы затрат на энергоресурсы
Расчет затрат на электроэнергию (Зэ/э) производится по формуле
:
 , (Б.2)
, (Б.2)
где Мi - установленная мощность i оборудования, используемого при проведении исследований,
кВт. Берется по паспортным данным используемого оборудования ;
Ti - время использования i оборудования
за весь период исследования, ч ;
Цэ/э - цена одного часа электроэнергии, руб. ;
Кмi
- коэффициент использования оборудования по мощности, доли единицы. Км принимается
в интервале от 0,7 до 0,9
Исходные данные и расчет суммы затрат на электроэнергию представлены в
таблице Б.3.
Таблица Б.3 - Расчет суммы затрат на электроэнергию
|
Наименование используемого оборудования
|
Установленная мощность в КВт, Mi
|
Число единиц оборудования, n
|
Время использования оборудования , час. Ti
|
Коэффициент используемой мощности, Км
|
Цена одного КВт /часа Электроэнергии, руб. Цэ
|
Затраты на электроэнергию руб, Зэ
|
|
Дистиллятор
|
3
|
1
|
20
|
0,9
|
3,53
|
190,62
|
|
Плитка электрическая
|
1,5
|
1
|
140
|
0,8
|
3,53
|
593,04
|
|
Вытяжной шкаф
|
1,5
|
1
|
7
|
0,9
|
3,53
|
33,4
|
|
Сушильный шкаф
|
0,6
|
1
|
30
|
0,9
|
3,53
|
57,19
|
|
ПЭВМ
|
0,5
|
1
|
400
|
0,9
|
3,53
|
635,4
|
|
Шейкер "memmert"
|
0,23
|
1
|
54
|
0,9
|
3,53
|
39,5
|
|
Лампы дневного освещения
|
0,035
|
6
|
750
|
0,9
|
3,53
|
83,40
|
|
Весы аналитические
|
0,025
|
1
|
8
|
0,9
|
3,53
|
0,6
|
|
рН-метр
|
0,009
|
1
|
70
|
0,7
|
3,53
|
1,6
|
|
Мешалка магнитная
|
0,003
|
1
|
90
|
0,7
|
3,53
|
0,7
|
|
Итого
|
|
|
|
|
|
1635
|
Расчет затрат на другие виды энергии (Зэi) осуществляется по формуле:
 , (Б.3)
, (Б.3)
где Рэi
- расход i-того энергоресурса, в натуральных
единицах измерения ;
Цэi -
цена i - того вида энергоресурса за ед.,
руб.
Цена обычной холодной воды 21,03 руб./м3. Всего было потрачено
20 м3 воды. Тогда затраты на воду составили :
З = 20*21,03 = 420,6 руб.
З = 421 руб.
.3 Расчет суммы затрат на приборы, оборудование для
научно-экспериментальных работ и суммы амортизационных отчислений
Сумма амортизационных отчислений (А) определяется по следующей формуле:
 , (Б.4)
, (Б.4)
где Фn -
первоначальная (восстановительная) стоимость оборудования и приборов, руб.;
На - годовая норма амортизации, берется из специального
справочника, % ;
Т - время использования конкретного оборудования и/или прибора для
проводимого исследования, месс.
Расчет стоимости специального оборудования и суммы амортизационных
отчислений приведен в таблице Б.4 .
Таблица Б.4 - Расчет стоимости специального оборудования и суммы
амортизационных отчислений
|
Наименование используемого оборудования
|
Кол-во ед., шт.
|
Ст-ть ед. оборудования. руб.
|
Сто-ть всего оборудования, руб.
|
Годовая норма амортизации, %
|
Время использования, мес.
|
Сумма амортизации
|
|
Дистиллятор
|
1
|
57000
|
57000
|
20
|
7
|
6650
|
|
Плитка электрическая
|
1
|
2600
|
2600
|
100
|
7
|
1517
|
|
Вытяжной шкаф
|
1
|
65800
|
65800
|
20
|
7
|
7677
|
|
Сушильный шкаф
|
1
|
30000
|
30000
|
20
|
7
|
3500
|
|
Персональный компьютер
|
1
|
20000
|
20000
|
100
|
7
|
11667
|
|
Шейкер "memmert"
|
1
|
30000
|
30000
|
20
|
7
|
3500
|
|
Весы аналитические
|
1
|
20000
|
20000
|
100
|
7
|
11667
|
|
pH-метр Thermo Orion 720A Plus
|
1
|
27000
|
27000
|
100
|
7
|
15750
|
|
Мешалка магнитная
|
1
|
3800
|
3800
|
100
|
7
|
2217
|
|
ICP
|
1
|
3500000
|
3500000
|
20
|
0,2
|
11667
|
|
Итого
|
10
|
|
|
|
|
75812
|
Амортизационные отчисления от приборов, стоимость которых менее 30000
руб. составляет 100%, а более 30000 руб. - 20 %.
Расчет затрат на стеклянные приборы и посуду приведены в таб. Б.5.
Таблица Б.5 - Расчет затрат на стеклянные приборы и посуду
|
Наименование используемого оборудования
|
Объем, см3
|
Кол-во ед., шт.
|
Стоимость единицы оборудования, руб.
|
Стоимость всего оборудования, руб.
|
|
Колба коническая
|
100
|
12
|
53,35
|
640,2
|
|
250
|
2
|
65,89
|
131,8
|
|
Колба мерная
|
1000
|
1
|
1177
|
1177
|
|
2000
|
1
|
2057
|
2057
|
|
Цилиндр мерный
|
50
|
1
|
269,5
|
269,5
|
|
250
|
1
|
451
|
451
|
1
|
1155
|
1155
|
|
Пробирки
|
15
|
48
|
30
|
1440
|
|
Пипетка
|
1
|
2
|
82,5
|
165
|
|
5
|
2
|
75
|
150
|
|
10
|
2
|
90,2
|
180,4
|
|
Стакан
|
50
|
3
|
52
|
156
|
|
1000
|
1
|
165
|
825
|
|
Итого
|
|
|
|
8798
|
.4 Расчет суммы заработной платы с обязательными начислениями
Основная заработная плата (ЗПосн) руководителя дипломной
работы определяется по формуле :
 , (Б.5)
, (Б.5)
где Тст - часовая тарифная ставка данного работника, руб. ;
Тф - время, затраченное конкретным работником, на данное
исследование, ч.
Часовая тарифная ставка может быть определена по формуле :
 , (Б.6)
, (Б.6)
где Ок - оклад работника за месяц, руб. ;
Д - среднее число рабочих дней в месяц (принято считать 22), дн.;
Тсм - продолжительность рабочего дня, ч.
Тст =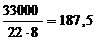 руб.
руб.
ЗПосн = руб.
руб.
Дополнительная заработная плата начисляется в размере 15 % от суммы
основной заработной платы :
Здоп
= 67875 Ч 0,15 = 10181,25 руб.
Здоп
= 10181 руб.
Обязательные начисления на социальные нужды берутся в виде установленного
действующим законодательством РФ на данный момент времени процента (34 %) от
суммы основной заработной платы :
Зсс
= (67875 +10181,25) Ч 0,34 = 25539,125 руб.
Зсс=
25539 руб.
Затраты
на основную заработную плату исследователя определяются исходя из размера
месячного заработка (стипендии), умножая на число месяцев, которые отводятся на
выполнение работы.
Зисп
= ЗПисп · Т (Б.7)
где
ЗПисп - заработная плата исследователя (стипендия) ;
Т
- число месяцев отводимых на выполнение дипломной работы (7 месяцев).
Зисп
= 2500. 7 = 17500 руб.
Сведем
полученные данные в таблицу Б.6
Таблица
В.6 - Расчет затрат на заработную плату и обязательных начислений на нее
|
Категория работников
|
Кол-во человек
|
Часовая тарифная ставка, руб.
|
Затраченное время, час.
|
Основная заработная плата, руб.
|
Дополнительная заработанная плата, руб.
|
Обязательные начисления, руб.
|
Итого затраты на заработную плату, руб.
|
|
Научный руководитель
|
1
|
187,5
|
362
|
67875
|
10181,25
|
25539,125
|
103595,375
|
|
Исследователь
|
1
|
-
|
-
|
17500
|
-
|
-
|
17500
|
|
Итого:
|
|
|
|
85375
|
10181
|
25539
|
121095
|
.5 Расчет суммы расходов на использование вычислительной техники
Рассчитываются данные суммы, исходя из количества часов вычислительной
техники и стоимости одного машино/часа ее эксплуатации. Для расчетов средняя
стоимость одного машино/часа использования компьютера может быть принята 200
руб. в час. В итоге сумма затрат по данной статье равна :
∙ 450= 90000 руб.
.6 Расчет сумм накладных расходов
Смета затрат на проведение научно-исследовательской работы представлена в
таблице Б.7.
Таблица Б.7 - Смета затрат на проведение научно-исследовательской работы
|
Наименование статей затрат
|
Сумма, руб.
|
Удельный вес, %
|
|
1 Сырье, материалы, реактивы
|
559
|
0,1
|
|
2 Энергетические ресурсы
|
|
|
|
а) электроэнергия
|
1635
|
0,4
|
|
б) вода
|
421
|
0,1
|
|
3 Сумма амортизационных отчислений специального
оборудования
|
75812
|
19,5
|
|
4 Стеклянные приборы и посуда
|
8798
|
2,3
|
|
5 Основная заработная плата
|
|
|
|
а) исполнителя
|
17500
|
4,5
|
|
б) научного руководителя
|
67875
|
17,5
|
|
6 Дополнительная заработная плата
|
10181
|
2,6
|
|
7 Отчисления на социальное страхование
|
25539
|
6,6
|
|
8 Использование вычислительной техники
|
90000
|
23,2
|
|
Итого
|
298320
|
76,9
|
|
9 Накладные расходы (30%)
|
89496
|
23,1
|
|
Всего затрат
|
390000
|
100
|
.7 Определение договорной цены на НИР
Договорная цена (Ц) рассчитывается по формуле :
 (Б.8)
(Б.8)
где
Зн- затраты на выполнение исследования, предусмотренного
планом дипломной работы, руб. ;
Р
- уровень рентабельности исследования, %;
К
- коэффициент, учитывающий поощрительную надбавку за качество разработки,
принят за 1.
Уровень
рентабельности исследования принимается равным 20 %.
Договорная
цена на НИР равна :
 руб.,
руб.,
Ц
= 468000 руб.
Выводы
Целью
данной работы является представление варианта технологии экстракционного разделения
РЗЭ. В результате работы была создана методика, в которой используются
сравнительно дешевые реагенты, технологически простые методы, что могло бы
позволить использовать их в промышленном масштабе.
2 Метод экстракционного разделения РЗЭ обладает высокой эффективностью.
На основании оценки конкурентоспособности можно сделать вывод, что
экстракция является наиболее эффективным методом выделения и разделения РЗЭ.
В результате расчётов получилась договорная цена, равная
Ц= 468000 рублей.
Приложение B
Охрана труда и окружающей среды
Введение
Экспериментальная часть дипломной работы проводилась в СПбГТИ (ТУ) на
кафедре технологии редких и рассеянных элементов и наноматериалов на их основе.
Работа посвящена моделированию процессов экстракции редкоземельных
элементов и азотной кислоты в системе H2O - HNO3 - NH4NO3 - Ln(NO3)3 - ТБФ 100%.
Все работы проводились в помещениях второго класса в соответствии и с
учетом нормативных документов. Рабочее место соответствует правилам по охране
труда. В ходе эксперимента проводилась работа с химическими веществами, а также
на различных приборах и лабораторным оборудованием.
Дипломная работа проводилась с учетом оценки уровней производственной
санитарии и гигиены труда, вредных физических факторов производственной среды,
системы вентиляции, освещения производственного помещения, категорированием
производств, помещений, наружных установок, зон, взрывозащищенного
оборудования, определения размеров санитарно-защитной зоны.
Рассмотрим подробно каждый из составляющих элементов охраны труда и
окружающей среды.
Химический фактор и пыль на производстве (таблица В.1)
Таблица В.1 - Химический фактор и пыль на производстве
|
Характеристики
|
Вещество
|
|
1
|
3
|
4
|
5
|
|
1 Название
|
Трибутилфосфат
|
Хлороводородная кислота
|
Уксусная кислота
|
Азотная кислота
|
|
2 Химическая формула
|
(С4H9O)3PO
|
HCl
|
CH3COOH
|
HNO3
|
|
3 Агрегатное состояние
|
ж
|
ж
|
ж
|
ж
|
|
4 ПДК воздуха рабочей зоны, мг/м3
|
0,5
|
5
|
5
|
2
|
|
5 Класс опасности
|
2
|
2
|
3
|
3
|
|
6 Особенности действия
|
Нарушение деятельности сердечно - сосудистой системы
|
Раздражение верхних дыхательных путей
|
Раздражение слизистой оболочки и верхних дыхательных путей
|
Раздражение верхних дыхательных путей, ожоги
|
|
7 Рабочее место
|
Промывка водой, применение в качестве экстрагента
|
Определение концентрации NaOH с помощью pH-м.
|
Служит реактивом при приготовление ацетатно-аммиачного
буфера
|
Применение в качестве реэкстрагента
|
|
8 Периодичность контроля
|
1 раз в месяц
|
1 раз в квартал
|
|
9 Средства защиты :
|
|
|
9.1 Индивидуальные :
|
Резиновые перчатки - ГОСТ 12.4.010-75, халат - ГОСТ
12.4.131-83, очки защитные - ГОСТ 12.4.230.1-2007
|
|
9.2 Коллективные :
|
Вентиляция - СНиП 2.04.05-91
|
Продолжение таблицы В.1
|
Характеристики
|
Вещество
|
|
1
|
2
|
|
1 Название
|
Нитрат аммония
|
Гидроксид натрия
|
|
2 Химическая формула
|
NH4NO3
|
NaOH
|
|
3 Агрегатное состояние
|
ж
|
ж
|
|
4 ПДК воздуха рабочей зоны, мг/м3
|
10
|
0,5
|
|
5 Класс опасности
|
4
|
2
|
|
6 Особенности действия
|
Оказывает раздражающее действие на верхние дыхательные
пути, глаза и кожу
|
При попадании на кожу вызывает химические ожоги
|
|
7 Рабочее место
|
Входит в состав экстрагируемой системы, растворение с РЗЭ
|
Определение концентрации кислоты азотной в системе с
помощью pH-метра
|
|
9 Периодичность контроля
|
1 раз в квартал
|
1 раз в месяц
|
|
9 Средства защиты :
|
|
|
9.1 Индивидуальные :
|
Резиновые перчатки - ГОСТ 12.4.010-75, халат - ГОСТ
12.4.131-83, очки защитные - ГОСТ 12.4.230.1-2007
|
|
9.2 Коллективные :
|
Вентиляция - СНиП 2.04.05-91
|
2 Вредные физические факторы производственной среды (таблица В.2)
Таблица В.2 - вредные физические факторы производственной среды
|
Вредные факторы
|
Рабочее место
|
|
Шум (ультразвук, инфразвук)
|
|
|
1 Характер шума
|
непостоянный
|
|
2 Нормативная величина в дБ А
|
60
|
|
Микроклимат
|
|
|
1 Тип микроклимата и нормативные значения параметров
микроклимата:
|
допустимый
|
|
1.1 температура воздуха, єС
|
19-24
|
|
1.2 влажность воздуха, %
|
15-75
|
|
1.3 скорость движения воздуха, м/с
|
0,1-0,2
|
|
1.4 интенсивность теплового облучения, Вт/м2
|
≤100
|
|
1.5 температура поверхностей
|
18-25
|
Сведения о системе вентиляции
Рассчитываем количество воздуха, удаляемое постоянно действующей
вентиляцией в м3/ч по формуле :
LП = КА • V, (В.1)
где  кратность вентиляции ;
кратность вентиляции ;
V -
строительный объем помещения, м3 ;
LП = 5 ∙ 140 = 700 м3/ч
Находим производительность вентилятора в м3/ч по формуле :
Q = К
• LП, (В.2)
где К - коэффициент, учитывающий потери или подсос воздуха (для стальных,
асбестоцементных, пластмассовых воздуховодов К=1,1) ;
Q= 1,1∙700=770 м3/ч
Необходимая установочная мощность на валу электродвигателя вентилятора N (Вт) определяется по формуле :
N = Kз • Q • H /(3600 • 102• мв • мп),
(В.3)
где Kз - коэффициент запаса, равный 1,1-1,5 ;
Q -
производительность вентилятора, м3/ч ;
H -
создаваемый напор, Па ;
мв - КПД вентилятора ;
мп - КПД передачи ;
Вт.
Таблица В.3 - Сведения о системе вентиляции
|
Параметр
|
Значение
|
|
Строительный объем помещения, м3
|
140
|
|
ПДК воздуха рабочей зоны наиболее опасного вещества, мг/м3
|
0,5
|
|
Температура воздуха рабочей зоны, tв, єС
|
20
|
|
Температура наружного воздуха, tн, єС
|
-26
|
|
Количество удаляемого воздуха из помещения, LA, м3/ч
|
700
|
|
Кратность вентиляции, KA, 1/ч
|
5
|
|
Тип постоянно действующей вентиляции
|
вытяжная
|
|
Производительность вентилятора, Q, м3/ч
|
770
|
|
Тип вентилятора, основные характеристики :
|
Вентилятор канальный типа КВП 40-20
|
|
Частота вращения, об/мин
|
3000
|
|
Производительность, м3/ч
|
950
|
|
Полное давление, Па
|
140
|
|
Масса без двигателя, кг
|
≤ 15,1
|
|
Установочная мощность электродвигателя, N, Вт
|
0,25
|
Освещение производственного помещения
Освещение помещения - важный фактор при работе на производстве, в
лаборатории. Это один из элементов благоприятных условий труда (таб. В.4).
Таблица В.4 - Сведения о совмещенном освещении
|
Параметр
|
Значение
|
|
Совмещенное освещение
|
|
Тип совмещенного освещения
|
комбинированное
|
|
Номер группы по ресурсам светового климата
|
3
|
|
Ориентация световых проёмов
|
СВ
|
|
Коэффициент светового климата, m
|
1,1
|
|
Расстояние до объекта различения, м
|
0,5
|
|
Размер объекта различения, мм
|
0,3
|
|
Разряд и подразряд зрительных работ
|
3В
|
|
Коэффициент естественной освещенности для совмещенного
освещения, ек
|
3,3
|
|
Освещенность, лк (минимальное значение)
|
200
|
|
Рекомендуемый источник света
|
ЛБЦТ, ЛГБУ
|
Категорирование производств, помещений, наружных установок, зон,
взрывозащищенного оборудования
Определение пожароопасной категории помещения осуществляется путем
сравнения максимального значения удельной временной пожарной нагрузки (далее по
тексту - пожарная нагрузка) на любом из участков с величиной удельной пожарной
нагрузки, приведенной в таблице В.5.
Таблица В.5 - Удельные пожарные нагрузки
|
Категория
|
Пожарная нагрузка, МДж×м-2
|
|
В1
|
>2200я
|
|
В2
|
|
В3
|
181-1400
|
|
В4
|
1-180
|
Рассчитаем пожарную нагрузку :
 , (В.5)
, (В.5)
где G - теплота сгорания, МДж S - площадь, 40 м2.
Теплота сгорания различных веществ рассчитывается по формуле :
 , (В.6)
, (В.6)
где  - удельная теплота сгорания, МДж/кг ;
- удельная теплота сгорания, МДж/кг ;
 - масса вещества, кг.
- масса вещества, кг.
Теплота сгорания дерева = 13,8×400 = 5520 МДж ;
бумаги = 13,40×15 = 201 МДж ;
древесно-стружечной плиты = 13,80×40=552 МДж.
Суммарная теплота сгорания  = 6273 МДж.
= 6273 МДж.
Пожарная нагрузка .
По таблице пожарных нагрузок определяем категорию помещения - В4.
Ф 4.2 - здания образовательных учреждений высшего профессионального
образования и дополнительного профессионального образования (повышения
квалификации) специалистов (таблица В.6)
Таблица В.6 - Классификация помещений
|
Наименование блока
|
Классификация помещений
|
|
Лаборатория
|
В4
|
Ф 4.2
|
V
|
Определение размеров санитарно-защитной зоны
Размер санитарно-защитной зоны - 50 м.
Приложение Г
Патентный поиск
Целью патентного поиска являлось выявление аналогов и прототипов
разрабатываемого технологического процесса. В ходе работы были изучены патенты
и авторские свидетельства, посвященные проблеме фракционирования высокоактивных
отходов и разделению редкоземельных и транс плутониевых элементов. Был выбран
один патент - аналог проводимой работы.
Таблица Г.1 - Перечень отобранных в процессе поиска аналогов
|
Страна
|
Индекс МПК
|
№ заявки или охранного документа (а.с. или патента)
|
Название изобретения
|
Дата публикации
|
|
СССР
|
|
1524519
|
Способ извлечения редкоземельных и актинидных элементов
|
17.12.1987
|
Цель изобретения «способ извлечения редкоземельных и актинидных
элементов» - увеличить эффективность извлечения редкоземельных и актинидных
элементов путем повышения степени извлечения и повышение пожаробезопасности
процесса. В качестве экстрагента использовались бидентатные нейтральные
фосфорорганические экстрагенты в органических разбавителях, в частности
метанитробензотрифторид и орто-нитрофенил-1,1,2,2-тетрафторэтиловый эфир.
Однако, существенное ограничение на применение метанитробензотрифторида и
орто-нитрофенил-1,1,2,2-тетрафторэтилового эфира накладывает токсичность этих
разбавителей. Отличием рассматриваемой работы от представленного патента
является использование в качестве растворителя экстракционной смеси полярного
фторированного неароматического соединения формаль-H2. Установлено, что
использование в качестве разбавителя фторированного эфира формаль Н-2 дает
возможность решить проблемы, связанные с ограничениями на использование вышеуказанных
фторированных разбавителей.
Приложение Д
Виды и объем работ, выполненных с использованием ЭВМ
В ходе выполнения дипломной работы использовалась
электронно-вычислительная техника кафедры технологии редких элементов и
наноматериалов на их основе. Общее количество времени, затраченного на
оформление дипломной работы и на реализацию ее цели, составило 700 часов.
При помощи ЭВМ были реализованы :
- расчеты концентрации кислот, РЗЭ, нитрата аммония и коэффициентов
распределения ;
- построение графиков, таблиц и общее оформление дипломной работы.
Для обработки экспериментальных данных и построения графиков применялись
следующие готовые программные средства: Microsoft Word (версия 2010), Microsoft Excel (версия 2010), Microsoft PowerPoint (версия 2010).
В результате применения электронно-вычислительной техники была
значительно увеличена скорость обработки экспериментальных данных, а также
повышена точность ее результатов.
Приложение Е
Стандартизация
Состав работы и содержание основных частей дипломной работы соответствует
СТО СПбГТИ (ТУ) 033-2011 «КС УКДВ. Положение о дипломированном специалисте
(специалисте). Общие требования».
Оформление текстового материала дипломной работы выполнено в соответствии
с требованиями СТП СПбГТИ 006-2009 «КС УКДВ. Подготовка и оформление авторских
текстовых оригиналов для издания» (раздел 6) и ГОСТ 7.32 - 2001.
Применяемые единицы в дипломной работе даны в системе СИ и соответствуют
требованиям ГОСТ 8.417 - 2002 «ГСИ. Единицы величин» и СТП 2.055.005-79 «КС
УКДВ. Единицы физических величин».
Описание источников соответствует требованиям ГОСТ 7.1-2003 и Р 01-2007
«КС УКДВ. Библиографическое описание документа. Примеры оформления».
Сокращение русских слов и словосочетаний в библиографическом описании
соответствует ГОСТ Р 7.0.12-2011 «Система стандартов по информации,
библиотечному и издательскому делу. Библиографическая запись. Сокращение слов и
словосочетаний на русском языке. Общие требования и правила»
При выполнении экспериментальной части дипломной работы соблюдались
требования стандартов на санитарные нормы, регламентированные в следующих
стандартах :
ГОСТ 12.1.005 - 88
«ССБТ. Общие санитарно-гигиенические требования к воздуху рабочей зоны» ;
ГОСТ 12.1.007 - 76 «ССБТ. Вредные вещества. Классификация и общие
требования безопасности» ;
ГОСТ 12.4.021-75
«ССБТ. Системы вентиляционные. Общие требования» ;
СНиП 23-05-95 «Естественное и искусственное
освещение» ;
СанПиН 2.2.1/2.1.1.1200-03 «Санитарно-защитные зоны и санитарная
классификация предприятий, сооружений и иных объектов» ;
СНиП 23-01-99 «Строительная климатология» ;
СП 12.13130.2009 "Определение категорий помещений, зданий и наружных
установок по взрывопожарной и пожарной опасности" ;
СанПиН 2.2.4.548-96 "Гигиенические требования к микроклимату
производственных помещений" ;
СН 2.2.4/2.1.8.566-96 «Производственная вибрация, вибрация в помещениях
жилых и общественных зданий»;
СН 2.2.4/2.1.8.562-96 «Шум на рабочих местах, в помещениях жилых,
общественных зданий и на территории жилой застройки».
При проведении исследований применялись стандарты на реактивы :
Таблица 1
|
Обозначение стандарта
|
Наименование стандарта
|
|
ГОСТ 22300 - 76
|
Эфиры этиловой и бутиловой уксусной кислоты. Технические
условия
|
|
ГОСТ 3118 - 77
|
Кислота соляная. Технические условия
|
|
ГОСТ 61 - 75
|
Кислота уксусная. Технические условия
|
|
ГОСТ 4328 -77
|
Натрия гидроокись. Технические условия
|
|
ГОСТ 4234 -77
|
Калий хлористый. Технические условия
|
|
ГОСТ 2 - 85
|
Селитра аммиачная. Технические условия
|
|
ГОСТ 4461 - 77
|
Кислота азотная. Технические условия
|
|
ГОСТ 6709 - 72
|
Вода дистиллированная. Технические условия
|
Приложение Ж
Таблица Ж.1- Результаты ICP - OES анализа экстрактов 1 серии
|
Sample
|
CeO2
|
Eu2O3
|
Gd2O3
|
La2O3
|
Nd2O3
|
Pr6O11
|
Sm2O3
|
Y2O3
|
TREO
|
|
|
4a-1E
|
2,58
|
0,008
|
0,011
|
1,30
|
0,60
|
0,24
|
0,06
|
0,006
|
4,7974
|
|
|
LnOx/TREO %
|
53,67959728
|
0,160503606
|
0,221995247
|
27,11520824
|
12,56461833
|
4,974048443
|
1,157918873
|
0,126109976
|
100
|
|
|
4a-2E
|
11,80
|
0,035
|
0,048
|
5,93
|
2,75
|
1,09
|
0,25
|
0,028
|
21,924
|
|
|
LnOx/TREO %
|
53,80051542
|
0,158730159
|
0,217797847
|
27,05174694
|
12,53774402
|
4,970010035
|
1,135513592
|
0,127941981
|
100
|
|
|
4a-3E
|
21,52
|
0,056
|
0,112
|
11,41
|
4,97
|
1,97
|
0,43
|
0,051
|
40,5255
|
|
|
LnOx/TREO %
|
53,11125094
|
0,139171633
|
0,276615958
|
28,16300848
|
12,26487027
|
4,871007144
|
1,049215926
|
0,124859656
|
100
|
|
|
4a-4E
|
31,92
|
0,087
|
0,160
|
16,81
|
7,30
|
2,91
|
0,71
|
0,090
|
60,0027
|
|
|
LnOx/TREO %
|
53,20360584
|
0,145660112
|
0,266654667
|
28,02073907
|
12,16678583
|
4,856448127
|
1,190279771
|
0,149826591
|
100
|
|
|
4a-5E
|
43,02
|
0,107
|
0,160
|
22,91
|
9,78
|
3,93
|
0,81
|
0,094
|
80,8237
|
|
|
LnOx/TREO %
|
53,23141603
|
0,132881816
|
0,197961736
|
28,34960538
|
12,10090605
|
4,867384195
|
1,003666004
|
0,116178794
|
100
|
|
|
4a-6E
|
55,82
|
0,131
|
0,202
|
30,01
|
12,58
|
5,07
|
1,02
|
0,120
|
104,9634
|
|
|
LnOx/TREO %
|
53,18387171
|
0,125186494
|
0,192448034
|
28,59396704
|
11,98551114
|
4,83406597
|
0,971005131
|
0,11394448
|
100
|
|
|
4a-7E
|
62,22
|
0,140
|
0,220
|
33,61
|
13,98
|
5,65
|
1,07
|
0,128
|
117,0284
|
|
|
LnOx/TREO %
|
53,16965796
|
0,119970879
|
0,187988557
|
28,72225887
|
11,94616008
|
4,831305905
|
0,913624385
|
0,109033363
|
100
|
|
|
4a-8E
|
76,31
|
0,159
|
0,281
|
41,73
|
16,95
|
6,88
|
1,24
|
0,147
|
143,693
|
|
|
LnOx/TREO %
|
53,10557926
|
0,110652572
|
0,195555803
|
29,04316842
|
11,79667764
|
4,784505856
|
0,861559018
|
0,102301434
|
100
|
|
|
4a-9E
|
91,56
|
0,186
|
0,305
|
50,04
|
20,34
|
8,27
|
1,43
|
0,176
|
172,306
|
|
LnOx/TREO %
|
53,13874734
|
0,107947489
|
0,176720486
|
29,04208211
|
11,80385477
|
4,800326164
|
0,828467958
|
0,101853679
|
100
|
|
4a-10E
|
100,76
|
0,204
|
0,325
|
55,24
|
22,34
|
9,12
|
1,63
|
0,186
|
189,804
|
|
LnOx/TREO %
|
53,08700027
|
0,107479294
|
0,170965838
|
29,10436556
|
11,76937788
|
4,805615266
|
0,857463489
|
0,097732398
|
100
|
|
LnOx/TREO %
|
53,08700027
|
0,107479294
|
0,170965838
|
29,10436556
|
11,76937788
|
4,805615266
|
0,857463489
|
0,097732398
|
100
|
|
4a-11E
|
123,76
|
0,246
|
0,377
|
67,24
|
27,44
|
11,18
|
1,99
|
0,226
|
232,458
|
|
LnOx/TREO %
|
53,24026276
|
0,105825568
|
0,161964742
|
28,92619312
|
11,80374519
|
4,81000869
|
0,85499316
|
0,097006771
|
100
|
|
4a-12E
|
152,76
|
0,287
|
0,422
|
82,44
|
33,94
|
13,78
|
2,41
|
0,263
|
286,301
|
|
LnOx/TREO %
|
53,35686917
|
0,100244149
|
0,147222678
|
28,79530634
|
11,85421986
|
4,813552869
|
0,840898216
|
0,091686721
|
100
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Концентрация редкоземельных элементов дана в г/л по окиси РЗЭ.
|
Sample
|
CeO2
|
Eu2O3
|
Gd2O3
|
La2O3
|
Nd2O3
|
Pr6O11
|
Sm2O3
|
Y2O3
|
TREO
|
|
|
4a-1R
|
0,15
|
0,001
|
0,002
|
0,07
|
0,04
|
0,01
|
0,013
|
0,001
|
0,290025
|
|
|
LnOx/TREO %
|
52,22825618
|
0,362037755
|
0,784415137
|
23,5324541
|
13,47297647
|
4,904749591
|
4,327213171
|
0,387897595
|
100
|
|
|
4a-2R
|
1,30
|
0,005
|
0,005
|
0,60
|
0,32
|
0,12
|
0,037
|
0,003
|
2,384325
|
|
|
LnOx/TREO %
|
54,33298732
|
0,207605926
|
0,200266323
|
25,22936261
|
13,26056641
|
5,09683034
|
1,537122666
|
0,135258406
|
100
|
|
|
4a-3R
|
4,16
|
0,016
|
0,017
|
1,89
|
1,03
|
0,39
|
0,11
|
0,010
|
7,6306
|
|
|
LnOx/TREO %
|
54,54223783
|
0,20968207
|
0,228029251
|
24,79752575
|
13,4550363
|
5,138521217
|
1,499226797
|
0,129740781
|
100
|
|
|
4a-4R
|
7,51
|
0,031
|
0,039
|
3,31
|
1,89
|
0,72
|
0,22
|
0,019
|
13,7346
|
|
|
LnOx/TREO %
|
54,69325645
|
0,226435426
|
0,285410569
|
24,1157369
|
13,73683981
|
5,2138395
|
1,590144598
|
0,138336755
|
100
|
|
|
4a-5R
|
10,48
|
0,047
|
0,058
|
4,44
|
2,67
|
1,01
|
0,32
|
0,029
|
19,056
|
|
|
LnOx/TREO %
|
55,00577246
|
0,248740554
|
0,305940386
|
23,31129303
|
13,99401763
|
5,290197313
|
1,691855584
|
0,152183039
|
100
|
|
|
4a-6R
|
12,48
|
0,060
|
0,080
|
5,12
|
3,26
|
1,22
|
0,41
|
0,037
|
22,6624
|
|
|
LnOx/TREO %
|
55,07757343
|
0,266079497
|
0,354772663
|
22,60219571
|
14,37049915
|
5,37498235
|
1,78886614
|
0,165031065
|
100
|
|
|
4a-7R
|
14,78
|
0,074
|
0,094
|
5,95
|
3,90
|
1,45
|
0,49
|
0,048
|
26,7835
|
|
|
LnOx/TREO %
|
55,1903224
|
0,275916142
|
0,349842254
|
22,2233838
|
14,54888271
|
5,406686953
|
1,827244386
|
0,177721358
|
100
|
|
|
4a-8R
|
15,96
|
0,088
|
0,112
|
6,10
|
4,32
|
1,58
|
0,59
|
0,059
|
28,8126
|
|
|
LnOx/TREO %
|
55,40562115
|
0,305769004
|
0,389412965
|
21,18656421
|
15,00524076
|
5,470523313
|
2,03313828
|
0,203730312
|
100
|
|
|
4a-9R
|
17,16
|
0,096
|
0,124
|
6,55
|
4,65
|
1,70
|
0,64
|
0,065
|
30,9939
|
|
LnOx/TREO %
|
55,37799373
|
0,3107063
|
0,400724013
|
21,14738707
|
15,01392209
|
5,472689787
|
2,067503606
|
0,209073398
|
100
|
|
4a-10R
|
18,16
|
0,117
|
0,165
|
6,59
|
5,09
|
1,83
|
0,75
|
0,079
|
32,7843
|
|
LnOx/TREO %
|
55,4039586
|
0,355658044
|
0,503899732
|
20,11450603
|
15,53609502
|
5,570349222
|
2,274869373
|
0,240663976
|
100
|
|
4a-11R
|
18,26
|
0,125
|
0,180
|
6,48
|
5,18
|
1,85
|
0,79
|
0,086
|
32,9598
|
|
LnOx/TREO %
|
55,4123508
|
0,378036274
|
0,546726618
|
19,67366307
|
15,72643038
|
5,60136894
|
2,399286403
|
0,262137513
|
100
|
|
4a-12R
|
17,56
|
0,140
|
0,202
|
6,04
|
5,12
|
1,80
|
0,85
|
0,101
|
31,824
|
|
LnOx/TREO %
|
55,19042232
|
0,438662645
|
0,635369532
|
18,99321267
|
16,09917044
|
5,644167924
|
2,682880845
|
0,316113625
|
100
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Концентрация редкоземельных элементов дана в г/л по окиси РЗЭ.
Таблица Ж.3- Результаты ICP - OES анализа экстрактов 2 серии
|
Sample
|
CeO2
|
Eu2O3
|
Gd2O3
|
La2O3
|
Nd2O3
|
Pr6O11
|
Sm2O3
|
Y2O3
|
TREO
|
|
5-1Э
|
0,98
|
<0.01
|
0,00
|
0,67
|
0,18
|
0,09
|
0,01
|
<0.01
|
1,94
|
|
LnOx/TREO %
|
50,63245392
|
н/о
|
0,092932005
|
34,73591822
|
9,411946925
|
4,429758893
|
0,578243585
|
н/о
|
100
|
|
5-2Э
|
4,53
|
≤0.01
|
≤0.01
|
2,79
|
0,72
|
0,38
|
0,04
|
<0.01
|
8,49
|
|
LnOx/TREO %
|
53,431309
|
н/о
|
н/о
|
32,843455
|
8,536139822
|
4,496116722
|
0,493806791
|
н/о
|
100
|
|
5-3Э
|
10,8
|
≤0.01
|
0,02
|
6,79
|
1,68
|
0,90
|
0,09
|
<0.01
|
20,3
|
|
LnOx/TREO %
|
53,23835792
|
н/о
|
0,100967813
|
33,42773413
|
8,261137242
|
4,445046421
|
0,451153742
|
н/о
|
100
|
|
5-4Э
|
8,36
|
≤0.01
|
≤0.01
|
5,62
|
1,33
|
0,70
|
0,07
|
<0.01
|
16,1
|
|
LnOx/TREO %
|
51,93098649
|
н/о
|
н/о
|
34,94166035
|
8,246455509
|
4,327323335
|
0,430557799
|
н/о
|
100
|
|
5-5Э
|
11,7
|
≤0.01
|
0,02
|
7,78
|
1,85
|
0,98
|
0,10
|
22,5
|
|
LnOx/TREO %
|
52,16963534
|
н/о
|
0,097496694
|
34,65361962
|
8,224001994
|
4,369543635
|
0,432725055
|
н/о
|
100
|
|
5-6Э
|
19,9
|
0,02
|
0,04
|
12,8
|
2,98
|
1,61
|
0,16
|
<0.01
|
37,6
|
|
LnOx/TREO %
|
53,03143254
|
0,066294283
|
0,096645882
|
34,16951102
|
7,926826021
|
4,274516904
|
0,432110927
|
н/о
|
100
|
|
5-7Э
|
34,1
|
0,04
|
0,06
|
21,6
|
5,30
|
2,89
|
0,29
|
≤0.01
|
64,3
|
|
LnOx/TREO %
|
53,02662949
|
0,068228938
|
0,094650167
|
33,62334518
|
8,233010373
|
4,484615074
|
0,4573981
|
н/о
|
100
|
|
5-8Э
|
78,1
|
0,11
|
0,10
|
51,3
|
13,2
|
6,47
|
0,73
|
<0.01
|
150,0
|
|
LnOx/TREO %
|
52,06444162
|
0,074011052
|
0,068610246
|
34,23177861
|
8,806181723
|
4,310977106
|
0,483605552
|
н/о
|
100
|
|
5-9Э
|
105,2
|
0,14
|
0,16
|
71,8
|
16,1
|
8,64
|
0,87
|
<0.01
|
202,9
|
|
LnOx/TREO %
|
51,84466661
|
0,068511752
|
0,079355339
|
35,40923943
|
7,939131991
|
4,256354219
|
0,42699087
|
н/о
|
100
|
|
5-10Э
|
164,2
|
0,22
|
0,28
|
110,3
|
25,2
|
13,6
|
1,39
|
<0.01
|
315,2
|
|
LnOx/TREO %
|
52,08855483
|
0,070430668
|
0,087245196
|
35,00594536
|
7,99714851
|
4,316416437
|
0,441397243
|
н/о
|
100
|
|
5-11Э
|
185,7
|
0,24
|
0,32
|
122,4
|
27,8
|
15,4
|
1,53
|
<0.01
|
353,4
|
|
LnOx/TREO %
|
52,55245378
|
0,067695525
|
0,090685124
|
34,64001967
|
7,868045081
|
4,358969353
|
0,433279658
|
н/о
|
100
|
|
5-12Э
|
177,7
|
0,24
|
0,37
|
121,4
|
27,2
|
14,8
|
1,51
|
<0.01
|
343,3
|
|
LnOx/TREO %
|
51,77878527
|
0,070866488
|
0,10735581
|
35,37497768
|
7,926354788
|
4,313314655
|
0,440289922
|
н/о
|
100
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Концентрация редкоземельных элементов дана в г/л по окиси РЗЭ.
Таблица Ж.4 - Результаты ICP - OES анализа реэкстрактов 2 серии
|
Sample
|
CeO2
|
Eu2O3
|
Gd2O3
|
La2O3
|
Nd2O3
|
Pr6O11
|
Sm2O3
|
Y2O3
|
TREO
|
|
5-1P
|
12,3
|
0,03
|
0,06
|
6,35
|
2,75
|
1,09
|
0,19
|
≤0.01
|
22,8
|
|
LnOx/TREO %
|
54,01333131
|
0,148589062
|
0,241649273
|
27,85880308
|
12,05480895
|
4,805769733
|
0,843687379
|
н/о
|
100
|
|
5-2P
|
21,8
|
0,06
|
0,10
|
11,3
|
4,88
|
1,93
|
0,34
|
≤0.01
|
40,5
|
|
LnOx/TREO %
|
53,90039197
|
0,150756501
|
0,237997558
|
28,00858076
|
12,0511287
|
4,781699644
|
0,843247839
|
н/о
|
100
|
|
5-3P
|
29,5
|
0,08
|
0,13
|
15,4
|
6,23
|
2,49
|
0,43
|
0,02
|
54,3
|
|
LnOx/TREO %
|
54,33699821
|
0,140125911
|
0,232929405
|
28,4173874
|
11,46454593
|
4,593772959
|
0,782937415
|
0,031302766
|
100
|
|
5-4P
|
32,1
|
0,09
|
0,16
|
16,9
|
7,59
|
2,87
|
0,52
|
≤0.01
|
60,2
|
|
LnOx/TREO %
|
53,3206576
|
0,155279116
|
0,267651069
|
28,02244451
|
12,59196615
|
4,771741359
|
0,855155541
|
н/о
|
100
|
|
5-5P
|
35,1
|
0,11
|
0,17
|
18,0
|
8,55
|
3,14
|
0,59
|
≤0.01
|
65,7
|
|
LnOx/TREO %
|
53,472486
|
0,164800074
|
0,263756239
|
27,37660357
|
13,01075654
|
4,787651489
|
0,904611586
|
н/о
|
100
|
|
5-6P
|
35,1
|
0,12
|
0,18
|
17,2
|
8,92
|
3,15
|
0,65
|
≤0.01
|
65,3
|
|
LnOx/TREO %
|
53,75506865
|
0,185566805
|
0,278924126
|
26,29692066
|
13,64577937
|
4,828256965
|
0,987444971
|
н/о
|
100
|
|
5-7P
|
40,8
|
0,15
|
0,25
|
19,7
|
10,8
|
3,72
|
0,80
|
0,02
|
76,3
|
|
LnOx/TREO %
|
53,52400656
|
0,19961493
|
0,3333471
|
25,80571993
|
14,16800563
|
4,883584179
|
1,053075283
|
0,032646383
|
100
|
|
5-8P
|
44,8
|
0,17
|
0,28
|
19,7
|
12,3
|
4,11
|
0,91
|
0,04
|
82,3
|
|
LnOx/TREO %
|
54,44384051
|
0,208003741
|
0,341611983
|
23,90676574
|
14,94736139
|
4,997919963
|
1,109191336
|
0,04530534
|
100
|
|
5-9P
|
48,0
|
0,20
|
0,33
|
19,8
|
13,9
|
4,42
|
1,04
|
0,05
|
87,7
|
|
LnOx/TREO %
|
54,72845036
|
0,222509278
|
0,37521731
|
22,54437792
|
15,84767488
|
5,042555968
|
1,1865642
|
0,052650083
|
100
|
|
5-10P
|
58,3
|
0,25
|
0,41
|
22,9
|
17,1
|
5,30
|
0,06
|
105,6
|
|
LnOx/TREO %
|
55,20779448
|
0,23404063
|
0,386439179
|
21,65999884
|
16,19229857
|
5,021390225
|
1,241148934
|
0,056889148
|
100
|
|
5-11P
|
70,8
|
0,33
|
0,55
|
25,2
|
23,1
|
6,72
|
1,77
|
0,09
|
128,6
|
|
LnOx/TREO %
|
55,07801853
|
0,259938618
|
0,429472257
|
19,58385713
|
17,96916588
|
5,229723913
|
1,37742193
|
0,072401751
|
0
|
|
5-12P
|
64,4
|
0,29
|
0,47
|
24,2
|
19,7
|
6,02
|
1,52
|
0,07
|
116,7
|
|
LnOx/TREO %
|
55,20962281
|
0,245309448
|
0,40642098
|
20,72382784
|
16,88774511
|
5,16311043
|
1,303632251
|
0,060331127
|
100
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Концентрация редкоземельных элементов дана в г/л по окиси РЗЭ.
Таблица Ж.5- Результаты ICP - OES анализа экстрактов 3 серии
|
Sample
|
CeO2
|
Eu2O3
|
Gd2O3
|
La2O3
|
Nd2O3
|
Pr6O11
|
Sm2O3
|
Y2O3
|
TREO
|
|
6-1E
|
0,4171125
|
<0.01
|
<0.01
|
0,27581
|
0,05823
|
0,02989
|
<0.01
|
<0.01
|
0,78104
|
|
LnOx/TREO %
|
53,40492614
|
н/о
|
н/о
|
35,3136
|
7,45483
|
3,82664
|
н/о
|
н/о
|
100
|
|
6-2E
|
1,84225
|
<0.01
|
<0.01
|
1,28625
|
0,2425
|
0,12675
|
≤0.01
|
<0.01
|
3,49775
|
|
LnOx/TREO %
|
52,6695733
|
н/о
|
н/о
|
36,7736
|
6,93303
|
3,62376
|
н/о
|
н/о
|
100
|
|
6-3E
|
5,81225
|
<0.01
|
≤0.01
|
3,93625
|
0,7665
|
0,40075
|
0,03255
|
<0.01
|
10,9483
|
|
LnOx/TREO %
|
53,08815067
|
н/о
|
н/о
|
35,9531
|
7,00109
|
3,66039
|
0,29731
|
н/о
|
100
|
|
6-4E
|
12,64225
|
≤0.01
|
≤0.01
|
8,11625
|
1,7645
|
0,90275
|
0,07505
|
<0.01
|
23,5008
|
|
LnOx/TREO %
|
53,79497719
|
н/о
|
н/о
|
34,5361
|
7,50826
|
3,84136
|
0,31935
|
н/о
|
100
|
|
6-5E
|
20,8905
|
0,0216
|
0,0227
|
13,333
|
3,0385
|
1,548
|
0,123
|
0,0056
|
38,9829
|
|
LnOx/TREO %
|
53,58888128
|
0,05540891
|
0,05823
|
34,2022
|
7,79444
|
3,97097
|
0,31552
|
0,014365273
|
100
|
|
6-6E
|
28,7905
|
0,034
|
0,0393
|
18,033
|
4,5085
|
2,238
|
0,204
|
0,0088
|
53,8561
|
|
LnOx/TREO %
|
53,45819694
|
0,063131196
|
0,07297
|
33,4837
|
8,37138
|
4,15552
|
0,37879
|
0,016339839
|
100
|
|
6-7E
|
48,82625
|
0,06595
|
0,075
|
28,3825
|
8,52625
|
3,935
|
0,383
|
0,01675
|
90,2107
|
|
LnOx/TREO %
|
54,12467701
|
0,073106627
|
0,08314
|
31,4625
|
9,45148
|
4,36201
|
0,42456
|
0,018567642
|
100
|
|
6-8E
|
64,42625
|
0,09435
|
0,116
|
37,1825
|
11,1463
|
5,145
|
0,555
|
0,02255
|
118,688
|
|
LnOx/TREO %
|
54,28207088
|
0,079494203
|
0,09774
|
31,328
|
9,39123
|
4,3349
|
0,46761
|
0,018999409
|
100
|
|
6-9E
|
83,0828125
|
0,1365625
|
0,17325
|
47,9031
|
15,2328
|
6,87375
|
0,81325
|
0,0314625
|
154,247
|
|
LnOx/TREO %
|
53,86347808
|
0,088534933
|
0,11232
|
31,0561
|
9,8756
|
4,45633
|
0,52724
|
0,020397476
|
100
|
|
6-10E
|
100,2828125
|
0,1705625
|
0,22925
|
58,5031
|
18,5328
|
8,33375
|
0,98125
|
0,0373625
|
187,071
|
|
LnOx/TREO %
|
53,60684056
|
0,091175312
|
0,12255
|
31,2732
|
9,90684
|
4,45486
|
0,52453
|
0,019972371
|
100
|
|
6-11E
|
121,4525
|
0,2125
|
0,266
|
67,665
|
22,5925
|
9,99
|
1,24
|
0,043
|
223,462
|
|
LnOx/TREO %
|
54,35052571
|
0,095094681
|
0,11904
|
30,2804
|
10,1102
|
4,47057
|
0,55491
|
0,019242688
|
100
|
|
6-12E
|
147,565625
|
0,268125
|
0,3235
|
80,5063
|
28,2656
|
12,3875
|
1,5025
|
0,045125
|
270,864
|
|
LnOx/TREO %
|
54,47955018
|
0,0989887
|
0,11943
|
29,722
|
10,4353
|
4,57332
|
0,55471
|
0,016659637
|
100
|
|
|
|
|
|
|
|
|
|
|
|
Концентрация редкоземельных элементов дана в г/л по окиси РЗЭ.
Таблица Ж.6 - Результаты ICP - OES анализа реэкстрактов 3 серии
|
Sample
|
CeO2
|
Eu2O3
|
Gd2O3
|
La2O3
|
Nd2O3
|
Pr6O11
|
Sm2O3
|
Y2O3
|
TREO
|
|
6-1P
|
7,94225
|
0,0232
|
0,0331
|
4,02625
|
1,7945
|
0,70775
|
0,13075
|
≤0.01
|
14,6578
|
|
LnOx/TREO %
|
54,18446152
|
0,158277504
|
0,225818336
|
27,46831039
|
12,2426285
|
4,828487222
|
0,892016537
|
≤0.01
|
100
|
|
6-2P
|
12,04225
|
0,0371
|
0,0532
|
6,01625
|
2,8145
|
1,08975
|
0,20775
|
≤0.01
|
22,2608
|
|
LnOx/TREO %
|
54,09621397
|
0,166660677
|
0,238985122
|
12,64330123
|
4,895376626
|
0,93325487
|
≤0.01
|
100
|
|
6-3P
|
14,64225
|
0,0512
|
0,0758
|
7,05625
|
3,7345
|
1,40975
|
0,28575
|
0,01545
|
27,27095
|
|
LnOx/TREO %
|
53,69174891
|
0,187745568
|
0,277951447
|
25,87460283
|
13,69405906
|
5,169420207
|
1,047818283
|
0,056653692
|
100
|
|
6-4P
|
15,7845
|
0,06
|
0,0894
|
7,0425
|
4,199
|
1,5395
|
0,3395
|
0,0189
|
29,0733
|
|
LnOx/TREO %
|
54,29208243
|
0,206374921
|
0,307498633
|
24,22325639
|
14,44280491
|
5,295236523
|
1,167738096
|
0,0650081
|
100
|
|
6-5P
|
15,9845
|
0,0709
|
0,105
|
6,7825
|
4,639
|
1,6395
|
0,3945
|
0,0224
|
29,6383
|
|
LnOx/TREO %
|
53,93190568
|
0,239217499
|
0,354271331
|
22,884241
|
15,65204482
|
5,531693788
|
1,331048002
|
0,075577884
|
100
|
|
6-6P
|
15,7845
|
0,0805
|
0,123
|
6,2525
|
4,959
|
1,6895
|
0,4415
|
0,026
|
29,3565
|
|
LnOx/TREO %
|
53,76833069
|
0,27421525
|
0,418987277
|
21,29851992
|
16,89234071
|
5,755113859
|
1,503925877
|
0,088566416
|
100
|
|
6-7P
|
15,2845
|
0,0933
|
0,146
|
5,7025
|
5,259
|
1,7095
|
0,5135
|
0,0306
|
28,7389
|
|
LnOx/TREO %
|
53,18401191
|
0,324647081
|
0,508022228
|
19,84244352
|
18,29923901
|
5,94838355
|
1,786776808
|
0,106475892
|
100
|
|
6-8P
|
15,7845
|
0,106
|
0,166
|
5,8225
|
5,679
|
1,8095
|
0,5665
|
0,0376
|
29,9716
|
|
LnOx/TREO %
|
52,66485606
|
0,353668139
|
0,553857652
|
19,42672397
|
18,94793738
|
6,037382055
|
1,890122649
|
0,125452095
|
100
|
|
6-9P
|
14,14525
|
0,10325
|
0,162
|
5,2365
|
5,34925
|
1,689
|
0,539
|
0,03665
|
27,2609
|
|
LnOx/TREO %
|
51,88841894
|
0,378747584
|
0,59425771
|
19,20883023
|
19,62242626
|
6,195686863
|
1,977190775
|
0,134441636
|
100
|
|
6-10P
|
15,9905
|
0,1225
|
0,192
|
5,953
|
5,9085
|
1,868
|
0,628
|
0,0463
|
30,7088
|
|
LnOx/TREO %
|
52,07139322
|
0,398908456
|
0,625227948
|
19,38532277
|
19,24041317
|
6,082946908
|
2,045016412
|
0,150771114
|
100
|
|
6-11P
|
16,6905
|
0,1225
|
0,192
|
6,513
|
5,9385
|
1,898
|
0,63
|
0,0487
|
32,0332
|
|
LnOx/TREO %
|
52,10375485
|
0,382415744
|
0,599378145
|
20,33203052
|
18,53857872
|
5,925102706
|
1,966709539
|
0,152029769
|
100
|
|
6-12P
|
18,1905
|
0,1565
|
0,255
|
6,323
|
6,9885
|
2,168
|
0,795
|
0,0704
|
34,9469
|
|
LnOx/TREO %
|
52,0518272
|
0,447822267
|
0,729678455
|
18,0931642
|
19,99748189
|
6,20369761
|
2,274879889
|
0,201448483
|
100
|
|
|
|
|
|
|
|
|
|
|
|
|
Концентрация редкоземельных элементов дана в г/л по окиси РЗЭ.
Таблица Ж.7 - Результаты ICP - OES анализа экстрактов 4 серии
|
Sample
|
CeO2
|
Eu2O3
|
Gd2O3
|
La2O3
|
Nd2O3
|
Pr6O11
|
Sm2O3
|
Y2O3
|
TREO
|
|
7-1E
|
4,56
|
≤0.01
|
≤0.01
|
2,47
|
0,92
|
0,39
|
0,05
|
<0.01
|
8,43
|
|
LnOx/TREO %
|
54,13410339
|
н/о
|
н/о
|
29,3217746
|
10,96379398
|
4,589495156
|
0,649882001
|
н/о
|
99,65904
|
|
7-2E
|
9,309125
|
0,01955
|
0,02865
|
5,01325
|
1,852375
|
0,7805
|
0,11525
|
0,00585
|
17,12568
|
|
LnOx/TREO %
|
54,35771145
|
0,114156084
|
0,167292676
|
29,27329872
|
10,81636198
|
4,557484595
|
0,672966175
|
0,034159238
|
99,95927
|
|
7-3E
|
16,07
|
0,03
|
0,05
|
8,94
|
3,21
|
1,36
|
0,20
|
≤0.01
|
29,88
|
|
LnOx/TREO %
|
53,79805086
|
0,1131199
|
0,16214968
|
29,92824584
|
10,74806391
|
4,534836244
|
0,671021894
|
н/о
|
99,95549
|
|
7-4E
|
22,17
|
0,05
|
0,07
|
12,32
|
4,38
|
1,87
|
0,27
|
0,02
|
41,15
|
|
LnOx/TREO %
|
53,88773727
|
0,11178642
|
0,165614011
|
29,94539476
|
10,64765649
|
4,532210285
|
0,66707331
|
0,042527442
|
99,68007
|
|
7-5E
|
30,25
|
0,06
|
0,09
|
16,85
|
5,91
|
2,54
|
0,37
|
0,02
|
56,10
|
|
LnOx/TREO %
|
53,92317648
|
0,110343795
|
0,164535255
|
30,02812965
|
10,54059546
|
4,52783908
|
0,664914951
|
0,040465334
|
100
|
|
7-6E
|
37,55
|
0,08
|
0,11
|
20,85
|
7,34
|
3,16
|
0,46
|
0,03
|
69,57
|
|
LnOx/TREO %
|
53,97059246
|
0,109954868
|
0,161698336
|
29,96090494
|
10,55423003
|
4,541926582
|
0,661166528
|
0,03952626
|
100
|
|
7-7E
|
50,72
|
0,10
|
0,14
|
27,97
|
9,90
|
4,23
|
0,62
|
0,02
|
93,69
|
|
LnOx/TREO %
|
54,13397646
|
0,108871013
|
29,85413953
|
10,56288982
|
4,514944948
|
0,657495529
|
0,021720834
|
100
|
|
7-8E
|
69,42
|
0,13
|
0,18
|
38,47
|
13,27
|
5,71
|
0,79
|
0,03
|
127,99
|
|
LnOx/TREO %
|
54,23655317
|
0,103914165
|
0,142784314
|
30,056977
|
10,36504734
|
4,461277324
|
0,613327968
|
0,02011872
|
100
|
|
7-9E
|
86,15
|
0,16
|
0,22
|
47,59
|
16,56
|
7,14
|
1,00
|
0,03
|
158,84
|
|
LnOx/TREO %
|
54,23354526
|
0,102616234
|
0,139248026
|
29,95858916
|
10,42392859
|
4,494968775
|
0,628760513
|
0,018343439
|
100
|
|
7-10E
|
112,75
|
0,20
|
0,28
|
62,23
|
20,72
|
9,17
|
1,27
|
0,06
|
206,66
|
|
LnOx/TREO %
|
54,55755623
|
0,096294407
|
0,13427989
|
30,11014822
|
10,0238123
|
4,437285001
|
0,61212274
|
0,028501209
|
100
|
|
7-11E
|
137,75
|
0,24
|
0,31
|
75,53
|
25,52
|
11,25
|
1,52
|
0,05
|
252,15
|
|
LnOx/TREO %
|
54,6293623
|
0,095578332
|
0,123141378
|
29,95250431
|
10,1190089
|
4,461644138
|
0,600834744
|
0,017925895
|
100
|
|
7-12E
|
168,1140625
|
0,3
|
0,37475
|
92,878125
|
32,3671875
|
14,13125
|
1,881875
|
0,0472125
|
310,0945
|
|
LnOx/TREO %
|
54,21382283
|
0,096744714
|
0,120850272
|
29,95155871
|
10,43784763
|
4,557079119
|
0,606871527
|
0,015225199
|
100
|
Концентрация редкоземельных элементов дана в г/л по окиси РЗЭ.
Таблица Ж.8 - Результаты ICP - OES анализа реэкстрактов 4 серии
|
Sample
|
CeO2
|
Eu2O3
|
Gd2O3
|
La2O3
|
Nd2O3
|
Pr6O11
|
Sm2O3
|
Y2O3
|
TREO
|
|
7-1P
|
5,637125
|
0,019075
|
0,02565
|
2,675625
|
1,363375
|
0,52025
|
0,1085
|
0,00395
|
10,35365
|
|
LnOx/TREO %
|
54,44577516
|
0,184234545
|
0,24773872
|
25,84233579
|
13,1680615
|
5,024798018
|
1,047939615
|
0,038150797
|
99,96088
|
|
7-2P
|
8,772125
|
0,030375
|
0,0413
|
4,125625
|
2,143375
|
0,81575
|
0,176
|
0,00645
|
16,11105
|
|
LnOx/TREO %
|
54,44787894
|
0,188535198
|
0,2563458
|
25,60742472
|
13,30375736
|
5,063295068
|
1,092417937
|
0,040034635
|
99,95966
|
|
7-3P
|
11,147125
|
0,040725
|
0,0558
|
5,135625
|
2,823375
|
1,05375
|
0,234
|
0,00875
|
20,49905
|
|
LnOx/TREO %
|
54,3787395
|
0,198667743
|
0,272207736
|
25,05299026
|
13,77319925
|
5,14048212
|
1,141516314
|
0,042684905
|
99,95780
|
|
7-4P
|
12,697125
|
0,049775
|
0,0687
|
5,810625
|
3,373375
|
1,24875
|
0,2875
|
0,01065
|
23,54635
|
|
LnOx/TREO %
|
53,92396274
|
0,211391574
|
0,291764966
|
24,67739161
|
14,32653044
|
5,303369737
|
1,220996035
|
0,04522994
|
99,95541
|
|
7-5P
|
14,645375
|
0,0597
|
0,080575
|
6,4435
|
3,999625
|
1,45325
|
0,339
|
0,0128
|
27,0339
|
|
LnOx/TREO %
|
54,17411102
|
0,220833842
|
0,298051705
|
23,83488879
|
14,79485017
|
5,37565797
|
1,253981113
|
0,047347959
|
99,95238
|
|
7-6P
|
16,645375
|
0,072
|
0,098875
|
7,2285
|
4,709625
|
1,68325
|
0,417
|
0,016025
|
30,87065
|
|
LnOx/TREO %
|
53,91974254
|
0,233231241
|
0,320288041
|
23,41544477
|
15,25599558
|
5,452590082
|
1,350797602
|
0,051910148
|
100
|
|
7-7P
|
19,240125
|
0,084825
|
0,12325
|
8,167125
|
5,508375
|
1,96175
|
0,4715
|
0,02095
|
35,5779
|
|
LnOx/TREO %
|
54,07886637
|
0,23842048
|
0,34642292
|
22,95561289
|
15,48257486
|
5,513956698
|
1,325260906
|
0,05888487
|
100
|
|
7-8P
|
20,240125
|
0,100525
|
0,14675
|
8,102125
|
6,253375
|
2,14675
|
0,565
|
0,0258
|
37,58045
|
|
LnOx/TREO %
|
53,85812304
|
0,267492805
|
0,39049559
|
21,55941454
|
16,63996839
|
5,71241164
|
1,503441284
|
0,068652717
|
100
|
|
7-9P
|
21,740125
|
0,116625
|
0,17175
|
8,322125
|
7,088375
|
2,37175
|
0,6455
|
0,03215
|
40,4884
|
|
|
LnOx/TREO %
|
53,69470021
|
0,288045465
|
0,424195572
|
20,55434396
|
17,50717489
|
5,857850644
|
1,594283795
|
0,079405459
|
100
|
|
|
7-10P
|
22,781375
|
0,1325
|
0,197375
|
8,4465
|
7,734625
|
2,55925
|
0,757
|
0,039175
|
42,6478
|
|
|
LnOx/TREO %
|
53,41746819
|
0,310684256
|
0,462802302
|
19,80524201
|
18,13604688
|
6,000895709
|
1,775003634
|
0,091857024
|
100
|
|
|
7-11P
|
25,18025
|
0,14825
|
0,229
|
9,60425
|
8,51175
|
2,8035
|
0,8335
|
0,05075
|
47,36125
|
|
|
LnOx/TREO %
|
53,16635435
|
0,31301961
|
0,483517644
|
20,27870886
|
17,97197076
|
5,919396131
|
1,759877537
|
0,107155111
|
100
|
|
|
7-12P
|
33,28025
|
0,17025
|
0,264
|
14,07425
|
10,18675
|
3,5135
|
0,937
|
0,06605
|
62,49205
|
|
|
LnOx/TREO %
|
53,25517406
|
0,422453736
|
22,52166476
|
16,30087347
|
5,622315158
|
1,499390722
|
0,105693444
|
100
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Концентрация редкоземельных элементов дана в г/л по окиси РЗЭ.
Таблица Ж.9- Зависимость коэффициентов распределения индивидуальных РЗЭ в
системе H2O - HNO3 - NH4NO3 - Ln(NO3)3
- ТБФ 100% от концентрации нитрата аммония в водной фазе при их совместной
экстракции
|
C NH4NO3, M, в.ф.
|
С ∑РЗЭ,г/л по окиси, ICP-OES в.ф.
|
C HNO3 в.ф., исход. расчетное
|
Ионная сила
|
Коэффициент распределения
|
|
|
|
|
La
|
Ce
|
Pr
|
Nd
|
Sm
|
Eu
|
Gd
|
Y
|
|
0
|
271
|
8,02
|
16,1
|
0,0898
|
0,141
|
0,200
|
0,283
|
0,605
|
0,667
|
0,901
|
1,78
|
|
0
|
305
|
0,010
|
10,8
|
0,291
|
0,461
|
0,591
|
0,582
|
1,10
|
1,18
|
1,59
|
0,783
|
|
0
|
310
|
5,42
|
15,4
|
0,152
|
0,198
|
0,249
|
0,315
|
0,498
|
0,568
|
0,705
|
1,40
|
|
0
|
343
|
0,010
|
12,5
|
0,199
|
0,362
|
0,407
|
0,724
|
1,01
|
1,18
|
1,29
|
н/о
|
|
0,338
|
353
|
0,010
|
13,4
|
0,206
|
0,381
|
0,437
|
0,831
|
1,16
|
1,4
|
1,72
|
н/о
|
|
0,362
|
252
|
4,95
|
12,7
|
0,127
|
0,183
|
0,249
|
0,334
|
0,550
|
0,615
|
0,738
|
1,12
|
|
0,475
|
296
|
0,010
|
11,3
|
0,314
|
0,519
|
0,680
|
0,667
|
1,36
|
1,41
|
2,18
|
1,02
|
|
0,725
|
207
|
4,24
|
10,7
|
0,136
|
0,202
|
0,279
|
0,373
|
0,598
|
0,666
|
0,711
|
0,665
|
|
0,914
|
223
|
6,81
|
14,8
|
0,112
|
0,16
|
0,222
|
0,307
|
0,593
|
0,673
|
0,842
|
1,32
|
|
0,966
|
159
|
3,77
|
8,87
|
0,175
|
0,252
|
0,332
|
0,428
|
0,646
|
0,715
|
0,777
|
1,10
|
|
1,21
|
128
|
2,83
|
7,54
|
0,211
|
0,292
|
0,376
|
0,471
|
0,72
|
0,756
|
0,803
|
1,00
|
|
1,35
|
315
|
0,010
|
12,3
|
0,207
|
0,355
|
0,390
|
0,679
|
0,942
|
1,11
|
1,49
|
н/о
|
|
1,45
|
93,7
|
2,36
|
6,17
|
0,292
|
0,379
|
0,464
|
0,557
|
0,765
|
0,832
|
0,901
|
1,03
|
|
1,69
|
69,6
|
1,89
|
5,10
|
0,347
|
0,443
|
0,533
|
0,641
|
0,907
|
0,941
|
0,879
|
0,583
|
|
1,81
|
56,1
|
1,73
|
4,51
|
0,383
|
0,484
|
0,572
|
0,676
|
0,909
|
0,964
|
0,873
|
0,564
|
|
1,83
|
187
|
5,61
|
13,8
|
0,119
|
0,186
|
0,262
|
0,372
|
0,747
|
0,839
|
0,977
|
1,45
|
|
1,90
|
229
|
0,010
|
9,77
|
0,344
|
0,545
|
0,689
|
0,698
|
1,43
|
1,55
|
1,93
|
1,02
|
|
1,93
|
41,2
|
1,18
|
3,92
|
0,472
|
0,573
|
0,670
|
0,770
|
1,05
|
1,08
|
1,01
|
0,609
|
|
2,03
|
203
|
0,010
|
8,79
|
0,275
|
0,457
|
0,512
|
0,863
|
1,20
|
1,41
|
2,05
|
н/о
|
|
2,05
|
29,9
|
0,943
|
3,48
|
0,574
|
0,693
|
0,778
|
0,879
|
1,17
|
1,21
|
1,15
|
н/о
|
|
2,18
|
17,1
|
0,629
|
3,02
|
0,823
|
0,942
|
1,05
|
1,157
|
1,53
|
1,55
|
1,44
|
1,103
|
|
2,29
|
8,43
|
0,314
|
2,69
|
1,08
|
1,24
|
1,34
|
1,475
|
1,98
|
н/о
|
н/о
|
н/о
|
|
2,44
|
154
|
4,81
|
11,0
|
0,0957
|
0,149
|
0,215
|
0,307
|
0,580
|
0,662
|
0,818
|
1,02
|
|
2,71
|
150
|
0,010
|
7,52
|
0,383
|
0,574
|
0,636
|
0,932
|
1,26
|
1,54
|
2,73
|
н/о
|
|
2,85
|
188
|
0,010
|
9,66
|
0,492
|
0,696
|
0,844
|
0,851
|
1,66
|
1,78
|
2,64
|
1,37
|
|
3,05
|
119
|
4,01
|
9,68
|
0,137
|
0,214
|
0,308
|
0,446
|
0,893
|
0,983
|
1,25
|
1,46
|
|
3,38
|
64,3
|
0,010
|
5,38
|
0,910
|
1,20
|
1,29
|
2,04
|
2,73
|
3,47
|
4,18
|
н/о
|
|
3,65
|
90,2
|
3,21
|
8,49
|
0,358
|
0,497
|
0,705
|
1,53
|
1,62
|
2,23
|
2,09
|
|
3,80
|
140
|
0,010
|
8,85
|
0,615
|
0,840
|
1,02
|
1,02
|
1,94
|
2,36
|
2,65
|
1,77
|
|
4,06
|
37,6
|
0,01
|
5,14
|
1,34
|
1,76
|
1,97
|
2,10
|
3,98
|
4,87
|
5,02
|
н/о
|
|
4,26
|
53,86
|
2,41
|
7,40
|
0,462
|
0,731
|
1,01
|
1,47
|
2,89
|
3,16
|
4,17
|
3,94
|
|
4,40
|
22,5
|
0,010
|
5,15
|
2,31
|
2,10
|
3,20
|
4,63
|
6,11
|
н/о
|
7,91
|
н/о
|
|
4,57
|
39,0
|
2,00
|
6,79
|
0,509
|
0,765
|
1,06
|
1,53
|
3,21
|
3,28
|
4,63
|
4,00
|
|
4,74
|
16,1
|
0,010
|
5,30
|
3,00
|
3,84
|
4,13
|
5,72
|
7,43
|
н/о
|
н/о
|
н/о
|
|
4,75
|
93,5
|
0,010
|
8,065
|
0,813
|
1,12
|
1,38
|
1,37
|
2,65
|
3,13
|
3,05
|
2,12
|
|
4,87
|
23,5
|
1,60
|
6,43
|
0,868
|
1,25
|
1,71
|
2,38
|
4,52
|
н/о
|
н/о
|
н/о
|
|
5,08
|
20,3
|
0,010
|
5,63
|
2,27
|
2,73
|
2,76
|
3,71
|
4,64
|
н/о
|
6,17
|
н/о
|
|
5,18
|
10,9
|
1,20
|
6,06
|
1,79
|
2,52
|
3,52
|
4,87
|
8,78
|
н/о
|
н/о
|
н/о
|
|
5,42
|
8,49
|
0,01
|
5,67
|
4,07
|
4,81
|
5,07
|
6,732
|
8,14
|
н/о
|
н/о
|
н/о
|
|
5,48
|
3,50
|
0,802
|
5,87
|
4,68
|
6,54
|
8,6
|
11,6
|
н/о
|
н/о
|
н/о
|
н/о
|
|
5,70
|
53,4
|
0,010
|
7,41
|
1,22
|
1,63
|
1,93
|
1,99
|
4,247
|
4,61
|
4,19
|
3,22
|
|
5,75
|
1,94
|
0,010
|
5,83
|
9,43
|
12,6
|
12,8
|
15,1
|
17,2
|
н/о
|
30,6
|
н/о
|
|
5,79
|
0,781
|
0,401
|
5,95
|
17,5
|
22,9
|
28,4
|
37,0
|
н/о
|
н/о
|
н/о
|
н/о
|
|
6,18
|
39,2
|
0,010
|
7,71
|
1,84
|
2,49
|
3,12
|
3,04
|
7,5
|
7,4
|
6,53
|
6,46
|
|
6,65
|
19,2
|
0,010
|
7,30
|
2,95
|
3,80
|
4,57
|
4,56
|
8,35
|
10,0
|
8,65
|
12,4
|
|
7,13
|
10,2
|
0,010
|
7,53
|
3,51
|
6,38
|
5,32
|
5,30
|
9,92
|
14,5
|
10,3
|
8,17
|
|
7,60
|
3,80
|
0,010
|
7,56
|
1,77
|
2,15
|
2,20
|
2,56
|
4,85
|
5,40
|
10,7
|
н/о
|
|
8,08
|
1,10
|
0,010
|
8,08
|
19,4
|
24,8
|
31,1
|
29,3
|
69,7
|
63,5
|
31,5
|
н/о
|
Таблица Ж.10 - Зависимость коэффициентов распределения индивидуальных РЗЭ
в системе H2O -HNO3 -NH4NO3-Ln2(NO3)3
- ТБФ 100% от концентрации ∑РЗЭ по окиси при их совместной экстракции
|
С ∑РЗЭ, г/л по окиси, ICP-OES в.ф.
|
C NH4NO3, M, в.ф.
|
C HNO3 в.ф., М исход. расчетное
|
Ионная сила
|
Коэффициент распределения
|
|
|
|
|
La
|
Ce
|
Pr
|
Nd
|
Sm
|
Eu
|
Gd
|
Y
|
|
0,781
|
5,79
|
0,401
|
5,95
|
17,5
|
22,9
|
28,4
|
37,0
|
н/о
|
н/о
|
н/о
|
н/о
|
|
1,10
|
8,08
|
0,010
|
8,08
|
19,4
|
24,8
|
31,1
|
29,3
|
69,7
|
63,5
|
31,5
|
н/о
|
|
1,94
|
5,75
|
0,010
|
5,83
|
9,43
|
12,6
|
12,8
|
15,1
|
17,2
|
н/о
|
30,6
|
н/о
|
|
3,50
|
5,48
|
0,802
|
5,87
|
4,68
|
6,54
|
8,60
|
11,6
|
н/о
|
н/о
|
н/о
|
н/о
|
|
3,80
|
7,60
|
0,010
|
7,56
|
1,77
|
2,15
|
2,20
|
2,56
|
4,85
|
5,40
|
10,7
|
н/о
|
|
8,43
|
2,29
|
0,314
|
2,69
|
1,08
|
1,24
|
1,34
|
1,48
|
1,98
|
н/о
|
н/о
|
н/о
|
|
8,49
|
5,42
|
0,010
|
5,67
|
4,07
|
4,81
|
5,07
|
6,73
|
8,14
|
н/о
|
н/о
|
н/о
|
|
10,2
|
7,13
|
0,010
|
7,53
|
3,51
|
5,32
|
5,30
|
9,92
|
14,5
|
10,3
|
8,17
|
|
10,9
|
5,18
|
1,20
|
6,06
|
1,79
|
2,52
|
3,52
|
4,87
|
8,78
|
н/о
|
н/о
|
н/о
|
|
16,1
|
4,74
|
0,010
|
5,30
|
3,00
|
3,84
|
4,13
|
5,72
|
7,43
|
н/о
|
н/о
|
н/о
|
|
17,1
|
2,18
|
0,630
|
3,02
|
0,820
|
0,940
|
1,05
|
1,16
|
1,53
|
1,55
|
1,44
|
1,10
|
|
19,2
|
6,65
|
0,010
|
7,30
|
2,95
|
3,80
|
4,57
|
4,56
|
8,35
|
10,00
|
8,65
|
12,40
|
|
20,3
|
5,08
|
0,010
|
5,63
|
2,27
|
2,73
|
2,76
|
3,71
|
4,64
|
н/о
|
6,17
|
н/о
|
|
22,5
|
4,40
|
0,010
|
5,15
|
2,31
|
2,10
|
3,20
|
4,63
|
6,11
|
н/о
|
7,91
|
н/о
|
|
23,5
|
4,87
|
1,60
|
6,43
|
0,87
|
1,25
|
1,71
|
2,38
|
4,52
|
н/о
|
н/о
|
н/о
|
|
29,9
|
2,05
|
0,94
|
3,48
|
0,57
|
0,69
|
0,78
|
0,88
|
1,17
|
1,21
|
1,15
|
н/о
|
|
37,6
|
4,06
|
0,010
|
5,14
|
1,34
|
1,76
|
1,97
|
2,10
|
3,98
|
4,87
|
5,02
|
н/о
|
|
39,0
|
4,57
|
2,00
|
6,79
|
0,51
|
0,77
|
1,06
|
1,53
|
3,21
|
3,28
|
4,63
|
4,00
|
|
39,2
|
6,18
|
0,010
|
7,71
|
1,84
|
2,49
|
3,12
|
3,04
|
7,50
|
7,40
|
6,53
|
6,46
|
|
41,2
|
1,93
|
1,18
|
3,92
|
0,470
|
0,570
|
0,670
|
0,770
|
1,05
|
1,08
|
1,01
|
0,61
|
|
53,4
|
5,70
|
0,010
|
7,41
|
1,22
|
1,63
|
1,93
|
1,99
|
4,25
|
4,61
|
4,19
|
3,22
|
|
53,9
|
4,26
|
2,41
|
7,40
|
0,460
|
0,73
|
1,01
|
1,47
|
2,89
|
3,16
|
4,17
|
3,94
|
|
56,1
|
1,81
|
1,73
|
4,51
|
0,38
|
0,480
|
0,57
|
0,680
|
0,910
|
0,960
|
0,87
|
0,56
|
|
64,3
|
3,38
|
0,010
|
5,38
|
0,91
|
1,20
|
1,29
|
2,04
|
2,73
|
3,47
|
4,18
|
н/о
|
|
69,6
|
1,69
|
1,89
|
5,10
|
0,350
|
0,440
|
0,530
|
0,640
|
0,910
|
0,940
|
0,880
|
0,580
|
|
90,2
|
3,65
|
3,21
|
8,49
|
0,230
|
0,360
|
0,50
|
0,71
|
1,53
|
1,62
|
2,23
|
2,09
|
|
93,5
|
4,75
|
0,010
|
8,07
|
0,810
|
1,12
|
1,38
|
1,37
|
2,65
|
3,13
|
3,05
|
2,12
|
|
93,7
|
1,45
|
2,36
|
6,17
|
0,290
|
0,380
|
0,460
|
0,560
|
0,770
|
0,830
|
0,900
|
1,03
|
|
119
|
3,05
|
4,01
|
9,68
|
0,140
|
0,210
|
0,310
|
0,450
|
0,890
|
0,980
|
1,25
|
1,46
|
|
128
|
1,21
|
2,83
|
7,54
|
0,210
|
0,290
|
0,380
|
0,470
|
0,720
|
0,760
|
0,800
|
1,00
|
|
140
|
3,80
|
0,010
|
8,85
|
0,620
|
0,840
|
1,02
|
1,02
|
1,94
|
2,36
|
2,65
|
1,77
|
|
150
|
2,71
|
0,010
|
7,52
|
0,380
|
0,570
|
0,640
|
0,930
|
1,26
|
1,54
|
2,73
|
н/о
|
|
154
|
2,44
|
4,81
|
11,00
|
0,100
|
0,150
|
0,220
|
0,310
|
0,580
|
0,660
|
0,820
|
1,02
|
|
15
|
0,900
|
3,77
|
8,87
|
0,180
|
0,250
|
0,330
|
0,430
|
0,65
|
0,72
|
0,78
|
1,10
|
|
187
|
1,83
|
5,61
|
13,80
|
0,120
|
0,190
|
0,260
|
0,370
|
0,75
|
0,84
|
0,98
|
1,45
|
|
188
|
2,85
|
0,010
|
9,66
|
0,490
|
0,700
|
0,840
|
0,850
|
1,66
|
1,78
|
2,64
|
1,37
|
|
202
|
2,03
|
0,010
|
8,79
|
0,280
|
0,460
|
0,510
|
0,860
|
1,41
|
2,05
|
н/о
|
|
207
|
0,73
|
4,24
|
10,7
|
0,140
|
0,200
|
0,280
|
0,370
|
0,600
|
0,670
|
0,71
|
0,67
|
|
223
|
0,91
|
6,81
|
14,8
|
0,110
|
0,160
|
0,220
|
0,310
|
0,590
|
0,670
|
0,84
|
1,32
|
|
229
|
1,90
|
0,010
|
9,77
|
0,340
|
0,550
|
0,690
|
0,700
|
1,43
|
1,55
|
1,93
|
1,02
|
|
252
|
0,36
|
4,95
|
12,7
|
0,130
|
0,180
|
0,250
|
0,33
|
0,550
|
0,620
|
0,74
|
1,12
|
|
271
|
0,00
|
8,02
|
16,1
|
0,090
|
0,140
|
0,200
|
0,28
|
0,610
|
0,670
|
0,90
|
1,78
|
|
296
|
0,48
|
0,010
|
11,3
|
0,310
|
0,520
|
0,680
|
0,67
|
1,36
|
1,41
|
2,18
|
1,02
|
|
305
|
0,00
|
0,010
|
10,8
|
0,290
|
0,460
|
0,590
|
0,58
|
1,10
|
1,18
|
1,59
|
0,78
|
|
310
|
0,00
|
5,42
|
15,4
|
0,150
|
0,200
|
0,250
|
0,32
|
0,500
|
0,570
|
0,71
|
1,40
|
|
315
|
1,35
|
0,010
|
12,3
|
0,210
|
0,360
|
0,390
|
0,68
|
0,94
|
1,11
|
1,49
|
н/о
|
|
343
|
0,00
|
0,010
|
12,50
|
0,200
|
0,360
|
0,410
|
0,72
|
1,01
|
1,18
|
1,29
|
н/о
|
|
353
|
0,340
|
0,010
|
13,40
|
0,210
|
0,380
|
0,440
|
0,83
|
1,16
|
1,40
|
1,72
|
н/о
|
Таблица Ж.11 -Зависимость коэффициентов распределения индивидуальных РЗЭ
в системе H2O -HNO3 -NH4NO3 -Ln2(NO3)3
-ТБФ 100% от концентрации HNO3 в водной фазе при их совместной
экстракции
|
C HNO3 в.ф., исход. расчетное
|
C NH4NO3, M, в.ф.
|
С ∑РЗЭ, г/л по окиси, ICP-OES в.ф.
|
Ионная сила
|
Коэффициент распределения
|
|
|
|
|
La
|
Ce
|
Pr
|
Nd
|
Sm
|
Eu
|
Gd
|
Y
|
|
0,010
|
0,00
|
305
|
10,8
|
0,291
|
0,461
|
0,591
|
0,582
|
1,10
|
1,18
|
1,59
|
0,783
|
|
0,010
|
0,00
|
343
|
12,5
|
0,199
|
0,362
|
0,407
|
0,724
|
1,01
|
1,18
|
1,29
|
н/о
|
|
0,010
|
0,338
|
353
|
13,4
|
0,206
|
0,381
|
0,437
|
0,831
|
1,16
|
1,40
|
1,72
|
н/о
|
|
0,010
|
0,475
|
296
|
11,3
|
0,314
|
0,519
|
0,680
|
0,667
|
1,36
|
1,41
|
2,18
|
1,02
|
|
0,010
|
1,35
|
315
|
12,3
|
0,207
|
0,355
|
0,390
|
0,679
|
0,942
|
1,11
|
1,49
|
н/о
|
|
0,010
|
1,90
|
229
|
9,77
|
0,344
|
0,545
|
0,689
|
0,698
|
1,43
|
1,55
|
1,93
|
1,02
|
|
0,010
|
2,03
|
202,9
|
8,79
|
0,275
|
0,457
|
0,512
|
0,863
|
1,20
|
1,41
|
2,05
|
н/о
|
|
0,010
|
2,71
|
150
|
7,52
|
0,383
|
0,574
|
0,636
|
0,932
|
1,26
|
1,54
|
2,73
|
н/о
|
|
0,010
|
2,85
|
188
|
9,66
|
0,492
|
0,696
|
0,844
|
0,851
|
1,66
|
1,78
|
2,64
|
1,37
|
|
0,010
|
3,38
|
64,3
|
5,38
|
0,91
|
1,20
|
1,29
|
2,04
|
2,73
|
3,47
|
4,18
|
н/о
|
|
0,010
|
3,8
|
140
|
8,85
|
0,615
|
0,84
|
1,02
|
1,02
|
1,94
|
2,36
|
2,65
|
1,77
|
|
0,010
|
4,06
|
37,6
|
5,14
|
1,34
|
1,76
|
1,97
|
2,10
|
3,98
|
4,87
|
5,02
|
н/о
|
|
0,010
|
4,4
|
22,5
|
5,15
|
2,31
|
2,10
|
3,20
|
4,63
|
6,11
|
н/о
|
7,91
|
н/о
|
|
0,010
|
4,74
|
16,1
|
5,30
|
3,00
|
3,84
|
4,13
|
5,72
|
7,43
|
н/о
|
н/о
|
н/о
|
|
0,010
|
4,75
|
93,5
|
8,065
|
0,813
|
1,12
|
1,38
|
1,37
|
2,65
|
3,13
|
3,05
|
2,12
|
|
0,010
|
5,08
|
20,3
|
5,63
|
2,27
|
2,73
|
2,76
|
3,71
|
4,64
|
н/о
|
6,17
|
н/о
|
|
0,010
|
5,415
|
8,49
|
5,67
|
4,07
|
4,81
|
5,07
|
6,732
|
8,14
|
н/о
|
н/о
|
|
0,010
|
5,70
|
53,4
|
7,41
|
1,22
|
1,63
|
1,93
|
1,99
|
4,247
|
4,61
|
4,19
|
3,22
|
|
0,010
|
5,75
|
1,94
|
5,83
|
9,43
|
12,6
|
12,8
|
15,1
|
17,2
|
н/о
|
30,6
|
н/о
|
|
0,010
|
6,18
|
39,2
|
7,71
|
1,84
|
2,49
|
3,12
|
3,04
|
7,50
|
7,4
|
6,53
|
6,46
|
|
0,010
|
6,65
|
19,2
|
7,30
|
2,95
|
3,80
|
4,57
|
4,56
|
8,35
|
10,0
|
8,65
|
12,4
|
|
0,010
|
7,13
|
10,2
|
7,53
|
3,51
|
6,38
|
5,32
|
5,3
|
9,92
|
14,5
|
10,3
|
8,17
|
|
0,010
|
7,60
|
3,80
|
7,56
|
1,77
|
2,15
|
2,2
|
2,56
|
4,85
|
5,4
|
10,7
|
-3,23
|
|
0,010
|
8,08
|
1,10
|
8,08
|
19,4
|
24,8
|
31,1
|
29,3
|
69,7
|
63,5
|
31,5
|
-243
|
|
0,314
|
2,29
|
8,43
|
2,69
|
1,08
|
1,24
|
1,34
|
1,475
|
1,98
|
н/о
|
н/о
|
н/о
|
|
0,401
|
5,79
|
0,781
|
5,95
|
17,5
|
22,9
|
28,4
|
37,0
|
н/о
|
н/о
|
н/о
|
н/о
|
|
0,629
|
2,18
|
17,1
|
3,02
|
0,823
|
0,942
|
1,05
|
1,16
|
1,53
|
1,55
|
1,44
|
1,103
|
|
0,802
|
5,48
|
3,50
|
5,87
|
4,68
|
6,54
|
8,6
|
11,6
|
н/о
|
н/о
|
н/о
|
н/о
|
|
0,943
|
2,05
|
29,9
|
3,48
|
0,574
|
0,693
|
0,778
|
0,879
|
1,17
|
1,21
|
1,15
|
н/о
|
|
1,18
|
1,93
|
41,2
|
3,92
|
0,472
|
0,573
|
0,67
|
0,77
|
1,05
|
1,08
|
1,01
|
0,609
|
|
1,20
|
5,18
|
10,9
|
6,06
|
1,79
|
2,52
|
3,52
|
4,87
|
8,78
|
н/о
|
н/о
|
н/о
|
|
1,60
|
4,87
|
23,5
|
6,43
|
0,868
|
1,25
|
1,71
|
2,38
|
4,52
|
н/о
|
н/о
|
н/о
|
|
1,73
|
1,81
|
56,1
|
4,51
|
0,383
|
0,484
|
0,572
|
0,676
|
0,909
|
0,964
|
0,873
|
0,564
|
|
1,89
|
1,69
|
69,6
|
5,10
|
0,347
|
0,443
|
0,533
|
0,641
|
0,907
|
0,941
|
0,879
|
0,583
|
|
2,00
|
4,57
|
39,0
|
6,79
|
0,509
|
0,765
|
1,06
|
1,53
|
3,21
|
3,28
|
4,63
|
4,00
|
|
2,36
|
1,45
|
93,7
|
6,17
|
0,292
|
0,379
|
0,464
|
0,557
|
0,765
|
0,832
|
0,901
|
1,03
|
|
2,41
|
4,26
|
53,9
|
7,40
|
0,462
|
0,731
|
1,01
|
1,47
|
2,89
|
3,16
|
4,17
|
3,94
|
|
2,83
|
1,21
|
128
|
7,54
|
0,211
|
0,292
|
0,376
|
0,471
|
0,72
|
0,756
|
0,803
|
1,00
|
|
3,21
|
3,65
|
90,2
|
8,49
|
0,23
|
0,358
|
0,497
|
0,705
|
1,53
|
1,62
|
2,23
|
2,09
|
|
3,77
|
0,966
|
159
|
8,87
|
0,175
|
0,252
|
0,332
|
0,428
|
0,646
|
0,715
|
0,777
|
1,10
|
|
4,01
|
3,05
|
119
|
9,68
|
0,137
|
0,214
|
0,308
|
0,446
|
0,893
|
0,983
|
1,25
|
1,46
|
|
4,24
|
0,725
|
207
|
10,7
|
0,136
|
0,202
|
0,279
|
0,373
|
0,598
|
0,666
|
0,711
|
0,665
|
|
4,81
|
2,44
|
154
|
11
|
0,0957
|
0,149
|
0,215
|
0,307
|
0,58
|
0,662
|
0,818
|
1,02
|
|
4,95
|
0,362
|
252
|
12,7
|
0,127
|
0,183
|
0,249
|
0,334
|
0,55
|
0,615
|
0,738
|
1,12
|
|
5,42
|
0,00
|
310
|
15,4
|
0,152
|
0,198
|
0,249
|
0,315
|
0,498
|
0,568
|
0,705
|
1,40
|
|
5,61
|
1,83
|
187
|
13,8
|
0,119
|
0,186
|
0,262
|
0,372
|
0,747
|
0,839
|
0,977
|
1,45
|
0,914
|
223
|
14,8
|
0,112
|
0,16
|
0,222
|
0,307
|
0,593
|
0,673
|
0,842
|
1,32
|
|
8,02
|
0,00
|
271
|
16,1
|
0,0898
|
0,141
|
0,2
|
0,283
|
0,605
|
0,667
|
0,901
|
1,78
|
Таблица Ж.12 - Зависимость коэффициентов распределения индивидуальных РЗЭ
в системе H2O - HNO3 - NH4NO3 -
Ln(NO3)3 - ТБФ 100% от равновесной ионной силы при их
совместной экстракции
|
Ионная сила
|
C NH4NO3, M, в.ф.
|
С ∑РЗЭ, г/л по окиси, ICP-OES в.ф.
|
C HNO3 в.ф., исход. расчетное
|
Коэффициент распределения
|
|
|
|
|
La
|
Ce
|
Pr
|
Nd
|
Sm
|
Eu
|
Gd
|
Y
|
|
2,69
|
2,29
|
8,43
|
0,314
|
1,08
|
1,24
|
1,34
|
1,475
|
1,98
|
н/о
|
н/о
|
н/о
|
|
3,02
|
2,18
|
17,1
|
0,629
|
0,823
|
0,942
|
1,05
|
1,157
|
1,53
|
1,55
|
1,44
|
1,103
|
|
3,48
|
2,05
|
29,9
|
0,943
|
0,574
|
0,693
|
0,778
|
0,879
|
1,17
|
1,21
|
1,15
|
н/о
|
|
3,92
|
1,93
|
41,2
|
1,18
|
0,472
|
0,573
|
0,67
|
0,77
|
1,05
|
1,08
|
1,01
|
0,609
|
|
4,51
|
1,81
|
56,1
|
1,73
|
0,383
|
0,484
|
0,572
|
0,676
|
0,909
|
0,964
|
0,873
|
0,564
|
|
5,1
|
1,69
|
69,6
|
1,89
|
0,347
|
0,443
|
0,533
|
0,641
|
0,907
|
0,941
|
0,879
|
0,583
|
|
5,14
|
4,06
|
37,6
|
0,01
|
1,34
|
1,76
|
1,97
|
2,1
|
3,98
|
4,87
|
5,02
|
н/о
|
|
5,15
|
4,4
|
22,5
|
0,01
|
2,31
|
2,1
|
3,2
|
4,63
|
6,11
|
н/о
|
7,91
|
н/о
|
|
5,3
|
4,74
|
16,1
|
0,01
|
3
|
3,84
|
4,13
|
5,72
|
7,43
|
н/о
|
н/о
|
н/о
|
|
5,38
|
3,38
|
64,3
|
0,01
|
0,91
|
1,2
|
1,29
|
2,04
|
2,73
|
3,47
|
4,18
|
н/о
|
|
5,63
|
5,08
|
20,3
|
0,01
|
2,27
|
2,73
|
2,76
|
3,71
|
4,64
|
н/о
|
6,17
|
н/о
|
|
5,67
|
5,415
|
8,49
|
0,01
|
4,07
|
4,81
|
5,07
|
6,732
|
8,14
|
н/о
|
н/о
|
н/о
|
|
5,83
|
5,75
|
1,94
|
0,01
|
9,43
|
12,6
|
12,8
|
15,1
|
17,2
|
н/о
|
30,6
|
н/о
|
|
5,87
|
5,48
|
3,5
|
0,802
|
4,68
|
6,54
|
8,6
|
11,6
|
н/о
|
н/о
|
н/о
|
н/о
|
|
5,95
|
5,79
|
0,781
|
0,401
|
17,5
|
22,9
|
28,4
|
37
|
н/о
|
н/о
|
н/о
|
н/о
|
|
6,06
|
5,18
|
10,9
|
1,2
|
1,79
|
2,52
|
3,52
|
4,87
|
8,78
|
н/о
|
н/о
|
н/о
|
|
6,17
|
1,45
|
93,7
|
2,36
|
0,292
|
0,379
|
0,464
|
0,557
|
0,765
|
0,832
|
0,901
|
1,03
|
|
6,43
|
4,87
|
23,5
|
1,6
|
0,868
|
1,25
|
1,71
|
2,38
|
4,52
|
н/о
|
н/о
|
н/о
|
|
6,79
|
4,57
|
39
|
2
|
0,509
|
0,765
|
1,06
|
1,53
|
3,21
|
3,28
|
4,63
|
4
|
|
7,3
|
6,65
|
19,2
|
0,01
|
2,95
|
3,8
|
4,57
|
4,56
|
8,35
|
10
|
8,65
|
12,4
|
|
7,4
|
4,26
|
53,86
|
2,41
|
0,462
|
0,731
|
1,01
|
1,47
|
2,89
|
3,16
|
4,17
|
3,94
|
|
7,41
|
5,7
|
53,4
|
0,01
|
1,22
|
1,63
|
1,93
|
1,99
|
4,247
|
4,61
|
4,19
|
3,22
|
|
7,52
|
2,71
|
150
|
0,01
|
0,383
|
0,574
|
0,636
|
0,932
|
1,26
|
1,54
|
2,73
|
н/о
|
|
7,53
|
7,13
|
10,2
|
0,01
|
3,51
|
6,38
|
5,32
|
5,3
|
9,92
|
14,5
|
10,3
|
8,17
|
|
7,54
|
1,21
|
128
|
2,83
|
0,211
|
0,292
|
0,376
|
0,471
|
0,72
|
0,756
|
0,803
|
1
|
|
7,56
|
7,6
|
3,8
|
0,01
|
1,77
|
2,15
|
2,2
|
2,56
|
4,85
|
5,4
|
10,7
|
-3,23
|
|
7,71
|
39,2
|
0,01
|
1,84
|
2,49
|
3,12
|
3,04
|
7,5
|
7,4
|
6,53
|
6,46
|
|
8,065
|
4,75
|
93,5
|
0,01
|
0,813
|
1,12
|
1,38
|
1,37
|
2,65
|
3,13
|
3,05
|
2,12
|
|
8,08
|
8,08
|
1,1
|
0,01
|
19,4
|
24,8
|
31,1
|
29,3
|
69,7
|
63,5
|
31,5
|
-243
|
|
8,49
|
3,65
|
90,2
|
3,21
|
0,23
|
0,358
|
0,497
|
0,705
|
1,53
|
1,62
|
2,23
|
2,09
|
|
8,79
|
2,03
|
202,9
|
0,01
|
0,275
|
0,457
|
0,512
|
0,863
|
1,2
|
1,41
|
2,05
|
н/о
|
|
8,85
|
3,8
|
140
|
0,01
|
0,615
|
0,84
|
1,02
|
1,02
|
1,94
|
2,36
|
2,65
|
1,77
|
|
8,87
|
0,966
|
159
|
3,77
|
0,175
|
0,252
|
0,332
|
0,428
|
0,646
|
0,715
|
0,777
|
1,1
|
|
9,66
|
2,85
|
188
|
0,01
|
0,492
|
0,696
|
0,844
|
0,851
|
1,66
|
1,78
|
2,64
|
1,37
|
|
9,68
|
3,05
|
119
|
4,01
|
0,137
|
0,214
|
0,308
|
0,446
|
0,893
|
0,983
|
1,25
|
1,46
|
|
9,77
|
1,9
|
229
|
0,01
|
0,344
|
0,545
|
0,689
|
0,698
|
1,43
|
1,55
|
1,93
|
1,02
|
|
10,7
|
0,725
|
207
|
4,24
|
0,136
|
0,202
|
0,279
|
0,373
|
0,598
|
0,666
|
0,711
|
0,665
|
|
10,8
|
0
|
305
|
0,01
|
0,291
|
0,461
|
0,591
|
0,582
|
1,1
|
1,18
|
1,59
|
0,783
|
|
11
|
2,44
|
154
|
4,81
|
0,0957
|
0,149
|
0,215
|
0,307
|
0,58
|
0,662
|
0,818
|
1,02
|
|
11,3
|
0,475
|
296
|
0,01
|
0,314
|
0,519
|
0,68
|
0,667
|
1,36
|
1,41
|
2,18
|
1,02
|
|
12,3
|
1,35
|
315,2
|
0,01
|
0,207
|
0,355
|
0,39
|
0,679
|
0,942
|
1,11
|
1,49
|
н/о
|
|
12,5
|
0
|
343,3
|
0,01
|
0,199
|
0,362
|
0,407
|
0,724
|
1,01
|
1,18
|
1,29
|
н/о
|
|
12,7
|
0,362
|
252
|
4,95
|
0,127
|
0,183
|
0,249
|
0,334
|
0,55
|
0,615
|
0,738
|
1,12
|
|
13,4
|
0,338
|
353,4
|
0,01
|
0,206
|
0,381
|
0,437
|
0,831
|
1,16
|
1,4
|
1,72
|
н/о
|
|
13,8
|
1,83
|
187
|
5,61
|
0,119
|
0,186
|
0,262
|
0,372
|
0,747
|
0,839
|
0,977
|
1,45
|
|
14,8
|
0,914
|
223
|
6,81
|
0,112
|
0,16
|
0,222
|
0,307
|
0,593
|
0,673
|
0,842
|
1,32
|
|
15,4
|
0
|
310
|
5,42
|
0,152
|
0,198
|
0,249
|
0,315
|
0,498
|
0,568
|
0,705
|
1,4
|
|
16,1
|
0
|
271
|
8,02
|
0,0898
|
0,141
|
0,2
|
0,283
|
0,605
|
0,667
|
0,901
|
1,78
|
Таблица Ж.13 - Зависимость факторов разделения пар РЗЭ в системе H2O
- HNO3 - NH4NO3 - Ln(NO3)3
- ТБФ 100% от концентрации нитрата аммония в водной фазе при их совместной
экстракции
|
C NH4NO3, М в.ф.
|
С ∑РЗЭ, г/л по окиси ICP-OES в.ф.
|
C HNO3 в.ф., исход. расчетное
|
Ионная сила
|
Фактор разделения в
|
|
|
|
|
Ce/La
|
Pr/Ce
|
Nd/Pr
|
Sm/Nd
|
Eu/Sm
|
Gd/Eu
|
Y/Gd
|
|
0
|
271
|
8,02
|
16,1
|
1,57
|
1,42
|
1,41
|
2,14
|
1,1
|
1,35
|
1,98
|
|
0
|
305
|
0,01
|
10,8
|
1,58
|
1,28
|
0,985
|
1,89
|
1,08
|
1,35
|
0,491
|
|
0
|
310
|
5,42
|
15,4
|
1,31
|
1,26
|
1,27
|
1,58
|
1,14
|
1,24
|
1,99
|
|
0
|
343,3
|
0,01
|
12,5
|
1,82
|
1,12
|
1,78
|
1,39
|
1,17
|
1,09
|
н/о
|
|
0,338
|
353,4
|
0,01
|
13,4
|
1,85
|
1,15
|
1,9
|
1,39
|
1,21
|
1,23
|
н/о
|
|
0,362
|
252
|
4,95
|
12,7
|
1,44
|
1,36
|
1,34
|
1,65
|
1,12
|
1,2
|
1,52
|
|
0,475
|
296
|
0,01
|
11,3
|
1,65
|
1,31
|
0,982
|
2,04
|
1,04
|
0,469
|
|
0,725
|
207
|
4,24
|
10,7
|
1,49
|
1,38
|
1,34
|
1,6
|
1,11
|
1,07
|
0,935
|
|
0,914
|
223
|
6,81
|
14,8
|
1,42
|
1,38
|
1,38
|
1,93
|
1,14
|
1,25
|
1,57
|
|
0,966
|
159
|
3,77
|
8,87
|
1,44
|
1,32
|
1,29
|
1,51
|
1,11
|
1,09
|
1,42
|
|
1,21
|
128
|
2,83
|
7,54
|
1,38
|
1,29
|
1,25
|
1,53
|
1,05
|
1,06
|
1,25
|
|
1,35
|
315,2
|
0,01
|
12,3
|
1,71
|
1,1
|
1,74
|
1,39
|
1,18
|
1,33
|
н/о
|
|
1,45
|
93,7
|
2,36
|
6,17
|
1,3
|
1,22
|
1,2
|
1,38
|
1,09
|
1,08
|
1,14
|
|
1,69
|
69,6
|
1,89
|
5,1
|
1,28
|
1,2
|
1,2
|
1,41
|
1,04
|
0,934
|
0,663
|
|
1,81
|
56,1
|
1,73
|
4,51
|
1,27
|
1,18
|
1,18
|
1,34
|
1,06
|
0,905
|
0,646
|
|
1,83
|
187
|
5,61
|
13,8
|
1,57
|
1,41
|
1,42
|
2,01
|
1,12
|
1,17
|
1,48
|
|
1,9
|
229
|
0,01
|
9,77
|
1,59
|
1,26
|
1,01
|
2,06
|
1,08
|
1,25
|
0,525
|
|
1,93
|
41,2
|
1,18
|
3,92
|
1,21
|
1,17
|
1,1
|
1,36
|
1,03
|
0,932
|
0,604
|
|
2,03
|
202,9
|
0,01
|
8,79
|
1,66
|
1,12
|
1,69
|
1,39
|
1,17
|
1,46
|
н/о
|
|
2,05
|
29,9
|
0,943
|
3,48
|
1,21
|
1,12
|
1,13
|
1,33
|
1,03
|
0,956
|
н/о
|
|
2,18
|
17,1
|
0,629
|
3,02
|
1,15
|
1,11
|
1,1
|
1,32
|
1,02
|
0,928
|
0,765
|
|
2,29
|
8,43
|
0,314
|
2,69
|
1,14
|
1,09
|
1,1
|
1,34
|
н/о
|
н/о
|
н/о
|
|
2,44
|
154
|
4,81
|
11
|
1,56
|
1,44
|
1,43
|
1,88
|
1,14
|
1,24
|
1,25
|
|
2,71
|
150
|
0,01
|
7,52
|
1,5
|
1,11
|
1,46
|
1,35
|
1,23
|
1,77
|
н/о
|
|
2,85
|
188
|
0,01
|
9,66
|
1,42
|
1,21
|
1,01
|
1,95
|
1,07
|
1,49
|
0,52
|
|
3,05
|
119
|
4,01
|
9,68
|
1,57
|
1,44
|
1,45
|
2
|
1,1
|
1,27
|
1,17
|
|
3,38
|
64,3
|
0,01
|
5,38
|
1,32
|
1,08
|
1,58
|
1,34
|
1,27
|
1,2
|
н/о
|
|
3,65
|
90,2
|
3,21
|
8,49
|
1,56
|
1,39
|
1,42
|
2,17
|
1,06
|
1,38
|
0,938
|
|
3,8
|
140
|
0,01
|
8,85
|
1,37
|
1,21
|
1
|
1,9
|
1,22
|
1,12
|
0,667
|
|
4,06
|
37,6
|
0,01
|
5,14
|
1,32
|
1,11
|
1,52
|
1,33
|
1,23
|
1,03
|
н/о
|
|
4,26
|
53,86
|
2,41
|
7,4
|
1,58
|
1,38
|
1,46
|
1,97
|
1,1
|
1,32
|
0,944
|
|
4,4
|
22,5
|
0,01
|
5,15
|
1,3
|
1,07
|
1,44
|
1,32
|
н/о
|
н/о
|
н/о
|
|
4,57
|
39
|
2
|
6,79
|
1,5
|
1,38
|
1,44
|
2,1
|
1,02
|
1,41
|
0,865
|
|
4,74
|
16,1
|
0,01
|
5,3
|
1,28
|
1,07
|
1,39
|
1,3
|
н/о
|
н/о
|
н/о
|
|
4,75
|
93,5
|
0,01
|
8,065
|
1,38
|
1,23
|
0,995
|
1,94
|
1,18
|
0,974
|
0,697
|
|
4,87
|
23,5
|
1,6
|
6,43
|
1,44
|
1,37
|
1,4
|
1,9
|
н/о
|
н/о
|
н/о
|
|
5,08
|
20,3
|
0,01
|
5,63
|
1,2
|
1,01
|
1,34
|
1,25
|
н/о
|
н/о
|
н/о
|
|
5,18
|
10,9
|
1,2
|
6,06
|
1,41
|
1,4
|
1,39
|
1,802
|
н/о
|
н/о
|
н/о
|
|
5,415
|
8,49
|
0,01
|
5,67
|
1,18
|
1,05
|
1,33
|
1,21
|
н/о
|
н/о
|
|
5,48
|
3,5
|
0,802
|
5,87
|
1,4
|
1,32
|
1,35
|
н/о
|
н/о
|
н/о
|
н/о
|
|
5,70
|
53,4
|
0,01
|
7,41
|
1,34
|
1,19
|
1,03
|
2,14
|
1,09
|
0,909
|
0,768
|
|
5,75
|
1,94
|
0,01
|
5,83
|
1,33
|
1,02
|
1,18
|
1,14
|
н/о
|
н/о
|
н/о
|
|
5,79
|
0,781
|
0,401
|
5,95
|
1,3
|
1,24
|
1,30
|
н/о
|
н/о
|
н/о
|
н/о
|
|
6,18
|
39,2
|
0,010
|
7,71
|
1,35
|
1,25
|
0,976
|
2,47
|
0,987
|
0,882
|
0,989
|
|
6,65
|
19,2
|
0,010
|
7,3
|
1,29
|
1,20
|
0,997
|
1,83
|
1,20
|
0,864
|
1,43
|
|
7,13
|
10,2
|
0,010
|
7,53
|
1,82
|
0,834
|
0,996
|
1,87
|
1,46
|
0,706
|
0,797
|
|
7,60
|
3,80
|
0,010
|
7,56
|
1,21
|
1,02
|
1,17
|
1,89
|
1,11
|
1,99
|
н/о
|
|
8,08
|
1,10
|
0,010
|
8,08
|
1,28
|
1,26
|
0,941
|
2,38
|
0,91
|
0,496
|
н/о
|
Таблица Ж.14 - Зависимость факторов разделения пар РЗЭ в системе H2O
- HNO3 - NH4NO3 - Ln(NO3)3
- ТБФ 100% от концентрации С ∑РЗЭ по окиси в водной фазе при
их совместной экстракции
|
С ∑РЗЭ, г/л по окиси ICP-OES в.ф.
|
C NH4NO3, М в.ф.
|
C HNO3 в.ф., исход. расчетное
|
Ионная сила
|
Фактор разделения в
|
|
|
|
|
Ce/La
|
Pr/Ce
|
Nd/Pr
|
Sm/Nd
|
Eu/Sm
|
Gd/Eu
|
Y/Gd
|
|
0,781
|
5,79
|
0,401
|
5,95
|
1,3
|
1,24
|
1,3
|
н/о
|
н/о
|
н/о
|
н/о
|
|
1,1
|
8,08
|
0,01
|
8,08
|
1,28
|
1,26
|
0,941
|
2,38
|
0,91
|
0,496
|
н/о
|
|
1,94
|
5,75
|
0,01
|
5,83
|
1,33
|
1,02
|
1,18
|
1,14
|
н/о
|
н/о
|
н/о
|
|
3,5
|
5,48
|
0,802
|
5,87
|
1,4
|
1,32
|
1,35
|
н/о
|
н/о
|
н/о
|
н/о
|
|
3,8
|
7,6
|
0,01
|
7,56
|
1,21
|
1,02
|
1,17
|
1,89
|
1,11
|
1,99
|
н/о
|
|
8,43
|
2,29
|
0,314
|
2,69
|
1,14
|
1,09
|
1,1
|
1,34
|
н/о
|
н/о
|
н/о
|
|
8,49
|
5,415
|
0,01
|
5,67
|
1,18
|
1,05
|
1,33
|
1,21
|
н/о
|
н/о
|
н/о
|
|
10,2
|
7,13
|
0,01
|
7,53
|
1,82
|
0,834
|
0,996
|
1,87
|
1,46
|
0,706
|
0,797
|
|
10,9
|
5,18
|
1,2
|
6,06
|
1,41
|
1,4
|
1,39
|
1,802
|
н/о
|
н/о
|
н/о
|
|
16,1
|
4,74
|
0,01
|
5,3
|
1,28
|
1,07
|
1,39
|
1,3
|
н/о
|
н/о
|
н/о
|
|
17,1
|
2,18
|
0,629
|
3,02
|
1,15
|
1,11
|
1,1
|
1,32
|
1,02
|
0,928
|
0,765
|
|
19,2
|
6,65
|
0,01
|
7,3
|
1,29
|
1,2
|
0,997
|
1,83
|
1,2
|
0,864
|
1,43
|
|
20,3
|
5,08
|
0,01
|
5,63
|
1,2
|
1,01
|
1,34
|
1,25
|
н/о
|
н/о
|
н/о
|
|
22,5
|
4,4
|
0,01
|
5,15
|
1,3
|
1,07
|
1,44
|
1,32
|
н/о
|
н/о
|
н/о
|
|
23,5
|
4,87
|
1,6
|
6,43
|
1,44
|
1,37
|
1,4
|
1,9
|
н/о
|
н/о
|
н/о
|
|
29,9
|
2,05
|
0,943
|
3,48
|
1,21
|
1,12
|
1,13
|
1,33
|
1,03
|
0,956
|
н/о
|
|
37,6
|
4,06
|
0,01
|
5,14
|
1,32
|
1,11
|
1,52
|
1,33
|
1,23
|
1,03
|
н/о
|
|
39
|
4,57
|
2
|
6,79
|
1,5
|
1,38
|
1,44
|
2,1
|
1,02
|
1,41
|
0,865
|
|
39,2
|
6,18
|
0,01
|
7,71
|
1,35
|
1,25
|
0,976
|
2,47
|
0,987
|
0,882
|
0,989
|
|
41,2
|
1,93
|
1,18
|
3,92
|
1,21
|
1,17
|
1,1
|
1,36
|
1,03
|
0,932
|
0,604
|
|
53,4
|
5,7
|
0,01
|
7,41
|
1,34
|
1,19
|
1,03
|
2,14
|
1,09
|
0,909
|
0,768
|
|
53,86
|
4,26
|
2,41
|
7,4
|
1,58
|
1,46
|
1,97
|
1,1
|
1,32
|
0,944
|
|
56,1
|
1,81
|
1,73
|
4,51
|
1,27
|
1,18
|
1,18
|
1,34
|
1,06
|
0,905
|
0,646
|
|
64,3
|
3,38
|
0,01
|
5,38
|
1,32
|
1,08
|
1,58
|
1,34
|
1,27
|
1,2
|
н/о
|
|
69,6
|
1,69
|
1,89
|
5,1
|
1,28
|
1,2
|
1,2
|
1,41
|
1,04
|
0,934
|
0,663
|
|
90,2
|
3,65
|
3,21
|
8,49
|
1,56
|
1,39
|
1,42
|
2,17
|
1,06
|
1,38
|
0,938
|
|
93,5
|
4,75
|
0,01
|
8,065
|
1,38
|
1,23
|
0,995
|
1,94
|
1,18
|
0,974
|
0,697
|
|
93,7
|
1,45
|
2,36
|
6,17
|
1,3
|
1,22
|
1,2
|
1,38
|
1,09
|
1,08
|
1,14
|
|
119
|
3,05
|
4,01
|
9,68
|
1,57
|
1,44
|
1,45
|
2
|
1,1
|
1,27
|
1,17
|
|
128
|
1,21
|
2,83
|
7,54
|
1,38
|
1,29
|
1,25
|
1,53
|
1,05
|
1,06
|
1,25
|
|
140
|
3,8
|
0,01
|
8,85
|
1,37
|
1,21
|
1
|
1,9
|
1,22
|
1,12
|
0,667
|
|
150
|
2,71
|
0,01
|
7,52
|
1,5
|
1,11
|
1,46
|
1,35
|
1,23
|
1,77
|
н/о
|
|
154
|
2,44
|
4,81
|
11
|
1,56
|
1,44
|
1,43
|
1,88
|
1,14
|
1,24
|
1,25
|
|
159
|
0,966
|
3,77
|
8,87
|
1,44
|
1,32
|
1,29
|
1,51
|
1,11
|
1,09
|
1,42
|
|
187
|
1,83
|
5,61
|
13,8
|
1,57
|
1,41
|
1,42
|
2,01
|
1,12
|
1,17
|
1,48
|
|
188
|
2,85
|
0,01
|
9,66
|
1,42
|
1,21
|
1,01
|
1,95
|
1,07
|
1,49
|
0,52
|
|
202,9
|
2,03
|
0,01
|
8,79
|
1,66
|
1,12
|
1,69
|
1,39
|
1,17
|
1,46
|
н/о
|
|
207
|
0,725
|
4,24
|
10,7
|
1,49
|
1,38
|
1,34
|
1,6
|
1,11
|
1,07
|
0,935
|
|
223
|
0,914
|
6,81
|
14,8
|
1,42
|
1,38
|
1,38
|
1,93
|
1,14
|
1,25
|
1,57
|
|
229
|
1,9
|
0,01
|
9,77
|
1,59
|
1,26
|
1,01
|
2,06
|
1,08
|
1,25
|
0,525
|
|
252
|
0,362
|
4,95
|
12,7
|
1,44
|
1,36
|
1,34
|
1,65
|
1,12
|
1,2
|
1,52
|
|
271
|
0
|
8,02
|
16,1
|
1,57
|
1,42
|
1,41
|
2,14
|
1,1
|
1,35
|
1,98
|
|
296
|
0,475
|
0,01
|
11,3
|
1,65
|
1,31
|
0,982
|
2,04
|
1,04
|
1,54
|
0,469
|
|
305
|
0
|
0,01
|
10,8
|
1,58
|
1,28
|
0,985
|
1,89
|
1,08
|
1,35
|
0,491
|
|
310
|
0
|
5,42
|
15,4
|
1,31
|
1,26
|
1,27
|
1,58
|
1,14
|
1,24
|
1,99
|
|
315,2
|
1,35
|
0,01
|
12,3
|
1,71
|
1,1
|
1,74
|
1,39
|
1,18
|
1,33
|
н/о
|
|
343,3
|
0
|
0,01
|
12,5
|
1,82
|
1,12
|
1,78
|
1,39
|
1,17
|
1,09
|
н/о
|
|
353,4
|
0,338
|
0,01
|
13,4
|
1,85
|
1,15
|
1,9
|
1,39
|
1,21
|
1,23
|
н/о
|
Таблица Ж.15 - Зависимость факторов разделения пар РЗЭ в системе H2O
- HNO3 - NH4NO3 - Ln(NO3)3
-ТБФ 100% от ионной силы при их совместной экстракции
|
Ионная сила.
|
C NH4NO3, М в.ф.
|
С ∑РЗЭ, г/л по окиси ICP-OES в.ф
|
C HNO3 в.ф., исход. расчетное
|
Фактор разделения в
|
|
|
|
|
Ce/La
|
Pr/Ce
|
Nd/Pr
|
Sm/Nd
|
Eu/Sm
|
Gd/Eu
|
Y/Gd
|
|
2,69
|
2,29
|
8,43
|
0,314
|
1,14
|
1,09
|
1,1
|
1,34
|
н/о
|
н/о
|
н/о
|
|
3,02
|
2,18
|
17,1
|
0,629
|
1,15
|
1,11
|
1,1
|
1,32
|
1,02
|
0,928
|
0,765
|
|
3,48
|
2,05
|
29,9
|
0,943
|
1,21
|
1,12
|
1,13
|
1,33
|
1,03
|
0,956
|
н/о
|
|
3,92
|
1,93
|
41,2
|
1,18
|
1,21
|
1,17
|
1,1
|
1,36
|
1,03
|
0,932
|
0,604
|
|
4,51
|
1,81
|
1,73
|
1,27
|
1,18
|
1,18
|
1,34
|
1,06
|
0,905
|
0,646
|
|
5,10
|
1,69
|
69,6
|
1,89
|
1,28
|
1,20
|
1,20
|
1,41
|
1,04
|
0,934
|
0,663
|
|
5,14
|
4,06
|
37,6
|
0,01
|
1,32
|
1,11
|
1,52
|
1,33
|
1,23
|
1,03
|
н/о
|
|
5,15
|
4,4
|
22,5
|
0,01
|
1,30
|
1,07
|
1,44
|
1,32
|
н/о
|
н/о
|
н/о
|
|
5,3
|
4,74
|
16,1
|
0,01
|
1,28
|
1,07
|
1,39
|
1,30
|
н/о
|
н/о
|
н/о
|
|
5,38
|
3,38
|
64,3
|
0,01
|
1,32
|
1,08
|
1,58
|
1,34
|
1,27
|
1,20
|
н/о
|
|
5,63
|
5,08
|
20,3
|
0,01
|
1,20
|
1,01
|
1,34
|
1,25
|
н/о
|
н/о
|
н/о
|
|
5,67
|
5,415
|
8,49
|
0,01
|
1,18
|
1,05
|
1,33
|
1,21
|
н/о
|
н/о
|
н/о
|
|
5,83
|
5,75
|
1,94
|
0,01
|
1,33
|
1,02
|
1,18
|
1,14
|
н/о
|
н/о
|
н/о
|
|
5,87
|
5,48
|
3,50
|
0,802
|
1,40
|
1,32
|
1,35
|
н/о
|
н/о
|
н/о
|
н/о
|
|
5,95
|
5,79
|
0,781
|
0,401
|
1,30
|
1,24
|
1,30
|
н/о
|
н/о
|
н/о
|
н/о
|
|
6,06
|
5,18
|
10,9
|
1,20
|
1,41
|
1,40
|
1,39
|
1,802
|
н/о
|
н/о
|
н/о
|
|
6,17
|
1,45
|
93,7
|
2,36
|
1,30
|
1,22
|
1,20
|
1,38
|
1,09
|
1,08
|
1,14
|
|
6,43
|
4,87
|
23,5
|
1,60
|
1,44
|
1,37
|
1,40
|
1,90
|
н/о
|
н/о
|
н/о
|
|
6,79
|
4,57
|
39,0
|
2,00
|
1,50
|
1,38
|
1,44
|
2,10
|
1,02
|
1,41
|
0,865
|
|
7,3
|
6,65
|
19,2
|
0,01
|
1,29
|
1,2
|
0,997
|
1,83
|
1,20
|
0,864
|
1,43
|
|
7,4
|
4,26
|
53,86
|
2,41
|
1,58
|
1,38
|
1,46
|
1,97
|
1,10
|
1,32
|
0,944
|
|
7,41
|
5,7
|
53,4
|
0,01
|
1,34
|
1,19
|
1,03
|
2,14
|
1,09
|
0,909
|
0,768
|
|
7,52
|
2,71
|
150
|
0,01
|
1,50
|
1,11
|
1,46
|
1,35
|
1,23
|
1,77
|
н/о
|
|
7,53
|
7,13
|
10,2
|
0,01
|
1,82
|
0,834
|
0,996
|
1,87
|
1,46
|
0,706
|
0,797
|
|
7,54
|
1,21
|
128
|
2,83
|
1,38
|
1,29
|
1,25
|
1,53
|
1,05
|
1,06
|
1,25
|
|
7,56
|
7,6
|
3,8
|
0,01
|
1,21
|
1,02
|
1,17
|
1,89
|
1,11
|
1,99
|
н/о
|
|
7,71
|
6,18
|
39,2
|
0,01
|
1,35
|
1,25
|
0,976
|
2,47
|
0,987
|
0,882
|
0,989
|
|
8,065
|
4,75
|
93,5
|
0,01
|
1,38
|
1,23
|
0,995
|
1,94
|
1,18
|
0,974
|
0,697
|
|
8,08
|
8,08
|
1,10
|
0,01
|
1,28
|
1,26
|
0,941
|
2,38
|
0,91
|
0,496
|
н/о
|
|
8,49
|
3,65
|
90,2
|
3,21
|
1,56
|
1,39
|
1,42
|
2,17
|
1,06
|
1,38
|
0,938
|
|
8,79
|
2,03
|
203
|
0,01
|
1,66
|
1,12
|
1,69
|
1,39
|
1,17
|
1,46
|
н/о
|
|
8,85
|
3,8
|
140
|
0,01
|
1,37
|
1,21
|
1,00
|
1,90
|
1,22
|
1,12
|
0,667
|
|
8,87
|
0,966
|
159
|
3,77
|
1,44
|
1,32
|
1,29
|
1,51
|
1,11
|
1,09
|
1,42
|
|
9,66
|
2,85
|
188
|
0,01
|
1,42
|
1,21
|
1,01
|
1,95
|
1,07
|
1,49
|
0,52
|
|
9,68
|
3,05
|
119
|
4,01
|
1,57
|
1,44
|
1,45
|
2,00
|
1,10
|
1,27
|
1,17
|
|
9,77
|
1,9
|
229
|
0,01
|
1,59
|
1,26
|
1,01
|
2,06
|
1,08
|
1,25
|
0,525
|
|
10,7
|
207
|
4,24
|
1,49
|
1,38
|
1,34
|
1,60
|
1,11
|
1,07
|
0,935
|
|
10,8
|
0,00
|
305
|
0,01
|
1,58
|
1,28
|
0,985
|
1,89
|
1,08
|
1,35
|
0,491
|
|
11,0
|
2,44
|
154
|
4,81
|
1,56
|
1,44
|
1,43
|
1,88
|
1,14
|
1,24
|
1,25
|
|
11,3
|
0,475
|
296
|
0,01
|
1,65
|
1,31
|
0,982
|
2,04
|
1,04
|
1,54
|
0,469
|
|
12,3
|
1,35
|
315,2
|
0,01
|
1,71
|
1,10
|
1,74
|
1,39
|
1,18
|
1,33
|
н/о
|
|
12,5
|
0,00
|
343,3
|
0,01
|
1,82
|
1,12
|
1,78
|
1,39
|
1,17
|
1,09
|
н/о
|
|
12,7
|
0,362
|
252
|
4,95
|
1,44
|
1,36
|
1,34
|
1,65
|
1,12
|
1,20
|
1,52
|
|
13,4
|
0,338
|
353,4
|
0,01
|
1,85
|
1,15
|
1,9
|
1,39
|
1,21
|
1,23
|
н/о
|
|
13,8
|
1,83
|
187
|
5,61
|
1,57
|
1,41
|
1,42
|
2,01
|
1,12
|
1,17
|
1,48
|
|
14,8
|
0,914
|
223
|
6,81
|
1,42
|
1,38
|
1,38
|
1,93
|
1,14
|
1,25
|
1,57
|
|
15,4
|
0,00
|
310
|
5,42
|
1,31
|
1,26
|
1,27
|
1,58
|
1,14
|
1,24
|
1,99
|
|
16,1
|
0,00
|
271
|
8,02
|
1,57
|
1,42
|
1,41
|
2,14
|
1,10
|
1,35
|
1,98
|
Таблица Ж.16 - Зависимость факторов разделения пар РЗЭ в системе H2O
- HNO3 - NH4NO3 - Ln(NO3)3
- ТБФ 100% от исходной концентрации азотной кислоты при их совместной
экстракции
|
C HNO3 в.ф., исход. расчетное
|
C NH4NO3, М в.ф.
|
С ∑РЗЭ, г/л по окиси ICP-OES, в.ф.
|
Ионная сила
|
Фактор разделения в
|
|
|
|
|
Ce/La
|
Pr/Ce
|
Nd/Pr
|
Sm/Nd
|
Eu/Sm
|
Gd/Eu
|
Y/Gd
|
|
0,01
|
0
|
305
|
10,8
|
1,58
|
1,28
|
0,985
|
1,89
|
1,08
|
1,35
|
0,491
|
|
0,01
|
0
|
343,3
|
12,5
|
1,82
|
1,12
|
1,78
|
1,39
|
1,17
|
1,09
|
н/о
|
|
0,01
|
0,338
|
353,4
|
13,4
|
1,85
|
1,15
|
1,9
|
1,39
|
1,21
|
1,23
|
н/о
|
|
0,01
|
0,475
|
296
|
11,3
|
1,65
|
1,31
|
0,982
|
2,04
|
1,04
|
1,54
|
0,469
|
|
0,01
|
1,35
|
315,2
|
12,3
|
1,71
|
1,1
|
1,74
|
1,39
|
1,18
|
1,33
|
н/о
|
|
0,01
|
1,9
|
229
|
9,77
|
1,59
|
1,26
|
1,01
|
2,06
|
1,08
|
1,25
|
0,525
|
|
0,01
|
2,03
|
202,9
|
8,79
|
1,66
|
1,12
|
1,69
|
1,39
|
1,17
|
1,46
|
н/о
|
|
0,01
|
2,71
|
150
|
7,52
|
1,5
|
1,11
|
1,46
|
1,35
|
1,23
|
1,77
|
н/о
|
|
0,01
|
2,85
|
188
|
9,66
|
1,42
|
1,21
|
1,01
|
1,95
|
1,07
|
1,49
|
0,52
|
|
0,01
|
3,38
|
64,3
|
5,38
|
1,32
|
1,08
|
1,58
|
1,34
|
1,27
|
1,2
|
н/о
|
|
0,01
|
3,8
|
140
|
8,85
|
1,37
|
1,21
|
1
|
1,9
|
1,22
|
1,12
|
0,667
|
|
0,01
|
4,06
|
37,6
|
5,14
|
1,32
|
1,11
|
1,52
|
1,33
|
1,23
|
1,03
|
н/о
|
|
0,01
|
4,40
|
22,5
|
5,15
|
1,30
|
1,07
|
1,44
|
1,32
|
н/о
|
н/о
|
н/о
|
|
0,01
|
4,74
|
16,1
|
5,3
|
1,28
|
1,07
|
1,39
|
1,30
|
н/о
|
н/о
|
н/о
|
|
0,01
|
4,75
|
93,5
|
8,065
|
1,38
|
1,23
|
0,995
|
1,94
|
1,18
|
0,974
|
0,697
|
|
0,01
|
5,08
|
20,3
|
5,63
|
1,2
|
1,01
|
1,34
|
1,25
|
н/о
|
н/о
|
н/о
|
|
0,01
|
5,415
|
8,49
|
5,67
|
1,18
|
1,05
|
1,33
|
1,21
|
н/о
|
н/о
|
н/о
|
|
0,01
|
5,70
|
53,4
|
7,41
|
1,34
|
1,19
|
1,03
|
2,14
|
1,09
|
0,909
|
0,768
|
|
0,01
|
5,75
|
1,94
|
5,83
|
1,33
|
1,02
|
1,18
|
1,14
|
н/о
|
н/о
|
|
0,01
|
6,18
|
39,2
|
7,71
|
1,35
|
1,25
|
0,976
|
2,47
|
0,987
|
0,882
|
0,989
|
|
0,01
|
6,65
|
19,2
|
7,30
|
1,29
|
1,20
|
0,997
|
1,83
|
1,2
|
0,864
|
1,43
|
|
0,01
|
7,13
|
10,2
|
7,53
|
1,82
|
0,834
|
0,996
|
1,87
|
1,46
|
0,706
|
0,797
|
|
0,01
|
7,60
|
3,80
|
7,56
|
1,21
|
1,02
|
1,17
|
1,89
|
1,11
|
1,99
|
н/о
|
|
0,01
|
8,08
|
1,10
|
8,08
|
1,28
|
1,26
|
0,941
|
2,38
|
0,91
|
0,496
|
н/о
|
|
0,314
|
2,29
|
8,43
|
2,69
|
1,14
|
1,09
|
1,10
|
1,34
|
н/о
|
н/о
|
н/о
|
|
0,401
|
5,79
|
0,781
|
5,95
|
1,3
|
1,24
|
1,30
|
н/о
|
н/о
|
н/о
|
н/о
|
|
0,629
|
2,18
|
17,1
|
3,02
|
1,15
|
1,11
|
1,10
|
1,32
|
1,02
|
0,928
|
0,765
|
|
0,802
|
5,48
|
3,5
|
5,87
|
1,40
|
1,32
|
1,35
|
н/о
|
н/о
|
н/о
|
н/о
|
|
0,943
|
2,05
|
29,9
|
3,48
|
1,21
|
1,12
|
1,13
|
1,33
|
1,03
|
0,956
|
н/о
|
|
1,18
|
1,93
|
41,2
|
3,92
|
1,21
|
1,17
|
1,10
|
1,36
|
1,03
|
0,932
|
0,604
|
|
1,20
|
5,18
|
10,9
|
6,06
|
1,41
|
1,4
|
1,39
|
1,802
|
н/о
|
н/о
|
н/о
|
|
1,60
|
4,87
|
23,5
|
6,43
|
1,44
|
1,37
|
1,40
|
1,90
|
н/о
|
н/о
|
н/о
|
|
1,73
|
1,81
|
56,1
|
4,51
|
1,27
|
1,18
|
1,18
|
1,34
|
1,06
|
0,905
|
0,646
|
|
1,89
|
1,69
|
69,6
|
5,10
|
1,28
|
1,2
|
1,20
|
1,41
|
1,04
|
0,934
|
0,663
|
|
2,00
|
4,57
|
39,0
|
6,79
|
1,5
|
1,38
|
1,44
|
2,10
|
1,02
|
1,41
|
0,865
|
|
2,36
|
1,45
|
93,7
|
6,17
|
1,3
|
1,22
|
1,20
|
1,38
|
1,09
|
1,08
|
1,14
|
|
2,41
|
4,26
|
53,86
|
7,4
|
1,58
|
1,38
|
1,46
|
1,97
|
1,10
|
1,32
|
0,944
|
|
2,83
|
1,21
|
128
|
7,54
|
1,38
|
1,29
|
1,25
|
1,53
|
1,05
|
1,06
|
1,25
|
|
3,21
|
3,65
|
90,2
|
8,49
|
1,56
|
1,39
|
1,42
|
2,17
|
1,06
|
1,38
|
0,938
|
|
3,77
|
0,966
|
159
|
8,87
|
1,44
|
1,32
|
1,29
|
1,51
|
1,11
|
1,09
|
1,42
|
|
4,01
|
3,05
|
119
|
9,68
|
1,57
|
1,44
|
1,45
|
2,00
|
1,10
|
1,27
|
1,17
|
|
4,24
|
0,725
|
207
|
10,7
|
1,49
|
1,38
|
1,34
|
1,6
|
1,11
|
1,07
|
0,935
|
|
4,81
|
2,44
|
154
|
11
|
1,56
|
1,44
|
1,43
|
1,88
|
1,14
|
1,24
|
1,25
|
|
4,95
|
0,362
|
252
|
12,7
|
1,44
|
1,36
|
1,34
|
1,65
|
1,12
|
1,2
|
1,52
|
|
5,42
|
0,00
|
310
|
15,4
|
1,31
|
1,26
|
1,27
|
1,58
|
1,14
|
1,24
|
1,99
|
|
5,61
|
1,83
|
187
|
13,8
|
1,57
|
1,41
|
1,42
|
2,01
|
1,12
|
1,17
|
1,48
|
|
6,81
|
0,914
|
223
|
14,8
|
1,42
|
1,38
|
1,38
|
1,93
|
1,14
|
1,25
|
1,57
|
|
8,02
|
0,00
|
271
|
16,1
|
1,57
|
1,42
|
1,41
|
2,14
|
1,10
|
1,35
|
1,98
|
Таблица Ж.17 - Фактор разделения пары Sm/Nd в системе H2O -
HNO3 - NH4NO3 - Ln(NO3)3
- ТБФ 100% при различных концентрациях нитрата аммония, С ∑РЗЭ,
концентрации исходной азотной кислоты и ионной силе
|
Sm/Nd
|
C NH4NO3, М в.ф.
|
С ∑РЗЭ, г/л по окиси ICP-OES в.ф.
|
C HNO3 М, в.ф., исход. расчетное
|
Ионная сила
|
Фактор разделения в
|
|
|
|
|
|
Ce/La
|
Pr/Ce
|
Nd/Pr
|
Eu/Sm
|
Gd/Eu
|
Y/Gd
|
|
1,14
|
5,75
|
1,94
|
0,01
|
5,83
|
1,33
|
1,02
|
1,18
|
н/о
|
н/о
|
н/о
|
|
1,21
|
5,415
|
8,49
|
0,01
|
5,67
|
1,18
|
1,33
|
н/о
|
н/о
|
н/о
|
|
1,25
|
5,08
|
20,3
|
0,01
|
5,63
|
1,2
|
1,01
|
1,34
|
н/о
|
н/о
|
н/о
|
|
1,3
|
4,74
|
16,1
|
0,01
|
5,3
|
1,28
|
1,07
|
1,39
|
н/о
|
н/о
|
н/о
|
|
1,32
|
2,18
|
17,1
|
0,629
|
3,02
|
1,15
|
1,11
|
1,1
|
1,02
|
0,928
|
0,765
|
|
1,32
|
4,4
|
22,5
|
0,01
|
5,15
|
1,3
|
1,07
|
1,44
|
н/о
|
н/о
|
н/о
|
|
1,33
|
2,05
|
29,9
|
0,943
|
3,48
|
1,21
|
1,12
|
1,13
|
1,03
|
0,956
|
н/о
|
|
1,33
|
4,06
|
37,6
|
0,01
|
5,14
|
1,32
|
1,11
|
1,52
|
1,23
|
1,03
|
н/о
|
|
1,34
|
1,81
|
56,1
|
1,73
|
4,51
|
1,27
|
1,18
|
1,18
|
1,06
|
0,905
|
0,646
|
|
1,34
|
2,29
|
8,43
|
0,314
|
2,69
|
1,14
|
1,09
|
1,1
|
н/о
|
н/о
|
н/о
|
|
1,34
|
3,38
|
64,3
|
0,01
|
5,38
|
1,32
|
1,08
|
1,58
|
1,27
|
1,2
|
н/о
|
|
1,35
|
2,71
|
150
|
0,01
|
7,52
|
1,5
|
1,11
|
1,46
|
1,23
|
1,77
|
н/о
|
|
1,36
|
1,93
|
41,2
|
1,18
|
3,92
|
1,21
|
1,17
|
1,1
|
1,03
|
0,932
|
0,604
|
|
1,38
|
1,45
|
93,7
|
2,36
|
6,17
|
1,3
|
1,22
|
1,2
|
1,09
|
1,08
|
1,14
|
|
1,39
|
0
|
343,3
|
0,01
|
12,5
|
1,82
|
1,12
|
1,78
|
1,17
|
1,09
|
н/о
|
|
1,39
|
0,338
|
353,4
|
0,01
|
13,4
|
1,85
|
1,15
|
1,9
|
1,21
|
1,23
|
н/о
|
|
1,39
|
1,35
|
315,2
|
0,01
|
12,3
|
1,71
|
1,1
|
1,74
|
1,18
|
1,33
|
н/о
|
|
1,39
|
2,03
|
202,9
|
0,01
|
8,79
|
1,66
|
1,12
|
1,69
|
1,17
|
1,46
|
н/о
|
|
1,41
|
1,69
|
69,6
|
1,89
|
5,1
|
1,28
|
1,2
|
1,2
|
1,04
|
0,934
|
0,663
|
|
1,51
|
0,966
|
159
|
3,77
|
8,87
|
1,44
|
1,32
|
1,29
|
1,11
|
1,09
|
1,42
|
|
1,53
|
1,21
|
128
|
2,83
|
7,54
|
1,38
|
1,29
|
1,25
|
1,05
|
1,06
|
1,25
|
|
1,58
|
0
|
310
|
5,42
|
15,4
|
1,31
|
1,26
|
1,27
|
1,14
|
1,24
|
1,99
|
|
1,60
|
0,725
|
207
|
4,24
|
10,7
|
1,49
|
1,38
|
1,34
|
1,11
|
1,07
|
0,935
|
|
1,65
|
0,362
|
252
|
4,95
|
12,7
|
1,44
|
1,36
|
1,34
|
1,12
|
1,2
|
1,52
|
|
1,80
|
5,18
|
10,9
|
1,2
|
6,06
|
1,41
|
1,4
|
1,39
|
н/о
|
н/о
|
н/о
|
|
1,83
|
6,65
|
19,2
|
0,01
|
7,3
|
1,29
|
1,2
|
0,997
|
1,2
|
0,864
|
1,43
|
|
1,87
|
7,13
|
10,2
|
0,01
|
7,53
|
1,82
|
0,834
|
0,996
|
1,46
|
0,706
|
0,797
|
|
1,88
|
2,44
|
154
|
4,81
|
11
|
1,56
|
1,44
|
1,43
|
1,14
|
1,24
|
1,25
|
|
1,89
|
0
|
305
|
0,01
|
10,8
|
1,58
|
1,28
|
0,985
|
1,08
|
1,35
|
0,491
|
|
1,89
|
7,6
|
3,8
|
0,01
|
7,56
|
1,21
|
1,02
|
1,17
|
1,11
|
1,99
|
н/о
|
|
1,90
|
3,8
|
140
|
0,01
|
8,85
|
1,37
|
1,21
|
1
|
1,22
|
1,12
|
0,667
|
|
1,90
|
4,87
|
23,5
|
1,6
|
6,43
|
1,44
|
1,37
|
1,4
|
н/о
|
н/о
|
н/о
|
|
1,93
|
0,914
|
223
|
6,81
|
14,8
|
1,42
|
1,38
|
1,38
|
1,14
|
1,25
|
1,57
|
|
1,94
|
4,75
|
93,5
|
0,01
|
8,065
|
1,23
|
0,995
|
1,18
|
0,974
|
0,697
|
|
1,95
|
2,85
|
188
|
0,01
|
9,66
|
1,42
|
1,21
|
1,01
|
1,07
|
1,49
|
0,52
|
|
1,97
|
4,26
|
53,86
|
2,41
|
7,4
|
1,58
|
1,38
|
1,46
|
1,1
|
1,32
|
0,944
|
|
2,00
|
3,05
|
119
|
4,01
|
9,68
|
1,57
|
1,44
|
1,45
|
1,1
|
1,27
|
1,17
|
|
2,01
|
1,83
|
187
|
5,61
|
13,8
|
1,57
|
1,41
|
1,42
|
1,12
|
1,17
|
1,48
|
|
2,04
|
0,475
|
296
|
0,01
|
11,3
|
1,65
|
1,31
|
0,982
|
1,04
|
1,54
|
0,469
|
|
2,06
|
1,9
|
229
|
0,01
|
9,77
|
1,59
|
1,26
|
1,01
|
1,08
|
1,25
|
0,525
|
|
2,1
|
4,57
|
39
|
2
|
6,79
|
1,5
|
1,38
|
1,44
|
1,02
|
1,41
|
0,865
|
|
2,14
|
0
|
271
|
8,02
|
16,1
|
1,57
|
1,42
|
1,41
|
1,1
|
1,35
|
1,98
|
|
2,14
|
5,7
|
53,4
|
0,01
|
7,41
|
1,34
|
1,19
|
1,03
|
1,09
|
0,909
|
0,768
|
|
2,17
|
3,65
|
90,2
|
3,21
|
8,49
|
1,56
|
1,39
|
1,42
|
1,06
|
1,38
|
0,938
|
|
2,38
|
8,08
|
1,1
|
0,01
|
8,08
|
1,28
|
1,26
|
0,941
|
0,91
|
0,496
|
н/о
|
|
2,47
|
6,18
|
39,2
|
0,01
|
7,71
|
1,35
|
1,25
|
0,976
|
0,987
|
0,882
|
0,989
|
|
н/о
|
5,48
|
3,5
|
0,802
|
5,87
|
1,4
|
1,32
|
1,35
|
н/о
|
н/о
|
н/о
|
|
н/о
|
5,79
|
0,781
|
0,401
|
5,95
|
1,3
|
1,24
|
1,3
|
н/о
|
н/о
|
н/о
|
Таблица Ж.18 - Фактор разделения пары Nd/Pr в системе H2O -
HNO3 - NH4NO3 - Ln(NO3)3
- ТБФ 100% при различных концентрациях нитрата аммония, С ∑РЗЭ,
концентрации исходной азотной кислоты и ионной силе
|
Nd/Pr
|
C NH4NO3, в.ф.
|
С ∑РЗЭ, г/л по окиси ICP-OES в.ф.
|
C HNO3 М, в.ф., исход. расчетное
|
Ионная сила
|
Фактор разделения в
|
|
|
|
|
|
Ce/La
|
Pr/Ce
|
Sm/Nd
|
Eu/Sm
|
Gd/Eu
|
Y/Gd
|
|
0,941
|
8,08
|
1,10
|
0,010
|
8,08
|
1,28
|
1,26
|
2,38
|
0,910
|
0,496
|
н/о
|
|
0,976
|
6,18
|
39,2
|
0,010
|
7,71
|
1,35
|
1,25
|
2,47
|
0,987
|
0,882
|
0,989
|
|
0,982
|
0,475
|
296
|
0,010
|
11,3
|
1,65
|
1,31
|
2,04
|
1,04
|
1,54
|
0,469
|
|
0,985
|
0,000
|
305
|
0,010
|
10,8
|
1,58
|
1,28
|
1,89
|
1,08
|
1,35
|
0,491
|
|
0,995
|
4,75
|
93,5
|
0,010
|
8,07
|
1,38
|
1,23
|
1,94
|
1,18
|
0,974
|
0,697
|
|
0,996
|
7,13
|
10,2
|
0,010
|
7,53
|
1,82
|
0,834
|
1,87
|
1,46
|
0,706
|
0,797
|
|
0,997
|
6,65
|
19,2
|
0,010
|
7,30
|
1,29
|
1,20
|
1,83
|
1,20
|
0,864
|
1,43
|
|
1,000
|
3,800
|
140
|
0,010
|
8,85
|
1,37
|
1,21
|
1,90
|
1,22
|
1,12
|
0,667
|
|
1,010
|
1,900
|
229
|
0,010
|
9,77
|
1,59
|
1,26
|
2,06
|
1,08
|
1,25
|
0,525
|
|
1,01
|
2,85
|
188
|
0,010
|
9,66
|
1,42
|
1,21
|
1,95
|
1,07
|
1,49
|
0,520
|
|
1,03
|
5,70
|
53,4
|
0,010
|
7,41
|
1,34
|
1,19
|
2,14
|
1,09
|
0,909
|
0,768
|
|
1,10
|
1,93
|
41,2
|
1,18
|
3,92
|
1,21
|
1,17
|
1,36
|
1,03
|
0,932
|
0,604
|
|
1,10
|
2,18
|
17,1
|
0,629
|
3,02
|
1,15
|
1,11
|
1,32
|
1,02
|
0,928
|
0,765
|
|
1,10
|
2,29
|
8,43
|
0,314
|
2,69
|
1,14
|
1,09
|
1,34
|
н/о
|
н/о
|
н/о
|
|
1,13
|
2,05
|
29,9
|
0,943
|
3,48
|
1,21
|
1,12
|
1,33
|
1,03
|
0,956
|
н/о
|
|
1,17
|
7,60
|
3,80
|
0,010
|
7,56
|
1,21
|
1,020
|
1,89
|
1,11
|
1,99
|
н/о
|
|
1,18
|
1,81
|
1,73
|
4,51
|
1,27
|
1,18
|
1,34
|
1,06
|
0,905
|
0,646
|
|
1,18
|
5,75
|
1,94
|
0,010
|
5,83
|
1,33
|
1,02
|
1,140
|
н/о
|
н/о
|
н/о
|
|
1,20
|
1,45
|
93,7
|
2,36
|
6,17
|
1,30
|
1,22
|
1,38
|
1,09
|
1,08
|
1,14
|
|
1,20
|
1,69
|
69,6
|
1,89
|
5,10
|
1,28
|
1,20
|
1,410
|
1,040
|
0,934
|
0,663
|
|
1,25
|
1,21
|
128
|
2,83
|
7,54
|
1,38
|
1,29
|
1,53
|
1,05
|
1,06
|
1,25
|
|
1,27
|
0,000
|
310
|
5,42
|
15,4
|
1,31
|
1,26
|
1,58
|
1,14
|
1,24
|
1,99
|
|
1,29
|
0,966
|
159
|
3,77
|
8,87
|
1,44
|
1,32
|
1,51
|
1,11
|
1,09
|
1,42
|
|
1,30
|
5,79
|
0,781
|
0,401
|
5,95
|
1,30
|
1,24
|
н/о
|
н/о
|
н/о
|
н/о
|
|
1,33
|
5,42
|
8,49
|
0,010
|
5,670
|
1,18
|
1,05
|
1,21
|
н/о
|
н/о
|
н/о
|
|
1,34
|
0,362
|
252
|
4,95
|
12,7
|
1,44
|
1,36
|
1,65
|
1,120
|
1,200
|
1,520
|
|
1,34
|
0,725
|
207
|
4,24
|
10,7
|
1,49
|
1,38
|
1,60
|
1,11
|
1,07
|
0,935
|
|
1,34
|
5,08
|
20,3
|
0,010
|
5,63
|
1,20
|
1,01
|
1,25
|
н/о
|
н/о
|
н/о
|
|
1,35
|
5,48
|
3,50
|
0,802
|
5,87
|
1,40
|
1,32
|
н/о
|
н/о
|
н/о
|
н/о
|
|
1,38
|
0,914
|
223
|
6,81
|
14,8
|
1,42
|
1,38
|
1,93
|
1,14
|
1,25
|
1,57
|
|
1,39
|
4,74
|
16,1
|
0,010
|
5,30
|
1,28
|
1,07
|
1,30
|
н/о
|
н/о
|
н/о
|
|
1,39
|
5,18
|
10,9
|
1,20
|
6,06
|
1,41
|
1,40
|
1,80
|
н/о
|
н/о
|
н/о
|
|
1,40
|
4,87
|
23,5
|
1,60
|
6,43
|
1,44
|
1,37
|
1,90
|
н/о
|
н/о
|
н/о
|
|
1,41
|
0,000
|
271
|
8,02
|
16,1
|
1,57
|
1,42
|
2,14
|
1,10
|
1,35
|
1,98
|
|
1,42
|
1,83
|
187
|
5,61
|
13,8
|
1,57
|
1,41
|
2,01
|
1,12
|
1,17
|
1,48
|
|
1,42
|
3,65
|
90,2
|
3,21
|
8,49
|
1,56
|
1,39
|
2,17
|
1,06
|
1,38
|
0,938
|
|
1,43
|
2,44
|
154
|
4,81
|
11,0
|
1,56
|
1,44
|
1,88
|
1,14
|
1,24
|
1,25
|
|
1,44
|
4,40
|
22,5
|
0,010
|
5,15
|
1,30
|
1,07
|
1,32
|
н/о
|
н/о
|
н/о
|
|
1,44
|
4,57
|
39,0
|
2,00
|
6,79
|
1,50
|
1,38
|
2,10
|
1,02
|
1,41
|
0,865
|
|
1,45
|
3,05
|
119
|
4,01
|
9,68
|
1,57
|
1,44
|
2,00
|
1,10
|
1,27
|
1,170
|
|
1,46
|
2,71
|
150
|
0,010
|
7,52
|
1,50
|
1,11
|
1,35
|
1,23
|
1,77
|
н/о
|
|
1,46
|
4,26
|
53,9
|
2,41
|
7,40
|
1,58
|
1,38
|
1,97
|
1,10
|
1,32
|
0,944
|
|
1,52
|
4,06
|
37,6
|
0,010
|
5,14
|
1,32
|
1,11
|
1,33
|
1,23
|
1,03
|
н/о
|
|
1,58
|
3,38
|
64,3
|
0,010
|
5,38
|
1,32
|
1,08
|
1,34
|
1,27
|
1,20
|
н/о
|
|
1,69
|
2,03
|
203
|
0,010
|
8,79
|
1,66
|
1,12
|
1,39
|
1,17
|
1,46
|
н/о
|
|
1,74
|
1,35
|
315
|
0,010
|
12,3
|
1,71
|
1,10
|
1,39
|
1,18
|
1,33
|
н/о
|
|
1,78
|
0,000
|
343
|
0,010
|
12,5
|
1,82
|
1,12
|
1,39
|
1,17
|
1,09
|
н/о
|
|
1,90
|
0,338
|
353
|
0,010
|
13,4
|
1,85
|
1,15
|
1,39
|
1,21
|
1,23
|
н/о
|