Окислительно-восстановительные превращения хинонов
Министерство
науки и образования РФ
Федеральное
государственное бюджетное образовательное учреждение высшего профессионального
образования
«Кемеровский
государственный университет»
Кафедра
органической химии
Реферат
по дисциплине «Химия хинонов»
«Окислительно-восстановительные
превращения хинонов»
Проверил:
К.х.н. Ткаченко
Т.Б.
Выполнил:
студент группы
х-121
Никифоров В.Е.
Кемерово
Содержание
Введение
Хиноны
Восстановление
хинонов
Окисление
хинонов
Заключение
Список
литературы
Введение
Химия хинонов и их производных давно выделилась
в самостоятельную и обширную область органической химии, имеющую большое
практическое значение. Хиноны, его производные и их соединения, вырабатываемые
промышленностью, используют для получения органических красителей, пигментов,
для синтеза лекарственных и природных соединений, антибиотиков, в качестве
катализаторов, аналитических реагентов, средства защиты растений и т. д. В
природе соединения хинонов встречаются в растениях, насекомых, морских
животных, микроорганизмах.
Хиноны
Хиноны - циклические дикетоны, в молекулах
которых кетогруппы входят в систему сопряженных двойных связей. Наиболее
практическое значение имеют бензохиноны, нафтохиноны, 9,10-антрахинон а также
1,2- и 1,4-антрахиноны, 1,2-, 1,4- и 3,4-фенантрахиноны и некоторые дихиноны,
например 1,4,5,8- нафтодихинон (VI).

Хиноны - окрашенные кристаллы. Окраска хинонов
во многом зависит от взаимного расположения карбонильных групп в молекуле: 1,2-хиноны
окрашены, как правило, в красный или оранжево-красный цвет, 1,4-хиноны окрашены
менее интенсивно - в желтый или светло-желтый цвет. 1,4-Хиноны обладают большей
летучестью и более резким запахом, чем 1,2-хиноны. [2]
Восстановление хинонов
Наиболее важной реакцией хинонов является их
восстановление до двухатомных фенолов. Восстановление хинонов осуществляется в
две стадии. На первой стадии в результате одноэлектронного восстановления
образуются анион-радикалы, которые называют также семихинонами. Эти частицы
могут быть легко зарегистрированы с помощью ЭПР-спекроскопии. На второй стадии
анион-радикал присоединяет еще один электрон с образованием дианиона
двухатомного фенола.

Способность хинона восстанавливаться
до двухатомного фенола, т.е. свойство его как окислителя, оценивается с помощью
нормального редокс-потенциала, определяемого из уравнения Нернста для реакции:

Величина Ео представляет собой
нормальный потенциал, характерный для каждой системы хинон-гидрохинон, при
равных концентрациях хинона и гидрохинона и концентрации ионов водорода, равной
единице. Таким образом, Ео является количественной характеристикой
окислительной способности хинона. В таблице 3 приведены значения нормальных
редокс-потенциалов Ео для некоторых хинонов в воде при 25оС.
Таблица 1
Величины нормальных
редокс-потенциалов Ео некоторых хинонов в воде при 25оС
|
Хинон
|
Ео
в мв
|
Хинон
|
Ео
в мв
|
|
1,2-бензохинон
|
783
|
2,3-дихлор-1,4-нафтохинон
|
499
|
|
1,4-бензохинон
|
700
|
9,10-антрахинон
|
130
|
|
2-метил-1,4-бензохинон
|
645
|
1,4-антрахинон
|
400
|
|
2-хлор-1,4-бензохинон
|
713
|
9,10-фенантренхинон
|
440
|
|
1,2-нафтохинон
|
566
|
1,4-фенантренхинон
|
520
|
|
1,4-нафтохинон
|
470
|
1,6-пиренхинон
|
610
|
|
2,6-нафтохинон
|
758
|
3,4,5,6-тетрахлор-1,4-бензохинон
|
740
|
|
2-метил-1,4-нафтохинон
|
422
|
дифенохинон
|
954
|
Из данных, представленных в таблице 1 следует,
что 1,2-хиноны более сильные окислители, чем 1,4-хиноны, а бензохиноны
превосходят по окислительной способности хиноны нафталинового ряда, которые в
свою очередь превосходят антрахиноны и фенантренхиноны. Электроноакцепторные
группы усиливают окислительные свойства хинонов. Высокие редокс-потенциалы
хинонов определяются тем, что восстановление хинона в двухатомный фенол
сопровождается превращением ненасыщенного кетона в ароматическое соединение.

Окрашенный в темно-зеленый цвет хингидрон
представляет собой классический пример молекулярных комплексов, где один
компонент служит донором, а другой - является акцептором электрона. Такие
комплексы, где происходит перекрывание ВЗМО донора и НСМО акцептора, получили
название комплексов с переносом заряда. К ним относятся -комплексы
ароматических соединений с галогенами, катионами серебра и ртути;
1,3,5-тринитробензолом, пикриновой кислотой. Комплексы галогенов или тетрацианоэтилена
с n-донорами (спиртами, простыми эфирами) или -донорами - (алкенами или
алкинами), также следует рассматривать как комплексы с переносом заряда. В
кристаллах хингидрона молекулы хинона и гидрохинона чередуются и располагаются
в двух параллельных плоскостях друг над другом. Комплексы с переносом заряда
часто интенсивно окрашены. Так, например, тетрацианоэтилен образует с дуролом
(1,2,4,5-тетраметилбензолом) комплекс, окрашенный в красный цвет. Окраска
комплексов обусловлена переносом заряда от ароматического донора к акцептору,
хотя степень переноса заряда невелика и редко превышает 0,1 заряда электрона.
Восстановление хинонов до двухатомных фенолов
проводят с помощью самых разнообразных восстановителей, среди которых в
лабораторных условиях предпочтение отдается дитиониту натрия Na2S2O4 в щелочной
среде.

Помимо дитионита натрия в качестве
восстановителей употребляются алюмогидрид лития и боргидрид натрия, хлорид
олова (II) в соляной кислоте, цинк в уксусной кислоте и др. В промышленности
восстановление 1,4-бензохинона до гидрохинона осуществляется с помощью оксида
серы (IY) и железа в воде при 70-80оС.
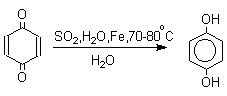
9,10-Антрахинон при восстановлении дитионитом
натрия образует 9,10-антрадиол (антрагидрохинон).

При восстановлении 9,10-антрахинона оловом в
смеси соляной и уксусной кислот получается антрон - простейший кетон ряда
антрацена.

Восстановление антрахиноновых и других кубовых
красителей дитионитом натрия в щелочной среде используется для перевода этих
нерастворимых в воде соединений в так называемую лейкоформу, которая в виде
динатриевой соли хорошо растворима в воде. Таким образом, например, упомянутый выше
индантрен восстанавливают в тетрагидропроизводное, имеющее четыре фенольных
гидроксила. Это лейкопроизводное хорошо растворимое в воде. Хлопчатобумажную
ткань пропитывают раствором лейкоформы и выдерживают на воздухе. Лейкоформа
окисляется кислородом до исходного красителя.
 [3]
[3]
Такой способ крашения гарантирует однородность
окраски ткани. Он применяется при крашении индигоидными и другими кубовыми
красителями.
Окисление хнонов
Окислительные превращения хинонов в большей
степени затрагивают заместители в бензольном кольце:
восстановление хинон
фенол



Окислению можно подвергать производные
антрахиноны, в которых бензольное кольцо конденсировано с антрахиноновым ядром.
При такой реакции будут образовываться и/или карбонильная и карбоксильная
группы.

[O]= KMnO4,K2Cr2O7 (H2SO4)

Реакции дегидрирования заместителей так же
относят к процессам окисления.

Превращения метильных групп в антрахинонах
наряду с циклизацией бензоилбонзойных кислот - один из главных методов
получения антрахинонкарбоновых кислот и практически единственный метод
получения соответствующих альдегидов. Метилантрахиноны окисляют хромовой и
азотной кислотами, диоксидом марганца, кислородом воздуха, озоном или
галогенируют метильные группы с последующим гидролизом.
Окисление хромовой кислотой применяют в
производстве 1-нитроантрахинон-2-карбоновой кислоты, обрабатывая
1-нитро-2-метилантрахинон CrO3 в концентрированной H2SO4 при 70 оC или K2Cr2O7
при 25-30 оC (выход >90%).
Окисление азотной кислотой осуществляют обычно
под давлением при концентрациях HNO3 ~20% и 190-210 оС. Так, из
2,3,6,7-тетраметилантрахинона синтезирована антрахинон-2,3,6,7-тетракарбоновая
кислота. 1-Метил-4-нитроантрахинон окислен в 4-нитроантрахинон-1-карбоновую
кислоту в 47%-ной HNO3 при 170оС.
Диоксидом марганца в H2SO4 метилантрахиноны
могут быть окислены как в альдегиды, так и в кислоты, причем метильные группы в
α-положении
окисляются легче, чем в β-положении.
Взаимодействие 1-метилантрахинона с MnO2 в ~85%-ной H2SO4 при 50оС приводит к
1-формилантрахинону. При большем избытке MnO2 с хорошим выходом образуются
карбоновые кислоты. Например, 2,3-диметиантрахинон при действии MnO2 в H2SO4 при
100 оС в присутствии NH4VO3 переходит в антрахинон-2,3-дикарбоновую кислоту.
Окисление кислородом воздуха β-антрахинонкарбоновые
кислоты протекает в уксусной кислоте в присутствии ацетатов Co2+,Mn2+ и NaBr
при 200 оС и ~2,5 МПа, окисление озоно-кислородной смесью - в уксусной кислоте
в присутствии ацетата Co2+ или 70%-ной H2SO4 в присутствии солей Cr3+,Mn2+.
Практически важно внутримолекулярное
окислительно-восстановительное превращение 2-метил-1-нитроантрахинона в
1-аминоантрахинон-2-карбоновую кислоту. При этом сначала идет циклизация . При
этом сначала идет циклизация под действием 60-65%-ного олеума или SO3 в
инертном растворителе при 5-15 оС в антра[1,2-с]изоксазол-6,11-дион , щелочной
гидролиз которого дает кислоту.
-Аминоантрахинон-2-карбоновая кислота и
1-амино-2-формилантрахинон могут быть получены так же окислением
1-амино-2-гидроксиметилантрахинона, образующегося при гидроксиметилировании
1-аминоантрагидрохинона. 1-Амино-2-гидроксиметилантрахинон при нагревании с
NaOH в водном диметилсульфокислоте (1:1) в атмосфере азота количественно
перегруппировывается в 1-амино-2формил-9,10-антрагидрохинон, который после
подкисления соляной кислотой окисляется воздухом в 1-амино-2-формилантрахинон
(рис. 1).

рис. 1.
Из других реакций окисления следует отметить
окисление аминогрупп в нитрогруппы пероксикислотами, имеющее препаративное
значение для синтеза нитроантрахиноно, которые нельзя получить нитрованием.
Так, кипячением соответствующего β-аминоантрахинона
в смеси перуксусной и уксусной кислот или трифторперуксусной кислоты и
хлороформа получены 2-нитро-1-хлорантрахинон (выход 82-90%),
2-бром-3-нитроантрахинон (61%), 2,3-динитроантрахинон (36%). Из
1,4-диамино-2,3-диметилантрахинона оксилением перуксусной кислотой синтезирован
2,3-диметил-1,4-динитроантрахинон, а из 1-амино-4-нитроантрахинона и его
5,8-дихлорзамещенного при обработке (NH4)2S2O8 и затем CrO3 - 1,4-динитро- и
1,4-динитро-5,8- дихлорантрахиноны. [4]
Заключение
Хиноны являются структурной основой пигментов.
Восстановление хинонов используется для превращения красителей в лейкоформу,
которые могут растворяться в воде и быть нанесенными на поверхность. Важнейший
краситель - ализарин (1,2-диоксиантрахинон). Ализариновые красители
светоустойчивы, применяются в лакокрасочной промышленности, полиграфии. Но
из-за большой стоимости используются реже, чем азокрасители. Окислительные
свойства хинонов проявляются в биохимических реакциях. Убихиноны (коферменты Q)
распространены в животном и растительном мире, участвуют в переносе электронов
и протонов в дыхательной цепи. [1]
Список литературы
[1]
Википедия - свободная энциклопедия. - Хиноны:
https://ru.wikipedia.org/wiki/Хиноны
[2]http://www.xumuk.ru/encyklopedia/2/5017.html
( Кэсон Д., в сб.: Органические реакции, пер. с англ., сб. 4, М., 1951, с.
270-336; Эфрос Л. С., Горелик М. В, Химия
<http://www.xumuk.ru/encyklopedia/2/4995.html> и технология промежуточных
продуктов, Л., 1980; Общая органическая химия, пер. с англ., т. 2, М., 1982, с.
830-47. См. также лит. при ст. Антрахиноновые красители
<http://www.xumuk.ru/encyklopedia/341.html>.)
[3]
Курц А. Л. Фенолы и Хиноны/ Курц А Л., Ливанцов М.В., Ливанцова Л.И. .-
http://www.chem.msu.su/rus/teaching/phenol/6.html. (2.4.2015)
[4]
Горелик М. В. - Химия антрахинонов и их производных. -М.: Химия, 1983.- 296 с.