Очистка конвертированного газа в производстве аммиака от диоксида углерода растворами горячего поташа
Министерство
образования и науки Российской Федерации
Федеральное
государственное бюджетное образовательное учреждение
высшего профессионального образования
Пермский
национальный исследовательский политехнический университет
Кафедра
Химические технологии
КУРСОВОЙ
ПРОЕКТ
По
дисциплине: Общая химическая технология
ОЧИСТКА
КОНВЕРТИРОВАННОГО ГАЗА ОТ ДИОКСИДА УГЛЕРОДА РАСТВОРОМ ГОРЯЧЕГО ПОТАША В
ПРОИЗВОДСТВЕ АММИАКА
СОДЕРЖАНИЕ
1. Введение. Краткое изложение
существа работы
. Выбор и обоснование источников
сырья, энергоресурсов, географической точки строительства
. Выбор и обоснование способа
производства
. Обоснование оптимальных
параметров технологического процесса
.1 Термодинамический анализ
.2 Кинетический анализ
. Синтез и анализ ХТС
.1 Химическая модель
.2 Структурная схема
.3 Операторная схема
Технологическая схема
. Выбор и основание
конструкции основного аппарата
Эскиз основного аппарата
. Расчет материального и
энергетического балансов. Определение расходных норм по сырью и энергии. Пути
использования вторичных энергоресурсов
.1 Материальный баланс процесса
.2 Тепловой баланс
.3 Расходные нормы по сырью и
энергии
.4 Пути использования вторичных
ресурсов
. Экологическая оценка
производства. Отходы производства и их утилизация. ПДК
Заключение
Список литературы
1. ВВЕДЕНИЕ. КРАТКОЕ ИЗЛОЖЕНИЕ СУЩЕСТВА РАБОТЫ
Во всех индустриально развитых странах азотная
промышленность является в настоящее время одной из основных ведущих отраслей.
Бурное развитие азотной промышленности диктуется в первую очередь
необходимостью удовлетворения неудержимо растущего населения земного шара
продуктами земледелия. Без минеральных удобрений, и в первую очередь азотных,
невозможно решить задачи интенсификации сельского хозяйства.
Производству азотных удобрений и их основы,
аммиака, в нашей стране всегда уделялось первостепенное внимание. Среднегодовой
прирост темпа аммиака за последние 20 лет составляет 10-19%.
Технологический газ, пригодный для синтеза
аммиака, может быть получен практически из любого углеводородного сырья:
природного газа, попутного газа нефтедобычи, газов переработки нефти, из нефти
и ее производных: бензинов, мазутов, из каменного и бурого углей, сланцев и
торфа. Основным сырьем производства аммиака (и азотных удобрений на его основе)
в нашей стране является природный газ. Производство аммиака подразделяется на 6
стадий:
1. Подготовка природного газа к конверсии
(сероочистка);
. Двухступенчатая паровоздушная конверсия
(риформинг) природного газа;
. Конверсия оксида углерода водяным
паром;
4. Очистка конвертированного газа от
диоксида углерода;
. Метанирование оксидов углерода;
. Синтез аммиака
Важную роль в производстве аммиака играет
очистка газов[1]. Она предусматривает удаление из
промышленных или природных газов вредных и балластных примесей с тем, чтобы
очищеный газ был пригоден для транспортирования, дальнейшей химической
переработки и непосредственного использования.
К настоящему времени на практике применяются
следующие виды очистки конвертированного газа от СО2:
· Абсорбция растворами карбонатов
· Абсорбция органическими
растворителями
· Водная и щелочная очистка
· Очистка водным раствором аммиака
В большем количестве получил распространение
метод поташной очистки (в зависимости от предприятия и технологической схемы
горячие поташные растворы или растворы, активированные соединениями мышьяка).
2. ВЫБОР И ОБОСНОВАНИЕ ИСТОЧНИКОВ СЫРЬЯ,
ЭНЕРГОРЕСУРСОВ, ГЕОГРАФИЧЕСКОЙ ТОЧКИ СТРОИТЕЛЬСТВА
Процесс производства аммиака характеризуется
большой энергоемкостью, что является главным его недостатком. Именно поэтому
постоянно ведутся научные разработки, которые призваны решить проблемы экономии
энергии. В частности разрабатываются способы утилизации выделенной энергии, а
также совмещение, например, производства аммиака и карбамида. Все это
способствует удешевлению деятельности предприятий и повышению их полезной
отдачи.
Первостепенным энергоресурсом будет являться
электроэнергия, расходуемая на работу оборудования: насосы, компрессоры,
установок, предназначенных для нагрева (котлы, печи) посредством электрической
энергии. Помимо технологического применения электричество используется для
освещения производственных помещений. Основным теплоносителем и хладагентом
будет являться водяной пар и вода.
Сама технологическая схема производства аммиака
зависит, прежде всего, от сырья, из которого получается конечный продукт. Дело
в том, что, в отличие от азота, который содержится в воздухе в больших
количествах, водород в чистом виде в природе практически не присутствует, а
выделять его из воды - довольно трудоемкий и энергозатратный процесс[2].
Географическое расположение подразумевает
размещение завода вблизи основного сырья - месторождений газа или заводов
нефтепереработки, которые могут предоставить попутный нефтяной газ или
природный газ на продажу.
Начнем рассмотрение процесса с изучения сырья и
получаемого целевого продукта. В качестве сырья для производства аммиака в
основном используются углеводороды, содержащиеся в природном газе. По
использованию окислителя и технологическому оформлению можно выделить следующие
варианты процесса получения водородосодержащих газов: высокотемпературная
кислородная конверсия, каталитическая парокислородная конверсия в шахтных ҏеакторах,
каталитическая пароуглекислотная конверсия в трубчатых печах. Перед
переработкой конвертированного природного газа необходимо провести процесс
очистки. Очистка технологического газа направлена на снижение концентрации
диоксида углерода с последующим его выводом из системы.
Оксид углерода(IV) - углекислый газ, газ без
запаха и цвета, при сильном охлаждении кристаллизуется в виде белой
снегообразной массы - «сухого льда». При атмосферном давлении он не плавится, а
испаряется, температура сублимации −78 °С. Углекислый газ образуется при
гниении и горении органических веществ. Содержится в воздухе и минеральных
источниках, выделяется при дыхании животных и растений. Растворим в воде (1
объём углекислого газа в одном объёме воды при 15 °С). Плотность при нормальных
условиях 1,97 кг/м³. Концентрация
углекислого газа в атмосфере Земли составляет в среднем 0,0395 %. Углекислый
газ легко пропускает ультрафиолетовые лучи, и лучи видимой части спектра,
которые поступают на Землю от Солнца и обогревают её. В то же время он
поглощает испускаемые Землёй инфракрасные лучи и является одним из парниковых
газов, вследствие чего принимает участие в процессе глобального потепления.
Постоянный рост уровня содержания этого газа в атмосфере наблюдается с начала
индустриальной эпохи.
Диоксид углерода играет одну из главных ролей в
живой природе, участвуя во многих процессах метаболизма живой клетки,
получается в результате множества окислительных реакций у животных, и
выделяется в атмосферу с дыханием. Углекислый газ атмосферы - основной источник
углерода для растений. Однако, ошибкой будет утверждение, что животные только
выделяют углекислый газ, а растения - только поглощают его. Растения поглощают
углекислый газ в процессе фотосинтеза, а без освещения они тоже его выделяют.
Диоксид углерода не токсичен, но не поддерживает
дыхание. Большая концентрация в воздухе вызывает гиперкапнию - состояние,
связанное с избытком CO2 в крови (оно может вызываться и задержкой дыхания),
когда его парциальное давление превышает 45 мм рт. ст. Однако недостаток
углекислого газа в крови (гипокапния, возникающая, например, при
гипервентиляции лёгких) тоже опасен.
В пищевой промышленности углекислота
используется как консервант и разрыхлитель, обозначается на упаковке кодом
Е290. Так же применяется для газирования лимонада и газированной воды, в
качестве защитной среды при сварке проволокой. «Сухой лёд» - используется в
качестве хладагента.
Очистку будем проводить поташным раствором,
рассмотрим его свойства. Карбонат калия (углекислый калий, пота́ш)
K2CO3 - средняя соль калия и угольной кислоты. Это белое кристаллическое
вещество, хорошо растворимое в воде. Малотоксичен, относится к III классу
опасности. Старое название соли - пота́ш,
от лат. Potassa. Поташ - одна из солей, известных людям ещё в древности. Обычно
поташ загрязнён различными примесями, поэтому не имеет такого чисто-белого
цвета, как измельчённый карбонат калия. До XX века поташ был одним из важнейших
промышленных химических реагентов. Его получали путём водной экстракции из
растительной золы, с дальнейшей очисткой до необходимого уровня. Производство
было сосредоточено в местах, богатых лесом - кое-где в Европе, но, в основном,
в России и Северной Америке.
В промышленности используют следующие виды
поташа: кальцинированный и полутораводный. В зависимости от физико-химических
свойств поташ подразделяется также на первый, второй и третий сорт. Используется
в химической и стекольной промышленности, в пожарном деле, в легкой
промышленности и в других отраслях. В строительстве поташ применяют в качестве
противоморозной добавки, в химической - для изготовления красок, в легкой - для
выделки кож. Также поташ применяется в изготовлении моющих средств. Он служит
сырьем для производства оптического стекла. В пожарном деле поташом
обрабатывают деревянные строения и конструкции. В сельском хозяйстве поташ
применяется в качестве удобрений, т.к. калий является жизненно важным элементом
для растений. Зарегистрирован в качестве пищевой добавки E501.
3.
ВЫБОР И ОБОСНОВАНИЕ СПОСОБА ПРОИЗВОДСТВА
Диоксид углерода содержится в природном и
коксовом газах, в конвертированном газе. В последнем содержание СО2 наибольшее
и составляет в зависимости от исходного сырья и метода конверсии 20 - 30 %
объемных. Можно выделить физические и химические методы очистки от диоксида
углерода. Физические методы основаны на повышенной растворимости его в
жидкостях или на конденсации СО2 при умеренном охлаждении. Большинство
химических методов основано на абсорбции этих примесей растворами химических
реагентов, а в случае тонкой очистки - на каталитическом восстановлении их Н2
до СН4. Почти все способы удаления СО2 дают возможность получить его в качестве
побочного продукта, используемого в производстве карбамида.
Для грубой очистки газа от двуокиси углерода
применяются следующие способы:
· Водная очистка под давлением, а
также физическая абсорбция органическими растворителями, имеющими низкое
давление паров при обычной температуре
· Моноэтаноламиновая очистка при
атмосферном давлении
· Очистка горячим раствором поташа
Для тонкой очистки газа от двуокиси углерода
применяются следующие способы:
· Моноэтаноламиновая очистка под
давлением
· Очистка водными растворами щелочей
· Низкотемпературная очистка
органическими растворителями с одновременным удалением из газа двуокиси
углерода и органических сернистых соединений
· Каталитическое гидрирование,
осуществляемое совместно с очисткой от окиси углерода
Водная очистка газов от СО2 под давлением
Способ очистки основан на различной
растворимости в воде двуокиси углерода. При невысоких парциальных давлениях
растворимость СО2 в воде невелика, но с увеличением давления она возрастает.
При следующем снижении давления растворённая двуокись углерода выделяется из
раствора. Водная очистка газа от двуокиси углерода под давлением весьма
эффективна при высоком содержании СО2 в газе. Этот способ отличается простотой
и позволяет многократно использовать оборотную воду. Одновременно с
растворением двуокиси углерода в воде растворяются и другие компоненты
конвертированного газа: водород, азот, окись углерода, сернистые соединения. По
химическим свойствам СО2 является ангидридом угольной кислоты. С водой реагирует
с образованием угольной кислоты, согласно уравнению:
Н2О + СО2 ↔ Н2СО3
В технической оборотной воде, используемой для
водной очистки от СО2, содержатся растворённые соли, которые понижают
растворимость СО2 в технической воде по сравнению с чистой. Существенное
значение для экономичности процесса водной очистки имеет расход воды на очистку
и расход энергии на подачу этой воды.
Расход воды на очистку конвертированного газа от
двуокиси углерода зависит от степени извлечения СО2, температуры, общего и
парциального давления СО2 в газовой смеси до очистки. Если конвертированный газ
в процессе конверсии углеводородов или газификации топлива получают при
атмосферном давлении, то перед водной очисткой газ компримируют. Выбор давления
для водной очистки от СО2 зависит от нескольких факторов.
С увеличением давления возрастает растворимость
СО2 в воде и уменьшается количество воды, необходимой для промывки, почти
обратно пропорционально давлению. При этом снижается расход энергии на подачу
воды. С другой стороны, работа сжатия двуокиси углерода от начального низкого
давления до давления абсорбции с увеличением давления возрастает. Суммарный
расход энергии на водную промывку газа в пределах 1-3 МПа практически не
зависит от давления. Однако с увеличением давления уменьшаются размеры
абсорбера и возрастает степень очистки газа от СО2.
Очистка газов от СО2 растворами этаноламинов
Для очистки газа от СО2 применяют растворы
этаноламинов (аминоспиртов), которые обладают щелочными свойствами и при
взаимодействии с кислотами образуют соли. Обычно используют водные растворы
моноэтаноламина СН2ОН-СН2-NH2, диэтаноламина (СН2ОН-СН2)2NH и триэтаноламина
(СН2ОН-СН2)3N. Наиболее сильным основанием среди этаноламинов является
моноэтаноламин, который нашёл широкое применение в промышленности для очистки
газов. При абсорбции СО2 растворами этаноламинов образуются карбонаты и
бикарбонаты. Попутно может абсорбироваться сероводород, и образовываться
сульфиды и бисульфиды. Эти соединения при температуре выше 100 °С диссоциируют
с выделением из растворов СО2 и H2S.
В процессе этаноламиновой очистки газа от СО2
протекают побочные реакции, вызывающие необратимые изменения состава раствора,
снижающие его поглотительную способность и приводящие к потерям амина. Растворы
этаноламинов вызывают коррозионное разрушение оборудования в определённых
условиях, особенно при высоких степенях насыщения кислыми газами. Подобно
растворам аммиака, они разрушающе действуют на медь, цинк и их сплавы. Поэтому
аппараты и трубы, соприкасающиеся с растворами аминов, нельзя выполнять из этих
металлов.
Очистка газов от СО2 горячим раствором поташа
Данный процесс основан на абсорбции кислых газов
водными растворами карбонатов калия и натрия, содержащими активирующие добавки
поливалентных металлов (As,
Se, Te,
Sb) или циклических
органических соединений. В промышленности в качестве таких активирующих добавок
получили соединения мышьяка, вводимые в растворы, как правило, в виде
мышьяковистого ангидрида.
Реакции поглощения двуокиси углерода можно
представить в виде следующих уравнений:
CO3 + H2O + CO2=2 KHCO3AsO3 + CO2+
H2O= KHCO3 + H3AsO33AsO3
+ K2CO3=
KHCO3+ KH2AsO3
Эффективность абсорбции CO2
горячими растворами поташа, активированными мышьяком, зависит от температуры,
парциального давления двуокиси углерода и водяного пара над раствором,
концентрации активирующей добавки и щелочности раствора.
Регенерация отработанных растворов с целью
выделения из них поглощенной двуокиси углерода производится путем снижения
давления раствора, поступающего на регенерацию. При регенерации таких растворов
воздухом возникает опасность окисления трехвалентного мышьяка в пятивалентный,
обладающий сильными кислотными свойствами, что снижает эффективность
абсорбента. Это нежелательное явление устраняется при частичном отборе раствора
для его последующего восстановления.
Недостатками метода очистки синтез-газа
моноэтаноламином являются коррозионные свойства растворителя, высокий расход
электроэнергии и пара для отгонки растворителя. Промывку синтез-газа горячим
раствором карбоната калия выгодно применять при давлениях 14 ат.
Щелочная очистка газа от СО2
Очистка газов от СО2 водным раствором едкого
натра NaOH основана на необратимой реакции:
+ СО2 = Na2СО3 + Н2О
Парциальное давление СО2 над раствором едкого
натра NaOH в процессе поглощения равно нулю до тех пор, пока вся щёлочь не
перейдёт в карбонат. Поглощение СО2 раствором карбоната натрия протекает с
образованием бикарбоната:
СО2 + Na2СО3 + Н2О = 2NaHСО3
Скорость абсорбции СО2 щёлочью возрастает с
повышением температуры. Увеличение концентрации карбоната в растворе
способствует снижению скорости абсорбции. В азотной промышленности очистка
водным раствором едкого натра NaOH применяется в качестве последней ступени
тонкой доочистки от СО2 конвертированного и коксового газа после водной очистки
(когда концентрация СО2 в газе составляет не более 0,3% объёмных).
Процесс проходит в жидкой фазе при 90 - 95 °С и
перемешивании. Установка регенерации щёлочи известью является громоздкой и
процесс недостаточно удовлетворяет современным санитарно - гигиеническим
требованиям (измельчение и гашение извести, транспортирование шлама в отвал и
т. д.). Поэтому регенерацию отработанной щёлочи предусматривают только при
значительном расходе щёлочи и необходимости привоза её со стороны. В остальных
случаях водные растворы отработанной щёлочи стараются использовать для
вспомогательных процессов нейтрализации и сбрасывают в специальные системы
химически загрязнённых стоков.
Очистка газа от СО2 методом низкотемпературной
абсорбции метанолом
В интервале температур от -30 до -60 °С и при
давлении 1 - 3 МПа метанол является эффективным абсорбентом не только двуокиси
углерода, но и сероводорода, органических соединений серы и некоторых других
примесей, присутствующих в газовой смеси. Растворимость СО2 в метаноле
значительно выше, чем в воде, и возрастает с понижением температуры и
увеличением давления. Так, при -60 °С растворимость двуокиси углерода в
метаноле в 75 раз превышает её растворимость в воде при 25 °С. Поэтому при
промывке газа метанолом в условиях низких температур расход абсорбента на
очистку единицы объёма газа значительно меньше, чем при водной очистке от СО2.
Благодаря этому соответственно уменьшаются
энергетические расходы в процессе абсорбции. Потери водорода при
низкотемпературной абсорбции также снижаются по сравнению с их потерями при
водной промывке газа под давлением. Это связано не только с сокращением
удельного расхода абсорбента, но и с уменьшением растворимости водорода в
метаноле при понижении температуры. Процесс низкотемпературной абсорбции
наиболее целесообразно проводить при 1 - 3 МПа. Нижний предел давления
составляет 0,5 МПа. Этот метод эффективен в случае одновременного удаления из
газовой смеси нескольких примесей при их достаточно высоком начальном
содержании. Несмотря на необходимость применения холодильной машины,
энергетические расходы в описанном процессе не превышают расхода энергии при
промывке газа водой.
Сравнение различных методов очистки
При выборе процесса очистки окончательным
критерием является величина приведенных затрат, зависящих в основном от
энергетических и капитальных затрат.
Однако в каждом случае необходимо учитывать
факторы, зависящие от конкретных условий и влияющие на экономику процесса. Эти
факторы можно разбить на три группы:
· внешние технологические параметры
процесса - состав, давление и температура очищаемого газа, требуемая степень
очистки, параметры энергоресурсов (давление пара, наличие отбросного тепла,
возможность использования вторичных энергоресурсов и т. д.);
· внутренние параметры процесса -
расход тепла, электроэнергии, растворителя, отходы, тип и вес аппаратов;
· экономические факторы - цены на
энергию, сырье, отходы, аппаратуру, а также дефицитность каких-либо видов сырья
и энергии.
Кроме того, следует иметь в виду, что для
крупнотоннажных агрегатов при сравнении методов очистки необходимо учитывать
степень надежности процесса и оборудования.
Наиболее распространенный производственный
вариант достаточно полной очистки - очистка горячим раствором поташа. Метод не
требует больших затрат на энергию и сырье, протекание процесса позволяет
повторно использовать некоторые ресурсы.
.
ОБОСНОВАНИЕ ОПТИМАЛЬНЫХ ПАРАМЕТРОВ ТЕХНОЛОГИЧЕСКОГО ПРОЦЕССА
Очистка конвертированного газа
от CO2 - процесс,
протекающий в несколько стадий. Во-первых, происходит физическая абсорбция газа
(растворение), во-вторых - химическая реакция, результатом которой является
связывание растворенного (абсорбированного) газа. Протекание абсорбционных
процессов характеризуется их статикой и кинетикой:
Статика абсорбции, т. е.
равновесие между жидкой и газовой фазами, определяет состояние, которое
устанавливается при весьма продолжительном соприкосновении фаз. Равновесие
между фазами определяется термодинамическими свойствами компонента и
поглотителя и зависит от состава одной из фаз, температуры и давления.
Кинетика абсорбции, т. е.
скорость процесса массообмена определяется движущей силой процесса (т. е.
степенью отклонения системы от равновесного состояния), свойствами поглотителя,
компонента и инертного газа, а также способом соприкосновения фаз (устройством
абсорбционного аппарата и гидродинамическим режимом его работы). В
абсорбционных аппаратах движущая сила, как правило, изменяется по их длине и
зависит от характера взаимного движения фаз (противоток, прямоток, перекрестный
ток и т. д.).
Различают физическую абсорбцию
и хемосорбцию.
При физической абсорбции
растворение газа не сопровождается химической реакцией (или, по крайней мере,
эта реакция не оказывает заметного влияния на процесс). В данном случае над
раствором существует более или менее значительное равновесное давление
компонента и поглощение последнего происходит лишь до тех пор, пока его
парциальное давление в газовой фазе выше равновесного давления над раствором.
Полное извлечение компонента из газа при этом возможно только при противотоке и
подаче в абсорбер чистого поглотителя, не содержащего компонента.
При хемосорбции (абсорбция,
сопровождаемая химической реакцией) абсорбируемый компонент связывается в
жидкой фазе в виде химического соединения. При необратимой реакции равновесное
давление компонента над раствором ничтожно мало и возможно полное его
поглощение. При обратимой реакции над раствором существует заметное давление
компонента, хотя и меньшее, чем при физической абсорбции. Уравнение реакции,
лежащей в основе хемосорбции рассматриваемого процесса при очистке
конвертированного газа:
K2CO3
+ H2O
+ CO2=2 KHCO3
Бикарбонат калия взаимодействует с растворенным
углекислым газом, связывая его, что влияет на изменение парциального давления
над раствором. С помощью термодинамического анализа определим термодинамические
условия протекания процесса, температуру, давление, концентрацию компонентов;
определим тепловой эффект реакции и температуру начала реакции. Так же найдем
условия протекания побочных реакций и условия максимального выхода целевого
продукта (в случае очистки подразумеваем максимальное связывание примесей в
ходе протекающей реакции).
4.1 ТЕРМОДИНАМИЧЕСКИЙ
АНАЛИЗ
Воспользуемся энтропийным методом для расчета
энергии Гиббса:

Термодинамические константы исходных веществ и
продуктов реакции взяты из справочной литературы[3] и представлены в таблице
3.1.
Проводим расчет 
 и
и 
 по формулам:
по формулам:



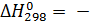
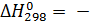 89,48 кДж/моль
89,48 кДж/моль

 89,48 кДж/моль
89,48 кДж/моль
Таблица 4.1.1
Термодинамические константы
участников основной реакции
|
Термодинамическая
величина
|
Вещество
|
|
K2CO3
|
H2O
|
CO2
|
KHCO3
|
|
  , кДж/моль-1150,18-285,83-393,51-959,5 , кДж/моль-1150,18-285,83-393,51-959,5
|
|
|
|
|
|
  , Дж/моль·К155,5268,95213,66128,7 , Дж/моль·К155,5268,95213,66128,7
|
|
|
|
|
Реакция идет с небольшим выделением тепла
(экзотермична), для смещения равновесия к продуктам необходимо отводить тепло
от системы. За счет последующего применения отведенного тепла к другим
процессам можем снизить затраты на энергию (вторичный энергоресурс).


 Дж/моль·K
Дж/моль·K
Процесс трудно осуществить при
атмосферном давлении, так как энтропия отрицательна. Определим температуру
начала реакции, используя следующее условие:
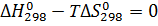

На основе температуры начала реакции
выберем температурный интервал расчета энергии Гиббса: 300
 600 К. С помощью энтропийного метода
проведем расчет
600 К. С помощью энтропийного метода
проведем расчет 
 при различных температурах:
при различных температурах:

 =
= 
 89480
89480 
 300· (
300· (
 182,13) =
182,13) = 
 34841 Дж/моль
34841 Дж/моль

 =
= 
 89480
89480 
 400· (
400· (
 182,13) =
182,13) = 
 16628 Дж/моль
16628 Дж/моль
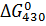
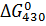 =
= 
 89480
89480 
 430· (
430· (
 182,13) =
182,13) = 
 11164 Дж/моль
11164 Дж/моль

 =
= 
 89480
89480 
 460· (
460· (
 182,13) =
182,13) = 
 5700,2 Дж/моль
5700,2 Дж/моль

 =
= 
 89480
89480 
 500· (
500· (
 182,13) = 1585 Дж/моль
182,13) = 1585 Дж/моль

 =
= 
 89480
89480 
 600· (
600· (
 182,13) = 19798 Дж/моль
182,13) = 19798 Дж/моль
Отобразим полученные данные на
графике (рис. 4.1) в координатах 
 . Сделаем вывод о влиянии
температуры на протекание реакции. Термодинамическая вероятность протекания
основной реакции с увеличением температуры уменьшается, необходимость отведения
тепла от системы подтверждается.
. Сделаем вывод о влиянии
температуры на протекание реакции. Термодинамическая вероятность протекания
основной реакции с увеличением температуры уменьшается, необходимость отведения
тепла от системы подтверждается.
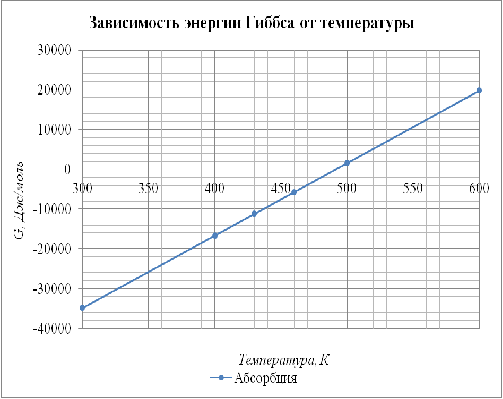
Рис. 4.1.1 
 График зависимости энергии Гиббса
от температуры
График зависимости энергии Гиббса
от температуры
аммиак двуокись углерод
абсорбция
Зависимость константы равновесия от
температуры может быть представлена в виде уравнения:






Рассчитаем значения констант
равновесия в указанном интервале температур, результаты представим в виде
таблицы 4.2. Построим график зависимости константы равновесия от температуры
протекания процесса.
Таблица 4.1.2
Значения константы равновесия основной реакции
при различных температурах
|
Температура,
К
|
K2CO3 + H2O + CO2=2 KHCO3
|
|
lgKp
|
Kp
|
|
300
|
6,073
|
9,3 1013
|
|
400
|
2,174
|
149,250
|
|
430
|
1,358
|
22,790
|
|
460
|
0,648
|
4,447
|
|
500
|
-0,166
|
0,683
|
|
600
|
-1,726
|
0,019
|

Рис. 4.1.2 
 График зависимости константы
равновесия от температуры
График зависимости константы
равновесия от температуры
Термодинамический анализ процесса
очистки конвертированного газа от диоксида углерода раствором поташа позволил
сделать следующие выводы:
1. В рассматриваемом интервале температур
(300-600 К) термодинамическая вероятность самопроизвольного протекания процесса
уменьшается, о чем свидетельствует значение энергии Гиббса.
. Согласно принципу Ле-Шателье увеличение
давления способствует смещению равновесия в сторону продуктов реакции
(Растворимость СО2 в горячем растворе поташа в значительной степени зависит от
парциального давления двуокиси углерода над раствором)
. Увеличение концентрации раствора поташа
по сравнению со стехиометрическим ведет к смещению равновесия в сторону
продуктов реакции (предельная концентрация соли в горячем растворе 40%, т.к.
дальше наблюдается выпадение осадка); горячие растворы поташа вызывают
коррозионное разрушение углеродистой стали, поэтому в растворы добавляют
ингибиторы коррозии.
4.2 КИНЕТИЧЕСКИЙ
АНАЛИЗ
В качестве побочной реакции рассмотрим процесс,
который применяют для выделения поглощенного газа (абсорбтива) из абсорбента и
получения его в чистом виде, а также для повторного использования абсорбента в
процессе абсорбции. Для проведения десорбции газа из жидкости необходимо, чтобы
концентрация этого газа в газовой фазе была ниже концентрации, соответствующей
равновесной в системе газ - жидкость. На практике для проведения процесса
десорбции используют три следующих метода:
· отгонку в токе инертного газа или
водяного пара;
· отгонку под действием подводимой к
абсорбенту теплоты;
· отгонку при снижении давления над
абсорбентом
Учитывая термодинамическую вероятность
самопроизвольного протекания основной реакции, заключаем, что в интервале
температур 300-600 К возможно протекание обратной реакции (десорбции газа), при
подведением тепла к системе.
В общем случае метод хемосорбционной очистки
обладает рядом особенностей оп сравнению с физической абсорбцией:
· Возможность абсорбции при низком
парциальном давлении вследствие более высокой поглотительной абсорбции
раствора;
· Относительно малая циркуляция
раствора и соответственно небольшой расход энергии на перекачку сорбента;
· Регенерацию осуществляют, как
правило, путем нагревания в сочетании со сбросом давления, при этом расход
тепла на десорбцию относительно невелик;
· Регенерацию проводят часто при
кипении абсорбента, его пары могут играть роль десорбирующего агента;
· Возможность проведения весьма тонкой
очистки;
· Увеличение коррозии и протекание
побочных реакций, обусловленных применением повышенных температур и щелочных
агентом - сильных и слабых электролитов
Метод поташной очистки основан на применении относительно
дешевого абсорбента, но имеет ряд недостатков: малая растворимость карбоната в
воде (особенно бикарбоната) при обычной температуре, низкая скорость абсорбции,
что приводит к необходимости значительной циркуляции раствора и обуславливает
увеличение габаритов аппаратов. Кроме того, равновесное парциальное давление
СО2 над растворами поташа относительно велико, и не удается достичь тонкой
очистки газа (0,08 -0,15% СО2 в газе после очистки). Преимущество метода -
сравнительно низкий расход тепла на регенерацию.
Скорость процесса абсорбции может быть
рассмотрена через применение основного уравнения массопередачи[4]. Если
выразить движущую силу процесса в концентрациях газовой фазы (парциальные
давления), то оно принимает следующий вид:

Где 
 - средняя движущая сила процесса,
выраженная в единицах давления;
- средняя движущая сила процесса,
выраженная в единицах давления;
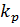
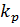 - коэффициент массопередачи,
отнесенный к единице движущей силы, выраженной через парциальные давления
поглощаемого газа;
- коэффициент массопередачи,
отнесенный к единице движущей силы, выраженной через парциальные давления
поглощаемого газа;
Химическая реакция, сопровождающая
процесс абсорбции, оказывает существенное влияние на кинетику процесса, т.к.
скорость определяется не только интенсивностью массопереноса, но и скоростью
протекания химической реакции. Благодаря химической реакции растворенный CO2 переходит
в связанной состояние (KHCO3). Концентрация свободного
газа в жидкости уменьшается, а процесс абсорбции ускоряется (рост величины 
 ), в сравнении с абсорбцией без
химического взаимодействия фаз[1]. Скорость хемосорбция зависит как от скорости
химической реакции, так и от скорости массопереноса между фазами. В зависимости
от лимитирующего процесса различаются кинетическую и диффузионную области
процесса хемосорбции.
), в сравнении с абсорбцией без
химического взаимодействия фаз[1]. Скорость хемосорбция зависит как от скорости
химической реакции, так и от скорости массопереноса между фазами. В зависимости
от лимитирующего процесса различаются кинетическую и диффузионную области
процесса хемосорбции.
Кинетическая область определяется
как протекание процесса, при котором скорость химического взаимодействия меньше
скорости массопереноса. В диффузионной области лимитирующая стадия - скорость
диффузии компонента в зоне реакции, которая зависит от гидродинамических
условий в системе и физических свойств.
Абсорбция, как и другие процессы,
протекает на границе раздела фаз. Как следствие - абсорбционные аппараты (далее
- абсорберы) должна иметь развитую поверхность контакта между жидкой и газовой
фазами. Абсорберы по своим конструктивным особенностям делят на следующие
основные группы: пленочные, насадочные, тарельчатые, распыливающие. На практике
очистка конвертированного газа от CO2 проводится
в насадочных колоннах. Варьирование площади поверхности раздела фаз происходит
за счет смены насадки. Основные применяемые виды - кольца Рашига и седловидная
насадка Берля.
Значения коэффициентов абсорбции CO2 растворами
карбонатов могут быть вычисленные по уравнениям[4]:

Где 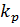
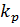 - объемный коэффициент абсорбции,
отнесенный к газовой пленке, кмоль/(м3·ч·атм)
- объемный коэффициент абсорбции,
отнесенный к газовой пленке, кмоль/(м3·ч·атм)
L - расход жидкости,
кг/(м3·ч)

 - удельная поверхность несмоченной
насадки, м2/м3
- удельная поверхность несмоченной
насадки, м2/м3
C’, n -
константы, зависящие от типа насадки

Где 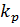
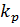 - объемный коэффициент абсорбции,
отнесенный к газовой пленке, кмоль/(м3·ч·атм)
- объемный коэффициент абсорбции,
отнесенный к газовой пленке, кмоль/(м3·ч·атм)

 - удельная поверхность насадки,
м2/м3
- удельная поверхность насадки,
м2/м3
a - 0,288 +
0,00316u, (u - плотность
орошения), м3/(м2
 ч)
ч)
b = 0,0059

 - вязкость раствора
- вязкость раствора
Таблица 4.2
|
Насадка
|

|
n
|

|
|
Кольца
Рашига d=9,5 мм d=25 мм
|
1,53
0,81
|
0,56
0,36
|
485
190
|
|
Седловидная
(насадка Берля), l = 25 мм
|
1,00
|
0,42
|
259
|
Выводы теоретического анализа:
. По условиям равновесия абсорбция
происходит тем полнее, чем ниже температура. Однако, скорость абсорбции тем
выше, чем выше температура. На основании сопоставления термодинамических и
кинетических факторов выбираем оптимальную температуру абсорбции 35-100оС.
Реакции, протекающие при очистке, являются экзотермическими и обратимыми, при
повышении температуры раствора химическое соединение разлагается с выделением
исходных компонентов, регенерация раствора протекает при 120-135оС.
. Согласно принципу Ле-Шателье увеличение
давления способствует смещению равновесия в сторону продуктов реакции. На
производстве применяется абсорбционный метод с давлением 2,5 - 2,8 мПа, с
последующей тонкой очисткой растворами моноэтаноламина или едкого натра.
. При десорбции применяется
дросселирование поглотительного раствора, при котором раствор вскипает и CO2
выдувается образующимся водяным паром.
. На основании справочных данных о
влиянии степени карбонизации на температуру выпадения твердой фазы в водных
растворах K2CO3,
выбираем оптимальную концентрацию раствора 30 - 40%.
.
СИНТЕЗ И АНАЛИЗ ХТС
5.1 ХИМИЧЕСКАЯ
МОДЕЛЬ
Абсорбционная очистка газа - циклический
процесс, на стадии абсорбции диоксид углерода поглощается растворителем,
очищенный газ отправляется на последующую переработку, а насыщенный раствор
регенерируют, что требует дополнительного расхода энергии. Процесс абсорбции
проводим в массообменном аппарате типа насадочной колонны (насадка - кольца
Рашига или седловидная насадка Берля).
Первоначально происходит физическая абсорбция CO2
раствором, после чего поглощенный диоксид углерода вступает в реакцию с
карбонатом калия. Благодаря химической реакции растворенный CO2
переходит в связанной состояние (KHCO3).
Концентрация свободного газа в жидкости уменьшается, а процесс абсорбции
ускоряется. Особую важность представляет десорбция компонента и вторичное
использование поташного раствора в целях экономии сырья. При десорбции
применяется дросселирование поглотительного раствора, при котором раствор
вскипает и CO2 выдувается
образующимся водяным паром.
Очистка газа поташным раствором основана на
взаимодействии диоксида углерода с карбонатом калия по суммарному уравнению
2CO3
+ H2O
+ CO2 = 2 KHCO3
Скорость реакции практически полностью
лимитируется скоростью медленно протекающей реакции в жидкой фазе
СO2
+ ОН- = HCO3-
5.2 СТРУКТУРНАЯ СХЕМА

Схема 4.2.1 Структурная схема очистки
конвертированного газа от СО2 раствором горячего поташа
Метод основан на применении относительно
дешевого абсорбента, но имеет ряд недостатков: малая растворимость карбоната в
воде (особенно бикарбоната), низкая скорость абсорбции, что приводит к
необходимости значительной циркуляции раствора и обуславливает увеличение
габаритов аппаратов. Кроме того, равновесное парциальное давление СО2 над
растворами поташа достаточно велико, и не удается достичь тонкой очистки газа
(0,08 - 0,15% СО2 в газ после очистки). Преимущество метода - сравнительно
низкий расход тепла на регенерацию.
5.3 ТЕХНОЛОГИЧЕСКАЯ СХЕМА
Проведен анализ различных технологических схем,
представленных в литературе[1] [4] [5] [8] [9]. Выделены следующие виды схем: с
разделенным потоком, схема поташной очистки с активатором, схема поташной
очистки без активатора.
Описание технологической схемы
Газ под давлением 12,5 - 15 атм при температуре
155оС, которая развивается при сжатии его в компрессоре, поступает в
теплообменник 1, куда подводится отработанный раствор после абсорбции. Часть
тепла газ передает раствору, охлаждаясь при этом до температуры 125-130 оС,
затем проходит водяной холодильник 2, где охлаждается до 122оС, и через
влагоотделитель 3 поступает в абсорбер 4.
В абсорбере имеется несколько слоев насадки из
колец Палля. Сюда подается регенерированный раствор поташа, 2/3 которого из
регенератора 5 поступает в нижнюю часть абсорбера при температуре 102 °С.
Примерно 1/3 раствора охлаждается в водяном холодильнике до 80 °С и затем
подается в верхнюю часть абсорбера. Такая схема циркуляции раствора
способствует снижению остаточного содержания СО2 в газе.
В абсорбере 4 газ очищается с 18 - 19% начальной
концентрации СО2 до остаточного содержания 0,3 - 1,5% и при температуре 80 °С
выходит из абсорбера. Далее очищенный газ охлаждается в водяных холодильниках
и, пройдя влагоотделитель, поступает на сжатие в газовые компрессоры.
Отработанный поташный раствор удаляется из
абсорбера через автоматический клапан регулятора уровня, проходит теплообменник
1 и дросселируется в верхнюю часть регенератора 5, где поддерживается
избыточное давление порядка 0,06 - 0,07 атм. При этом из раствора выделяется
двуокись углерода, концентрация которой достигает 99,5 - 99,8% СО2.
Регенератор представляет собой вертикальный
колонный аппарат с двумя слоями насадки из колец Палля. Раствор стекает сверху
вниз по насадке; при нагревании его парам из раствора выделяется двуокись
углерода. К низу регенератора подключен выносной подогреватель, в котором
раствор нагревается глухим паром до 104 - 105 °С.
Горячий регенерированный раствор перекачивается
из регенератора насосом 8 на орошение абсорбера 4. Уровень раствора в
регенераторе регулируется изменением подачи свежего конденсата в куб этого
аппарата.
Операторная и технологическая схема поташной
очистки конвертированного газа от СО2 приведены в приложениях 1 и 2
соответсвенно.


.
ВЫБОР И ОСНОВАНИЕ КОНСТРУКЦИЯ ОСНОВНОГО АППАРАТА
Основными аппаратами на стадии очистки являются
абсорберы[7] и регенераторы, в которых осуществляются массообменные процессы
поглощения и выделения диоксида углерода.
К массообменной температуре очистки предъявляют
следующие требования:
· Большая пропускная способность по
газу и жидкости, что позволяет создать малогабаритные аппараты и делает
возможным их транспортирование по железной дороге с завода изготовителя
· Высокая степень насыщения хемосорбента
а абсорбере, что обеспечивает высокие технико-экономические показатели процесса
· Глубокая степень извлечения СО2 из
газа, остаточное содержание не должно превышать 0,03 - 0,15% об.
· Минимальный расход тепла в
регенераторе
· Стабильность в работе и легкость
регулирования работы аппарата
Для очистки технологического газа от СО2 в
крупнотоннажных агрегатах производства аммиака используют насадочные колонны
(для случая не активированного поташного раствора). Массообменные аппараты с
нерегулярной насадкой обеспечивают высокую надежность эксплуатации в широком
диапазоне нагрузок по газу и жидкости, что важно для агрегатов большой
единичной мощности. В качестве насадки в абсорберах и регенераторах применяют
кольца Рашига, насадку Берля, металлические кольца Палля, керамические седла
Инталлокс.
Абсорбер представляет собой двухсекционный
аппарат, верхняя секция имеет диаметр 3,9, нижняя - 4,2 м. Аппараты изготовляют
из конструкционной низколегированной стали 09Г2С с термообработкой сварных
швов. Рабочий диапазон температур для стали от -70оС до +450оС.
Общий вид абсорбера поташной очистки из
справочной литературы [5] и показан в приложении 3 Технологические и некоторые
конструктивные данные, характеризующие абсорбер приведены в таблице 5.1.,
проведен сравнительный анализ представленных данных на основе расчетов из
литературы[6].
Таблица 5.1
Технологические и конструктивные характеристики
абсорбера поташной очистки
|
Показатель
|
Значение
|
|
Диаметр
аппарата, м
|
4,242/2,740
|
|
Высота
аппарата, м
|
58,5
|
|
Характеристика
насадки, м
|
|
нижняя
секция, 3 слоя колец Палля, м
|
0,05
|
|
верхняя
секция, 2 слоя колец Палля, м
|
0,04
|
|
Скорость
газа на входе в аппарат, м/с
|
0,24
|
|
Давление
в абсорбере, МПа
|
2,7
|
|
Температура
раствора, оС
|
|
вход,
I поток
|
80
|
|
вход,
II поток
|
102
|
|
выход
|
80
|
|
Концентрация
СО2 в газе, %
|
|
вход
|
18
- 19%
|
|
выход
|
0,3
- 1,5
|
|
Сопротивление
аппарата, МПа
|
0,05
|
Помимо основных аппаратов - абсорберов и
регенераторов, на стадии очистки применяют теплообменные аппараты - газовые и
паровые кипятильники, воздушные холодильники, конденсатор-холодильник. Для
подачи в абсорбер регенерированного раствора используют насосы с приводом от
паровых турбин или с электроприводом.
.
РАСЧЕТ МАТЕРИАЛЬНОГО И ЭНЕРГЕТИЧЕСКОГО БАЛАНСОВ. ОПРЕДЕЛЕНИЕ РАСХОДНЫХ НОРМ ПО
СЫРЬЮ И ЭНЕРГИИ. ПУТИ ИСОЛЬЗОВАНИЯ ВТОРИЧНЫХ ЭНЕРГОРЕСУРСОВ
7.1 МАТЕРИАЛЬНЫЙ
БАЛАНС
Используя данные из литературы[4][5] по
входящему и выходящему из абсорбера потоков, рассчитаем материальный баланс в
программе Microsoft
Office Excel
2007. Исходные данные потоков представлены в таблице 6.1.
Таблица 6.1
Исходные данные по входному и выходному потоку
абсорбционного аппарата в методе поташной очистки конвертированного газа от
диоксида углерода в производстве аммиака
|
КОНВЕРТИРОВАННЫЙ
ГАЗ
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Вход
в абсорбер
|
|
|
|
Выход
из абсорбера
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Статья
|
|
|
%
об.
|
|
|
Статья
|
|
|
%
об.
|
|
Разница
|
|
|
Газ
|
207123
|
|
|
|
Сухой
газ
|
171336
|
|
|
35787
|
|
|
|
N2
|
41298
|
19,59
|
|
|
|
N2
|
41298
|
23,86
|
|
0
|
|
|
|
Ar
|
521
|
0,25
|
|
|
|
Ar
|
521
|
0,30
|
|
0
|
|
|
|
H2
|
127671
|
60,56
|
|
|
|
H2
|
127671
|
73,75
|
|
0
|
|
|
|
CO
|
1036
|
0,49
|
|
|
|
CO
|
1036
|
0,60
|
|
0
|
|
|
|
CO2
|
35958
|
17,06
|
|
|
|
CO2
|
0,10
|
|
35787
|
|
|
|
CH4
|
639
|
0,30
|
|
|
|
CH4
|
639
|
0,37
|
|
0
|
|
|
|
|
|
|
|
|
|
|
|
|
|
0
|
|
|
Вода
|
3690
|
1,75
|
|
|
Вода
|
1777
|
1,03
|
|
1913
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
В
систему приходит
|
210813
|
|
|
|
Выходит
из системы
|
173113
|
|
|
37700
|
|
|
Начальное
содержание СО2 в газе
|
17,06
|
%
|
|
|
Остаточное
содержание СО2 в газе
|
0,099
|
%
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Степень
очистки от СО2
|
|
99,421
|
%
|
|
На
хемосорбцию расходуется СО2
|
35787
|
нм3/ч
|
|
Конденсируется
воды
|
|
|
1913
|
нм3/ч
|
|
|
|
|
|
Таблица 6.2
Сводная таблица материального баланса для
абсорбера поташной очистки от диоксида углерода в производстве аммиака
|
|
Вход
в абсорбер
|
|
|
Выход
из абсорбера
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Статья
|
|
|
Об.
|
Масс.
|
|
Статья
|
|
Об.
|
Масс.
|
|
|
Конвертированный
газ
|
210813
|
113489,20
|
|
Сухой
газ
|
173113
|
43193,30
|
|
|
14
|
|
N2
|
|
41298
|
25811,25
|
|
|
N2
|
41298
|
25811,25
|
|
|
40
|
|
Ar
|
|
521
|
930,36
|
|
|
Ar
|
521
|
930,36
|
|
|
2
|
|
H2
|
|
127671
|
11399,20
|
|
|
H2
|
127671
|
11399,20
|
|
|
28
|
|
CO
|
|
1036
|
1295,00
|
|
|
CO
|
1036
|
1295,00
|
|
|
44
|
|
CO2
|
|
35958
|
70631,79
|
|
|
CO2
|
171
|
335,89
|
|
|
16
|
|
CH4
|
|
639
|
456,43
|
|
|
CH4
|
639
|
456,43
|
|
|
18
|
|
H2O
|
|
3690
|
2965,18
|
|
|
H2O
|
1777
|
1427,95
|
|
|
|
|
|
|
|
|
Вода,
конденсат
|
|
|
|
|
|
|
|
|
|
|
|
H2O
конд
|
1913
|
1537,23
|
|
|
Раствор
поташа
|
|
734911,61
|
|
Раствор
поташа
|
|
|
|
|
|
K2CO3
|
|
|
220473,48
|
|
|
H2O
|
|
485680,71
|
|
|
|
H2O
|
|
|
514438,13
|
|
На
десорбцию
|
|
|
|
|
|
|
|
|
|
|
|
KHCO3
|
|
319526,786
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
В
систему приходит
|
|
|
848400,80
|
|
Выходит
из системы
|
|
848400,80
|
|
|
|
|
|
|
кг/ч
|
|
|
|
кг/ч
|
|
Вывод: Согласно материальному балансу для
данного аппарата за час абсорбируется 35787 нм3, а на десорбцию уходит 848400,8
кг абсорбента. Используя последний показатель можно рассчитать материальный
баланс для десорбции.
7.2 ТЕПЛОВОЙ
БАЛАНС
|
Вход
|
395
|
K
|
|
Выход
|
353
|
K
|
|
|
|
|
|
Cp=
a + b·T + c·T2
|
|
a
|
b
|
c'
|
|
Cp=
a + b·T + c'·T-2
|
|
N2
|
27,88
|
0,00427
|
|
|
29,567
|
Дж/моль·К
|
|
Ar
|
27,88
|
0,00427
|
|
|
29,567
|
|
|
H2
|
27,28
|
0,00326
|
0,000005
|
|
28,568
|
|
|
CO
|
28,41
|
0,0041
|
-4,6E-05
|
|
30,029
|
|
|
CO2
|
44,14
|
0,00904
|
-0,00085
|
|
47,711
|
|
|
CH4
|
14,32
|
0,07466
|
-0,00017
|
|
16,616
|
|
|
H2O
|
39,02
|
0,07664
|
0,001196
|
|
69,293
|
|
|
K2CO3
|
80,29
|
0,10904
|
|
|
123,361
|
|
Используя данные из литературы[3] по
коэффициентами теплоемкости рассчитаем теплоемкость веществ на входе и
количество теплоты приносимое веществами в систему.
|
ПРИХОД
ТЕПЛА В СИСТЕМУ
|
|
|
Тепло,
приносимое конвертированным газом
|
1672565,221
|
кДж/ч
|
|
|
Теплота
химической реакции
|
|
|
39710,06076
|
кДж/ч
|
|
|
Тепло,
подводимое
|
|
2310792,774
|
кДж/ч
|
|
|
|
|
|
Итого
|
4023068,055
|
кДж/ч
|
|
|
РАСХОД
ТЕПЛА СИСТЕМОЙ
|
|
Теплота
конденсации воды
|
3549469,018
|
кДж/ч
|
|
Тепло,
уносимое очищенным газом
|
451046,7019
|
кДж/ч
|
|
Потери
тепла
|
|
|
|
22552,3351
|
кДж/ч
|
|
|
|
|
Итого
|
4023068,055
кДж/ч
|
|
|
|
|
|
|
|
|
|
|
|
|
Расчет теплового баланса показал, что необходимо
подводить к абсорберу количество теплоты, равное 4023060 кДж. Подача такого
количества энергии возможна через нагрев раствора поташа.
.3
ВТОРИЧНОЕ ИСПОЛЬЗОВАНИЕ ЭНЕРГОРЕСУРСОВ
Технологическая схема, описанная ранее,
подразумевает циклическое использование раствора поташа и переносимого им
тепла.. На примере теплообменника 01 можем наблюдать охлаждение газа за счет
частичной передачи теплоты охлажденному отработанному раствору. Далее
отработанный раствор переходит в десорбер 05, где претерпевает дросселирование
и обработку водяным паром, за счет чего происходит регенерация поташного
раствора, в результате которой горячий раствор идет на дальнейшую абсорбцию, а
пар, частично сконденсировавшаяся вода и СО2 выходят из системы. Данная
технология позволяет существенно экономить энергию на нагрев и поддержание
температуры газа и поташного раствора.
Так же возможно замыкание обмена воды между
теплообменниками 02, 03, подачей водяного пара и скруббером-промывателем, что
так же существенно снизит затраты на использование энергии и ресурса
технической воды.
Тонкая очистка от СО2 позволяет получить два
готовых к синтезу или транспортировке и последующей продаже следующие продукты:
конвертированный газ (производство аммиака) и СО2 (производство карбамида)
.
ЭКОЛОГИЧЕСКАЯ ОЦЕНКА ПРОИЗВОДСТВА. ОТХОДЫ ПРОИЗВОДСТВА, ИХ УТИЛИЗАЦИЯ. ПДК
Экологические проблемы отрасли производства
аммиака непосредственно связаны с ее экономическими проблемами. Устаревшие
технологии и оборудование не способствуют решению проблем загрязнения среды. Поэтому
вложения в модернизацию промышленности напрямую связаны с улучшением
экологической ситуации в отрасли. Недостаток таких вложений ведет к снижению
спроса на продукцию и объема производства. Неэффективность производства и
относительно большое количество отходов на единицу продукции уменьшают доходы,
необходимые для инвестирования в природоохранные объекты В производстве аммиака
имеются выбросы газов в атмосферу, сточные воды и твёрдые отходы.
Выбросы в атмосферу
Выбросы газов в атмосферу разделяются на:
· постоянные выбросы газов,
обусловленные ведением постоянного технологического процесса;
· периодические выбросы газов в период
пуска и остановки производства;
· периодические выбросы газов,
обусловленные нарушением технологического режима;
В производстве аммиака имеются постоянные
выбросы газов, содержащие вредные компоненты: дымовые газы после подогревателя
природного газа, дымовые газы после трубчатой печи и вспомогательной печи,
«грязная фракция» СО2 или «чистая фракция» СО2 вместе с «грязной», вентвыбросы
из аккумуляторной и кислотной. Вредными веществами в выбрасываемых дымовых
газах огневого подогревателя сероочистки и первичного риформинга является
сернистый ангидрид, окислы азота, окись углерода. Вредными веществами,
выбрасываемыми в атмосферу с углекислым газом, является угарный газ,
моноэтаноламин и сероводород.
Диаметры и высоты труб выбросов выбраны таким
образом, чтобы количество вредных веществ, выбрасываемых в атмосферу, не
создавали в приземном слое концентраций вредных веществ, превышающие санитарные
нормы (после их рассеивания).
Периодически при пуске агрегата в атмосферу
выбрасываются:
· дымовые газы из огневого
подогревателя синтеза
· парогазовая смесь из отпарной
колонны
Периодически при пуске, остановке, нарушении
технологического режима предусмотрено сжигание газов в факельной установке для
предотвращения загрязнения атмосферы при выбросах газа. Кроме того,
периодически в аварийных случаях в атмосферу сбрасываются выбросы от
предохранительных клапанов и перед ремонтом оборудования.
Сточные воды
Для обеспечения надёжности охраны водных
ресурсов при аварийных ситуациях и остановках на ремонт агрегата предусмотрено
наличие аварийных и дренажных ёмкостей. Все вредные стоки направляются на
очистные сооружения и на биологическую очистку. Сбросы после химической очистки
(промывки) системы парообразования перекачиваются в накопительные ёмкости и
далее на очистные сооружения.
Стоков, содержащих аммиак, из блоков синтеза не
имеется. Аммиачная вода, образующаяся в период восстановления катализатора
синтеза, а также опорожнения аппаратов от остаточного количества аммиака перед
ремонтом направляются в дренажную ёмкость, размещённую на складе жидкого
аммиака.
Твёрдые и жидкие отходы
Отработанные катализаторы процессов сероочистки,
конверсии метана, конверсии диоксида углерода, метанирования и синтеза аммиака
отправляются в отвал, на металлолом или на переработку.
Продувочные газы
Продувочные газы разделяются на фракции в
зависимости от температуры. Разделение происходит на аммиачную воду; водород,
который поступает обратно на компрессор сжатия газа; метан, который
используется в качестве топлива и аргон, который является готовой продукцией.
Рассмотрим предельно допустимые концентрации
вредных веществ в воздухе рабочей зоны. Данные представлены в документе ГН
2.2.5.2100-06 "Предельно допустимые концентрации (ПДК) вредных веществ в
воздухе рабочей зоны" и Дополнению N 2 к ГН 2.2.5.1313-03.
При концентрации углерода диоксида в воздухе
0,25-1% у человека изменяется функция дыхания и кровообращения, при 2,5-5%
наблюдается головная боль, раздражение верх, дыхательных путей и др., при 7%
учащается сердцебиение, появляются рвота, головокружение и другие симптомы. При
высоких концентрациях углерода диоксида в воздухе наступает смерть от остановки
дыхания (при 20% через несколько секунд).
Окись углерода образует с гемоглобином крови
стойкие соединения, кровь теряет способность поглощать кислород воздуха,
наступает кислородное голодание. Лёгкое отравление угарным газом сопровождается
головной болью, шумом в ушах, мельканием и туманом в глазах, слабостью и
сильным головокружением, рвотой. При остром отравлении наступает отдышка,
потеря сознания, судороги, удушье. Систематическое отравление небольшими дозами
угарного газа сопровождается быстрой утомляемостью, раздражительностью,
головными болями. ПДК газа в воздухе рабочей зоны составляет 20 мг/м3. Окись
углерода - горючий газ, в смеси с воздухом или кислородом образует
взрывоопасные смеси.
Водород (Н2) - физиологически инертный газ без
запаха и цвета. Может вызывать удушье вследствие снижения концентрации
кислорода в воздухе. Легко воспламеняется, пламя бледно-голубого цвета. В смеси
с воздухом и кислородом образует взрывоопасные смеси.
Аммиак (NH3)
- сильно токсичное, огне- и взрывоопасное вещество. В нормальных условиях -
газ, хорошо растворим в воде, имеет резкий характерный запах нашатырного
спирта. При нарушении герметичности оборудования и трубопроводов высокого
давления мгновенно образует облако большой концентрации. В зоне выделения
аммиака у человека могут возникнуть спазмы органов дыхания: из-за сильного
слезотечения и рези в глазах происходит потеря ориентации. ПДК аммиака 20
мг/м3.
Моноэтаноламин (МЭА) - и его растворы имеют
запах аммиака, токсичны и огнеопасны, вызывают ожоги, опасно попадание их в
глаза.
ЗАКЛЮЧЕНИЕ
В ходе курсовой работы была рассмотрена
технологическая схема поташной очистки конвертированного газа раствором
горячего поташа. В современной технологии переработки природного газа очистка
от диоксида углерода с использованием растворов поташа занимает первое место в
общем числе промышленных способов.
Как уже было отмечено выше, эффективность
процесса абсорбции СО2 карбонатными растворами зависит от температуры,
парциального давления диоксида углерода и водяного пара над раствором, состава
и концентрации активирующих добавок, а также от основности раствора. Повышение
температуры абсорбции, хотя и приводит к уменьшению поглотительной способности
раствора, однако увеличивает растворимость карбонатных солей в воде и скорость
абсорбции. В промышленности существуют различные модификации этого процесса,
основными отличиями которых являются различные активаторы, температура и
концентрация растворов
Дальнейшие научные и технические разработки для
данного процесса необходимо направить на повышение степени очистки
конвертированного газа и повышение степени десорбции поташного раствора для
снижения количества используемого сырья и частичного решения проблем
экологического характера.
СПИСОК ЛИТЕРАТУРЫ
[1]
Семенова, Т.А. Очистка технологических газов / Семенова Т.А., Лейтес И.Л.,
Аксельрод Ю.В., [и др.] М:, Химия 1977, - 488с.
[2]
Степанов, А.В. Получение водорода и водородосодержащих газов /Степанов А.В,
Киев: Наукова думка 1982, - 312 с.
[3]
Равдель, А.А. Краткий справочник физико-химических величин / Равдель, А.А.,
Пономарева А.М., Спб:. Иван Федоров 2003, - 240 с.
[4]
Справочник азотчика: Физико-химические свойства газов и жидкостей. Производство
технологических газов. Очистка технологических газов. Синтез аммиака. - 2-е
изд., перераб / Под редакцией Е.Я. Мельников, М.: Химия 1986, - 512 с.
[5]
Семенов, В.П. Производство аммиака / Семенов В.П., Киселев Г.Ф., Орлов А.А.,
Семенова Т.А., М:. Химия, 1985, - 368 с..
[6]
Александров, И.А. Ректификационные и абсорбционные аппараты: Методы расчета и
основы конструирования / Александров И.А., М:. Химия, - 296 с.
[7]
Андреев Ф.А. Технология связанного азота/ Андреев Ф.А., Каргин С.И., Козлов
Л.И., Приставко В.Ф., М:. Химия 1966, - 500 с.
[8]
Ведерников М.И. Производство аммиака из природного газа / Ведерников М.И., Киев:
Технiка 1970, - 232 с.