Фракционирование белков мяса. Количественное определение белков
Министерство
образования и науки РФ
Федеральное
государственное бюджетное образовательное учреждение высшего профессионального
образования
Ивановский
государственный химико-технологический университет
Факультет
ОХиТ
Кафедра
технологии пищевых продуктов и биотехнологии
Лабораторная
работа
по курсу
«Введение в технологию продуктов питания»
«Фракционирование
белков мяса. Количественное определение белков»
Выполнил: студент гр. 4-29
Ивлев П.А.
Иваново 2012
Цель работы:
. Проведение экстракции и последующего
анализ белков животного происхождения по растворимости говяжьего мяса;
. Освоение спектрофотометрического метода
анализа белков говяжьего мяса;
Теоретическое введение:
Мясо - части туши сельскохозяйственных животных,
состоящие из мышечной и сопутствующих тканей: соединительной, жировой,
хрящевой, костной, нервной, крови, а также, кровеносных сосудов и лимфатических
узлов.
Мясные продукты являются одним из основных
источников полноценного белка, содержание которых колеблется в пределах 11-22%.
В состав мяса и мясопродуктов входят простые и
сложные белки, в том числе водо-, соле- и щелочерастворимые, обеспечивающие,
например, такие важные функции, как удержание воды, набухаемость и
растворимость, а также сложные белки-пигменты, отвечающие за цвет продукта.
Белки различаются не только химическим и пространственным строением, но и
размерами частиц, а также формой молекул. Последняя включает две группы:
фибриллярные и глобулярные, отличающиеся физико-химическими свойствами, прежде
всего растворимостью в воде, водно-солевых растворах и водных растворах
полярных растворителей, а также способностью к денатурации, гидролизу и другим
превращениям. Белки животного происхождения, и в частности белки мяса, по
аминокислотному составу более соответствуют структуре человеческого тела, а
значит более отвечают потребностям организма, а в частности белки мышечной
ткани хорошо сбалансированы по аминокислотному составу, в них нет недостатка
незаменимых аминокислот.
Белки - главный компонент органических веществ.
Они влияют не только на пищевую и биологическую ценность в мясе, но и
предопределяют ф/х, технологические показатели сырья и готовой продукции в
целом.
Мышечные белки по их растворимости (и
морфологическому строению клеток) делят на три группы:
1. Белки мышечной ткани:
Миозин - фибриллярный белок, составляет около
40% белков клетки мышечной ткани, состоящий из двух навитых друг на друга
б-спиральных полипептидов. Миозин - полноценный, хорошо перевариваемый белок.
Совершенно чистый миозин растворим в воде и образует вязкий раствор с массовой
долей до 4% белка. Температура денатурации миозина около 45 - 50 °С (у птицы
около 51 °С); изоэлектрическая точка определяется при рН 5,4. Биологические
функции миозина связаны с координированным движением живых организмов и
автолитическими превращениями мышечных тканей после убоя животных.
Актин составляет 12-15% всех мышечных белков и
является основным компонентом тонких нитей. Этот белок существует в двух формах
- глобулярной (Г-форма) и фибриллярной (Ф-форма). В растворах с низкой ионной
силой актин существует в виде мономера. При повышении ионной силы раствора до
физиологического уровня Г-актин полимеризуется в Ф-актин, очень похожий на
нить. Г-актин представляет собой одну полипептидную цепочку, сложенную в
глобулу. Быстрая полимеризация актина происходит также при добавлении ионов Mg2+.
При этом образуется двунитчатая спираль, каждая составляющая в которой
напоминает нить бус, закрученных одна вокруг другой. Актин относится к
полноценным и легкоусвояемым белкам.
Миоглобин - хромопротеид, составляющий в среднем
0,6-1,0% общего количества белков. Миоглобин - белок, обуславливающий
характерную красную окраску мяса мышечной ткани. Он состоит из белковой части -
глобина и простетической группы - гемма (Рис. 1).
мясо белок фракционирование
растворимость
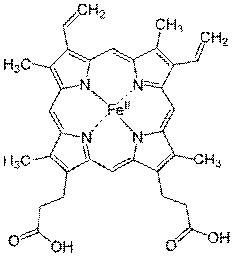
Рис. 1. Структурная формула гемма.
Структура белка представлена одной полипептидной
цепью, состоящей из 153 аминокислотных остатков. Функция данного белка состоит
в передаче кислорода, доставляемого гемоглобином, ферментативным системам
клеток.
Миоглобин мяса легко присоединяет кислород, с
образованием ярко-красного фермента - оксимиоглобина (MbO2).
При этом железо не окисляется, а остается двух валентным, т. е. гем в молекуле
миоглобина окружен остатками глобина. Но под воздействием света, кислорода
воздуха в течение длительного времени происходит более глубокое окисление - до Fe3+
- коричневое окрашивание.

Рис. 2. Формы миоглобина.
Соотношение вышеуказанных производных
миоглобина, присутствующих в мясе и определяет его цвет. Отличить эти формы
друг от друга и определить их содержание можно по ЭСП миоглобина.
Миоальбумины составляют около 1-2% белков
мышечного волокна. Растворимы в воде и нерастворимы в кислой среде, так как
имеют изоэлектрическую точку около рН 3,0-3,5; температура денатурации 45-47
°С.
Глобулин составляет около 20% общего количества
белковых веществ мышечного волокна. Растворим в солевых растворах даже очень
низкой концентрации, температура денатурации при рН 6,5 около 50 °С, при рН 7,0
- около 80 °С, изоэлектрическая точка лежит в интервале рН 5,0-5,2.
Тропомиозин - белок палочковидной формы с
относительной молекулярной массой около 70 000, постоянно присутствующий в
структуре тонких (актиновых) филаментов. Биологическая роль тропомиозина
сводится к регулированию взаимодействия актина и миозина в процессе мышечного
сокращения. Массовая доля тропомиозина составляет 10-12% всех белков миофибрилл
или 2,5% белков мышц. Растворим в воде, но из мышечной ткани водой не
извлекается. Изоэлектрическая точка определяется при рН 5,1.
2. Белки соединительной ткани
Коллаген - фибриллярный белок, составляющий
основу соединительной ткани организма (сухожилие, кость, хрящ, дерма и т. п.) и
обеспечивающий ее прочность и эластичность. Коллаген обнаружен у многоклеточных
животных; отсутствует у растений, бактерий, вирусов, простейших и грибов. Это
основной компонент соединительной ткани и самый распространенный протеин у
млекопитающих, составляющий от 25% до 35% протеинов во всём теле. Молекула
коллагена представляет собой правозакрученную спираль из трёх б-цепей. При
частичном гидролизе коллаген превращается в желатин - бесцветную или имеющую
желтоватый оттенок смесь полипептидов, продукт переработки (денатурации)
соединительной ткани животных.
Эластин - белок, обладающий эластичностью и
позволяющий тканям восстанавливаться, например, при защемлении или порезе кожи.
Эластин - белок, отвечающий за упругость соединительных тканей. Подобно
коллагену, богат глицином и алинином, в то же время содержит большое количество
лизина и мало пролина; существует в виде сети полипептидных цепей, благодаря
чему обладает большой упругостью.
Качество мяса в значительной степени зависит от
содержания в ней соединительной ткани: чем больше соединительной ткани, тем
ниже биологическая и пищевая ценность.
Мышечные белки по их растворимости (и
морфологическому строению клеток) делят на три группы:
· Миофибриллярные (солерастворимые) - белки
нерастворимые в воде, но растворимые в 1%-ом и более растворе поваренной соли.
Данный тип белков составляет 55 % от общего количества белков.
· Сакроплазматические - белки,
растворимые в воде и в растворах малой ионной силы ( < 0,6 ммоль/дм3).
К ним относят окислительные и липидосодержащие ферменты, миоглобин, а также
гемовые и гликолетические пегменты.
· Белки стромы - преимущественно белки
(3-5 % от общего содержания) соединительной ткани, которые служат каркасом, поддерживающим
структуру мышц. Являются щелочерастворимыми белками.
Состав говяжьего мяса:
Говядина I
и II категории
содержит: воды 67,7 и 71,7 %, белков - 18,9 и 20,2 г %, жиров - 12,4 и 7,0 г
%(калорийность - 187 и 144 ккал в 100 г продукта); калий - 315 и 334 мг %,
натрия 60 и 65 мг %, кальций 9 и 10 мг %, магния - 21 и 23 мг %, фосфора - 198
и 210 мг %, железа - 2,6 и 2,8 мг %; Витаминов: В1 - 0,06 и 0,07 мг %, В2 -
0,15 и 0,18 мг %, РР - 2,8 и 3,0 мг %. Малоценных белков эластина и коллагена
говядина в среднем содержит 2,6 %. Первый из них главным образом сосредоточена
внутри сухожилий, фасций, коллаген - основной компонент связочного аппарата.
Жиры, накапливающиеся непосредственно в мышечной ткани, создают привычное для
большинства людей ощущение вкусности блюда из говядины и, разумеется, повышает
его калорийность.
По различны данным, холестерина в говяжьем жире
в среднем 75 %, а противохолестеринового фактора - лецитина в среднем 70 %.
Однако сами мышечные волокна содержат большое количество лецитина и, что не
менее важно, довольно много холина и метионина. Поэтому говядина обладает
немалыми липотропными свойствами. В 100 г говядины содержится примерно 0,35 г
азотистых экстрактивных веществ. Кроме уже перечисленных минеральных веществ,
микроэлементов есть в ней также кобальт, цинк, медь, никель, сера, марганец.
Биуретовая реакция - качественная на все без
исключения белки, а также продукты их неполного гидролиза, которые содержат не
менее двух пептидных связей. Биуретовая реакция обусловлена присутствием в
белках пептидных связей, которые в щелочной среде образуют с сульфатом меди
(ІІ) окрашенные медные солеобразные комплексы.
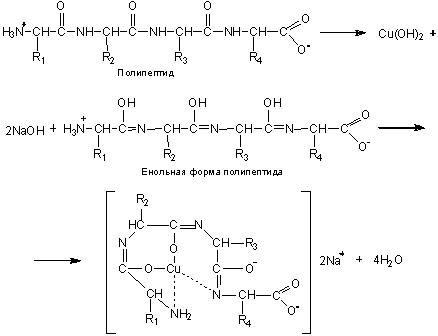
Рис. 3
Биуретовую реакцию дают также некоторые
небелковые вещества, например биурет (NH2-CO-NH-CO-NH2),
оксамид (NH2CO-CO-NH2), ряд аминокислот (гистидин, серин,
треонин, аспарагин).
Ход работы:
I. Фракционирование
белков говяжьего мяса.
После экстракции белков, т.е. перевод белков в
растворенное состояние, приступают к разделению - фракционированию смеси белков
на индивидуальные белки. Для этого применяют разнообразные методы: высаливание,
тепловую денатурацию, осаждение органическими растворителями, хроматографию,
электрофорез, распределение в двухфазных системах, кристаллизацию и др. Растворение
белков в воде связано с гидратацией каждой молекулы, что приводит к образованию
вокруг белковой глобулы водных (гидратных) оболочек, состоящих из
ориентированных в определенной форме в пространстве молекул воды. По химическим
и физическим свойствам вода, входящая в состав гидратной оболочки, отличается
от чистого растворителя. В частности, температура замерзания ее составляет
-40°С. В этой воде хуже растворяются сахара, соли и другие вещества. Растворы
белков отличаются крайней неустойчивостью, и под действием разнообразных
факторов, нарушающих гидратацию, белки легко выпадают в осадок. Поэтому при
добавлении к раствору белка любых водоотнимающих средств (спирт, ацетон,
концентрированные растворы нейтральных солей щелочных металлов), а также под
влиянием физических факторов (нагревание, облучение и др.) наблюдаются
дегидратация молекул белка и их выпадение в осадок.
1. Выделение водорастворимых белков:
В плоскодонную колбу (100 мл) помещаем 2 г
гомогенизированной мышечной ткани, заливаем дист. Водой, экстрагируем в
термостате при температуре 30 0С в течение 15 минут (при постоянном
перемешивании).
Водорастворимой фракции белков даем отстоятся,
отфильтровываем осадок, а фильтрат используем для исследования растворения
альбуминов. Промытый водой осадок мышечной ткани оставляем для выделения
глобулинов, а фильтрат, содержащие альбуминовые белки разделяем на две порции:
к первой порции ( ≈ 1 мл) добавляем 1 мл
биуретового реактива (цвет
ко второй порции (≈ 3 мл) добавляем 1 мл
мелкоизмельченный порошок (NH4)2SO4
при
нагревании до насыщения.
Выпавшие альбуминовые белки отфильтровываем.
Результаты:
В результате в раствор переходят альбуминовые
фракции белков мышечной ткани (мионин, миоглобин, миоглобулин, глобулин). При
добавлении биуретового реактива наблюдаем образование сине-фиолетового
окрашивания.
Из другой части раствора, где проводили
высаливание альбуминовой фракции при добавлении (NH4)2SO4
до насыщения - ионы соли связывают молекулы воды, что приводит к разрушению
гидратных оболочек на поверхности белковой молекулы, в результате этого
происходит их укрупнение, образуется осадок. В нашем случае серьезных изменений
в структуре белка не происходит: он не теряет своих первоначальных свойств,
поэтому полученный осадок может повторно растворяться в воде.
Растворимость белков в воде зависит от
количества полярных групп, структуры, размеров и формы молекул. Водорастворимые
белки имеют преимущественно глобулярное строение, (т. е. сферическую форму),
причем неполярные радикалы аминокислот (лейцина, валина, аланина, финилаланина)
находятся внутри белковой молекулы, а на наружной - полярные группы, за счет
чего увеличивается растворимость в воде.
Молекулярные массы глобулиновых белков выше, чем
у белков альбуминовой фракции, поэтому размеры глобулинов больше - на них хуже
образуются гидратные оболочки и их растворимость в воде значительно ниже.
2. Выделение солерастворимых белков:
Оставшуюся на марле кашицу из мышечной ткани
(после извлечения водорастворимых белков) отжимаем, переносим в ступку и
растираем с 10 мл 10 % раствора (NH4)2SO4
для
извлечения глобулиновой фракции белков.
Полученный экстракт отстаиваем и
отфильтровываем, а фильтрат, содержащий глобулиновую фракцию белков мяса,
разделяем на две части.
к первой порции ( ≈ 2 мл) добавляем
добавляем равный объем (NH4)2SO4
для
достижения полунасыщения; выпавшие глобулины отфильтровываем и проверяем их
растворимость. К раствору добавляем биуретовый реактив (бесцветный раствор),
тем самым доказав, что в растворе не осталось белков.
ко второй порции ( ≈ 5 мл), для осаждения
миозина, добавляем сухой порошок NaCl
при
нагревании до полного насыщения. Образовавшийся осадок - миозин, спустя 5 мин
отделяем на центрифуге, а оставшуюся жидкость декантируем. Оставшийся на дне
миозин растворяем в дистилировной воде и проводим качественную реакцию на
наличие белков с биуретовым реактивом (фиолетовый цвет).
Результаты:
3. Выделение щелочерастворимых белков:
Оставшийся после экстракции водо- и
солерастворимых белков осадок переносим в плоскодонную колбу и заливаем 5 мл 10
%-ого раствора NaOH
и помещаем на 20 мл в кипящую водяную баню, полученный раствор охлаждаем и
отфильтровываем. К 3 мл фильтрата добавляем по каплям раствор 0,1 Н уксусной
кислоты для нейтрализации щелочи. Выпавший осадок, который представляет собой
белки стромы, спустя 5 мин отфильтровываем. К фильтрату добавляем 1 мл
биуретового реактива, в результате фильтрат приобретает фиолетовую окраску.
Результаты:
Полученный фильтрат представляет собой белки
стромы. При биуретовой реакции окраска раствора приобрела бледно-фиолетовый
цвет, т.е. белки удалось выделить не полностью, при добавлении уксусной
кислоты, но при избытке которой белки переходят в осадок, а фиолетовая окраска
говорит о том, что в фильтрате присутствуют такие белки как альбумины, которые
кроме воды растворимы и в солевых растворах кислот и щелочей.
Полученные в ходе эксперимента данные заносим в
Таблицу 1.
Таблица 1. Таблица данных по эксперименту
фракционирования белков говяжьего мяса
|
Исходный
материал
|
Растворитель
|
Растворимый
белок
|
Из
какого растворителя высаливается
|
Биуретовая
реакция
|
|
Мясо
(говядина)
|
фильтрат
альбуминовой фракции белков
|
H2O
|
Миоген,
миоглобин, альбумин
|
(NH4)2SO4
|
+
|
|
фильтрат
глобулиновой фракции
|
(NH4)2SO4
|
Миозин,
актин, глобулины
|
(NH4)2SO4
|
+
|
|
|
(NH4)2SO4
|
Миозин
|
NaCl
|
+
|
|
фильтрат,
содержащий белки стромы
|
NaOH
|
Белки
стромы
|
CH3COOH
|
+
|
II.
Количественное определение белков
В данной работе содержание белков определялось
спектрофотометрическим методом Варбурга-Христиана, который основан на
способности ароматических радикалов таких аминокислот, как тирозин, триптофан,
фенилаланин, содержащихся в белках, к светопоглощению при 280 нм. Однако при
данной длине волны дают поглощение и нуклеиновые кислоты (Absmax
≈
260 нм). Поэтому при определении массовой доли белка, измерение оптической
плотности раствора производят при 260 и 280 нм, внося тем самым поправку на
присутствие нуклеиновых кислот и нуклеотидов.
Определение массовой доли белка:
Для анализа брали 1 мл исследуемого
белоксодержащей пробы (содержание белка 0,05…2 мг), затем добавляли 9 мл 0,85 %
раствора хлорида натрия и снимали спектр полученного раствора, с помощью
спектрофотометра Cary
50 (базисная линия была снята относительно 0,85% раствора NaCl).
Массовую долю белка (Б, %) определяем по формуле:
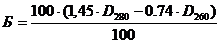
определение массовой доли миоглобина:

Рис. 3. ЭСП для миоглобина
Миоглобин, как указывалось выше, относится к
водорастворимым белкам; полученный раствор миоглобина имеет ярко красный цвет.
Наличие трех максимумов поглощения: при 416 нм, 542 нм и 580 нм, указывает на
то, что полученная белковая смесь содержит миоглобин в окси форме (MbO2).
Т.о. массовая доля миоглобина в мышечной ткани
следуемого говяжьего мяса:
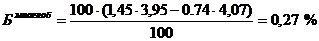
определение массовой доли водорастворимых
белков:
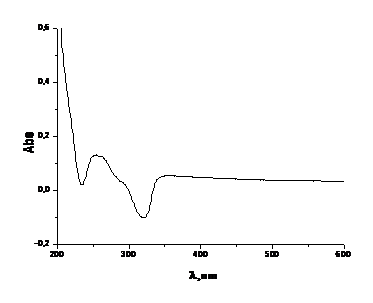
Рис. 4. ЭСП для водорастворимых белков
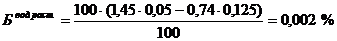
Вывод:
в ходе проведения данной лабораторной работы была проведена экстракция,
фракционирование и анализ белков животного происхождения (в частности белков
мясо говяжьего) по растворимости: за счет того, что альбумины лучше
растворяются в воде, они осаждаются из насыщенного раствора (NH4)2SO4,
в свою очередь глобулины осаждаются уже при достижении полунасыщения (NH4)2SO4.
Миозин выделяли из насыщенного раствора NaCl,
а белки стромы осаждаются при нейтрализации щелочного раствора уксусной
кислотой.
Освоен спектрофотометрический метод
количественного определения содержания белков в мясе, в результате которого
содержания белков в мясе говяжьем составило %:
· миоглобина: 0,27 ;
· водорастворимых: 0,002.
Список использованной литературы
1. Скурихин И.М.
Химический состав пищевых продуктов. Кн.2: Справочные таблицы содержания
аминокислот, жирных кислот, витаминов, макро- и микроэлементов, органических
кислот и углеводов. / Под. ред. проф., д.т.н. И.М. Скурихина и проф. д.м.н.
М.Н. Волгарева. - 2-е изд., перераб. и доп. - М.: Агропромиздат, 1987. - 360 с.
2. Гамаюрова В.С., Ржачитская Л.Э.
Пищевая химия: лабораторный практикум