Фармацевтический исследование производных фенотиазина
Курсовая
работа
"Фармацевтический
анализ производных фенотиазина"
Введение
Фенотиазины - исторически первый
класс антипсихотических средств - по своей химической структуре представляют
собой трициклические молекулы.
Все фенотиазины подразделяются на
три основных подтипа:
. алифатические,
. пиперидиновые,
. пиперазиновые производные.
Фенотиазины с алифатическими
боковыми цепями (например, хлорпромазин) в основном являются низкопотентными
соединениями (то есть для достижения терапевтического эффекта необходимо
использовать более высокие дозы препарата). Пиперидиновые производные обладают
антихолинергическими свойствами и в меньшей степени способны вызывать развитие
экстрапирамидных расстройств (например, тиоридазин, мезоридазин). Пиперазиновые
фенотиазины (например, перфеназин, трифлюоперазин, флуфеназин) являются
наиболее мощными антипсихотическими соединениями.
Связь
«структура-действие»
В основе химической структуры данной
группы препаратов лежит гетероциклическая система, состоящая из шестичленного
гетероцикла тиазина, конденсированного с двумя ядрами бензола (рис. 1).
Препараты, производные фенотиазина,
представляют собой сходные по химической структуре соединения, отличающиеся
только заместителями в положении 2 и 10 фенотиазинового кольца, причем между
структурой заместителей и фармакологическим действием проявляется четкая
зависимость: если в 10 положении находится липофильная группировка, содержащая
третичный азот во 2’ или 3’ положении, то препарат оказывает нейролептическое,
седативное и противоаллергическое действие. Если же эта группировка
гидрофильная (карбоксильная группа), то препарат оказывает коронарорасширяющее
и антиаритмическое действие.
Фармацевический анализ
фенотиазина
Фенотиазин

Получение
Фенотиазин получают нагреванием
дифениламина с S при 180-250 0C в высококипящих растворителях в
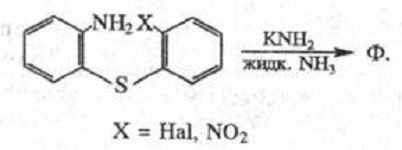
присутствии I2 или AlCl3. Общий метод получения
фенотиазина и его производных - циклизация 2'-замещенных производных
2-аминодифенил-сульфида в присутствии сильных оснований:
1. Описание.
Представляет собой желтые кристаллы.
Хорошо растворим при нагревании в
этаноле, уксусной кислоте, плохо - в диэтиловом эфире и бензоле. В холодной
серной кислоте растворим с выделением SO2.
3. Качественный
анализ.
.1. Химические свойства.
Имеет похожие свойства ароматических
соединений. Является хорошим донором электронов и с различными акцепторами
образует комплексы с переносом заряда. Легко вступает в электрофильное
замещение, которое направляется в первую очередь в положения 3 и 7 и часто
сопровождается окислением.
3.2. Реакционная
способность
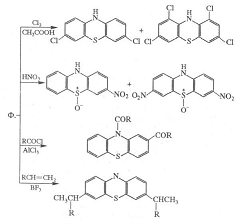
Бромирование фенотиазина в
нитробензоле протекает с образованием 1,2,3,7,8,9-гексабромпроизводного,
аналогичное хлорирование - с образованием продукта глубокого (до 11 атомов Cl)
хлорирования и потерей ароматичности одного из колец.
Окисление фенотиазина действием H2O2
или KMnO4 приводит к фенотиазин-5-оксиду или фенотиазин-5,5-диоксиду.
Реакции протекают в виде последовательных стадий с промежуточным образованием
катиона, в котором положение 3 чувствительно к атаке нуклеофильных реагентов,
например:

4. Примеси.
. Количественный
анализ.
Хранение.
Хранить их следует в банках из
оранжевого стекла, плотно закрытых пробками, залитыми парафином, в сухом месте
(это связано с легкоокисляемостью, и высокой гигроскопичностью).
Применение
Фенотиазин используется в качестве
инсектицида, антигельминта, антиоксиданта смазочных масел.
Фармацевтический анализ
производных фенотиазина
1. Аминазин
2. Трифтазин
3. Дипразин
1. Описание.
Гораздо большее значение имеют
производные фенотиазина, имеющие заместителя (R) в положениях 2 и 10 цикла.
Чаще R10 представляет собой остаток 3-диалкиламинопропанола

2. Растворимость.
Очень легко растворимы в воде, легко
- в 95% спирте, хлороформе; практически нерастворимы в эфире и бензоле.
3. Качественный
анализ.
.1. Химические свойства.
Из химических свойств производных
фенотиазина наиболее характерным является способность их к окислению. В
зависимости от характера окислителя (бромная вода, азотная и серная кислоты,
хлорид окисного железа и др.) образуются различного цвета продукты окисления.
Поэтому эти реакции используются для идентификации препаратов фенотиазинового
ряда.
3.2. Реакционная
способность.
Местом наибольшей реакционной
способности в молекуле фенотиазина и его производных является атом серы,
которая может окисляться до S4+ и S6+.
Окисление фенотиазина или его
производных бромом в уксусной кислоте или другим окислителем, например
перекисью водорода, приводит к образованию S-оксида (I) и диоксида-сульфона (II).

За счет третичного азота в молекуле
производные феноти-азина могут вступать в реакции с общеалкалоидными реактивами
(см. «Алкалоиды»).
Все препараты фенотиазинового ряда
применяются в виде гидрохлоридов, поэтому после выделения основания щелочью в
фильтрате обнаруживается хлор-ион с раствором нитрата серебра.
4. Примеси.
Из возможных примесей в препаратах
ГФ X допускает сульфаты, тяжелые металлы и фенотиазин в пределах эталонов.
Определяется также предел кислотности.
5. Количественное
определение.
Методы количественного определения
препаратов фенотиазинового ряда разнообразны и базируются на свойствах
соединений. Фармакопейным методом является метод кислотно-основного титрования
в неводных средах. Препарат растворяют в ледяной уксусной кислоте или ацетоне,
добавляют ацетат окисной ртути и титруют хлорной кислотой по индикатору
кристаллический фиолетовый или метиловый оранжевый.

Фармакопейным методом является и
обычный метод нейтра: лизации с дифференцирующими растворителями. Этот метод ГФ
X рекомендует для раствора и таблеток дипразина. Определение азота по методу
Кьельдаля ГФХ рекомендует для количественного определения аминазина в растворе.
Хранение.
Меры предосторожности.
При работе с производными
фенотиазина нужно исключить возможность попадания порошка и растворов на кожу и
слизистые оболочки, так как они вызывают сильное раздражение, отечность кожи
век, понижение артериального давления.
Использованные
литературные источники
фенотиазин химический
фармацевтический производный
1. Гетероциклические соединения, под ред. P. Эльдерфидда,
пер. с англ., т. 6, M., 1960, с. 568-91;
. Общая органическая химия, пер. с англ., т. 9, M., 1985,
с. 627-35. Г.А. Швехгеймер, В.И. Келарев;
. http://ru.wikipedia.org
. Мелентьева