Валидационная оценка методики анализа лекарственной формы состава: натрия хлорида 0,5; натрия ацетата 0,2; воды очищенной до 1 л
ГОУ
ВПО Пятигорская государственная
фармацевтическая
академия Росздрава
зав.
кафедрой проф. Е.Н. Вергейчик
КУРСОВАЯ
РАБОТА
по
фармацевтической химии на тему:
Валидационная
оценка методики анализа лекарственной формы состава: натрия хлорида 0,5; натрия
ацетата 0,2; воды очищенной до 1 л
Исполнитель:
Студент 5 курса 20 группы
Бойко
Денис Викторович
Руководитель:
Волокитин Сергей Васильевич
Пятигорск,
2010
1. Введение
Фармакологическая
группа веществ
Натрия ацетат и Натрия хлорид. Регуляторы водно-электролитного баланса и КЩС в
комбинациях <#"484193.files/image001.gif"> CH3COOCH2CH3
+ H2O
Аналитический эффект: характерный фруктовый
запах этилацетата.
2. По реакции с хлоридом железа (III)
3FeCl3 + 9CH3COO-
+ 2H2O →
[(CH3COO)6Fe(OH)2]CH3COO
+ 2CH3COOH + 9Cl-
Аналитический эффект: раствор окрашивается в
красно-бурый цвет.
2.2 Количественное определение
2.2.1 Первый компонент (по
хлорид-иону)
1. Аргентометрия (по Мору)
Титруют 1 мл раствора 0,1М раствором серебра
нитрата до оранжево-желтого окрашивания (индикатор - калия хромат).
Cl-
+ AgNO3
→ AgCl↓ + NO3-
AgNO3
+ K2CrO4
→ Ag2CrO4↓
+ 2KCl - в точке
титрования
2. Аргентометрия (по Фольгарду)
Добавляют избыток (точное количество) первого
титранта AgNO3.
Его остаток отитровывают вторым титрантом NH4NCS
до красного окрашивания (индикатор - железоаммонийные квасцы).
Cl- + AgNO3 →
AgCl↓ + NO3-
AgNO3 + NH4NCS
→ AgNCS↓ + NH4NO3
3NH4NCS
+ FeNH4(SO4)2
→ Fe(NCS)3
+ 2(NH4)2SO4
- в точке титрования
3. Аргентометрия (по Фаянсу)
Титруют 1 мл раствора 0,1М раствором серебра
нитрата до образования бледно-розового раствора над осадком (индикатор -
флуоресцеин).
4. Меркуриметрия
Тутруют раствором нитрата ртути (II)
до образования красного осадка (индикатор - дифенилкарбазон)
5. Меркурометрия
Титруют раствором нитрата ртути (I)
до обесцвечивания раствора (индикатор - тиоцианат железа (III))
2.2.2 Второй компонент (по
ацетат-иону)
1. Ацидиметрия
К 2 мл раствора прибавляют 3-5 мл эфира, 2 к.
раствора метилового оранжевого, 1 к. раствора метиленового синего и титруют
0,1М раствором соляной кислоты при взбалтывании до перехода зеленой окраски в
фиолетовую, сходную с окраской контрольного раствора.
2. Фотоколориметрический метод
Помещают 5 мл раствора в мерную колбу
вместимостью 25 мл и доводят до метки водой (раствор А).
К 5 мл раствора А прибавляют 1 мл 1% раствора
железа(III) хлорида, 4
мл воды и перемешивают. Через 50 мин. измеряют оптическую плотность (А1)
окрашенного раствора при длине волны около 370 нм в кювете с толщиной слоя 3
мм. Окраска устойчива 15-20 мин.
Раствор сравнения - смесь 1 мл 1% раствора
железа (III) хлорида и
9 мл воды (готовят одновременно с окрашенным анализируемым раствором).
Параллельно в тех же условиях проводят реакцию с
5 мл раствора СО натрия ацетата (0,0026 г) и измеряют оптическую плотность (А2).
2.3 Вывод
Из всех возможных методик количественного
анализа данной лекарственной формы приведенного состава были выбраны:
- фотоколориметрия (для Натрия ацетата);
- аргентометрия по Мору (для Натрия хлорида).
Из всех возможных методик качественного анализа
данной лекарственной формы приведенного состава были выбраны:
- образование осадка хлорида серебра (для
хлорид-иона);
- окрашивание пламени горелки (для иона натрия);
- образование этилацетата (для ацетат-иона).
3. Экспериментальная часть
3.1 Специфичность
3.1.1 Установление специфичности в
тестах «Испытание на подлинность»
Следует убедиться в отсутствии положительного
эффекта реакции на сопутствующие вещества: другие ингредиенты лекарственного
средства и вспомогательные вещества.
Практическое установление специфичности
Были приготовлены три модельные смеси состава:
Первая:
1. Натрия хлорида 0,5 г
2. Натрия ацетата 0,2 г
3. Воды очищенной до 100 мл
Вторая:
1. Натрия ацетата 0,2 г
2. Воды очищенной до 100 мл
Третья:
1. Натрия хлорида 0,5 г
2. Воды очищенной до 100 мл
Для проведения валидационной оценки, с тремя
модельными смесями были проведены следующие реакции:
1. Хлорид-ион
К 0,5 мл модельного раствора прибавили по 0,5 мл
HNO3
разб. и раствор AgNO3
0,1М. Образовался белый творожистый осадок, растворившийся в растворе аммиака.
2. Ион натрия
На шпатель была помещена капля раствора и
внесена в пламя горелки. Наблюдалось окрашивание пламени в желтый цвет.
3. Ацетат-ион
Упаривали 10 мл раствора на водяной бане до 1
мл, прибавляли 0,5 мл кислоты серной конц., 1 мл спирта этилового 96% и
нагревали. Ощущался запах этилацетата.
CH3COONa + CH3CH2OH
→ CH3COOC2H5↑ + NaOH
3.1.2 Установление специфичности в
тестах «Количественное определение»
Следует убедиться, что растворители и
сопутствующие компоненты не вступают в реакцию с титрантом, а также необходимо
удостовериться в специфичности индикатора.
1. Для проведения специфичности Хлорида натрия
использовали титриметрический метод анализа. Для чего брали три модельные
смеси. Титрование проводилось по следующей методике: к 5 мл навески прибавляли
2 мл воды, 2 капли K2CrO4
и
титровали 0,1М раствором AgNO3
до появления оранжево-желтой окраски.
NaCl + AgNO3 → AgCl↓
+ NaNO3
AgNO3 + K2CrO4
→ Ag2CrO4↓ + 2KNO3
2. Для проведения специфичности Ацетата натрия
использовали фотоколориметрический метод анализа. Для этого использовали 3
модельные смеси. Определение проводилось следующим образом: помещали 5 мл
раствора в мерную колбу вместимостью 25 мл и доводили до метки водой (раствор
А). К 5 мл раствора А прибавляли 1 мл 1% раствора FeCl3,
4 мл воды и перемешивали. Через 50 мин измерили оптическую плотность
окрашенного раствора при длине волны около 490 нм в кювете с толщиной слоя 3
мм. Параллельно готовили раствор сравнения - смесь 1 мл 1% раствора FeCl3
и 9 мл воды. Параллельно в тех же условиях проводили реакцию с 5 мл раствора СО
натрия ацетата (0,0026 г) и измеряли оптическую плотность.
Результаты испытания на специфичность
представлены в таблице 1 и 2
Табл 1. Подлинность
|
Модельные
смеси
|
|
Компоненты
|
I
|
II
|
III
|
|
1.
Натрия хлорид
|
+
|
+
|
-
|
|
белый
осадок
|
белый
осадок
|
|
|
2.
Натрия ацетат
|
+
|
-
|
+
|
|
запах
|
|
запах
|
Табл 2. Количественное определение
|
Модельные
смеси
|
|
Компоненты
|
I
|
II
|
III
|
|
1.
Натрия хлорид
|
5,0
мл
|
4,8
мл
|
-
|
|
2.
Натрия ацетат
|
0,035
|
-
|
0,035
|
3.1.3 Вывод
По результатам экспериментов можно сделать
заключение о специфичности выбранных методик определения подлинности и
количественного определения.
3.2 Прецизионность
(повторяемость)
Для установления повторяемости было проведено 6
параллельных определений содержания компонента в модельной смеси.
3.2.1 Опеделение прецизионности в
тесте «Количественное определение» титриметическим методом
Для этого из модельной смеси 3 было отобрано 6
аликвот, которые оттитровали раствором нитрата серебра 0,1М. Результаты
измерений представлены в таблице 3.
Табл 3. Результаты определения прецизионности
титриметрическим методом
|
Vтит,
мл
|
Найдено,
Xi
|
Xi-
|
(Xi- )2 )2
|
метрологические
характеристики
|
|
4,1
|
4,79
|
-0,04167
|
0,001736
|
SD=0,065727
|
|
4,1
|
4,79
|
-0,04167
|
0,001736
|
|
|
4,1
|
4,79
|
-0,04167
|
0,001736
|
|
|
4,2
|
0,078333
|
0,006136
|
RSD=2,7%
|
|
4,2
|
4,91
|
0,078333
|
0,006136
|
|
|
4,2
|
4,91
|
0,078333
|
0,006136
|
|
|
 =4,85 =4,85
|
|
∑=0,0216
|
|
SD=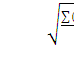 RSD=
RSD=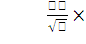 Xi=
Xi=
T=M×Mм×
Mм=58,44

М=0,1М
K=1,00
P=1000 мл
a=5 мл
3.2.2 Определение прецизионности в
тесте «Количественное определение» фотоколоримитрическим методом
Для этого из модельной смеси 2 было приготовлено
6 аликвот. Проведено 6 имерений оптической плотности. Результаты представлены в
таблице 4.
Табл. 4 Результаты определения прецизионности
фотоколориметрического метода
|
Ax
|
Найдено,
Xi
|
Xi-
|
(Xi- )2 )2
|
метрологические
характеристики
|
|
0,065
|
1,69
|
0,624
|
0,389376
|
SD=0,383445
|
|
0,030
|
0,78
|
-0,286
|
0,081796
|
|
|
0,035
|
0,91
|
-0,156
|
0,024336
|
|
|
0,045
|
1,17
|
0,104
|
0,010816
|
RSD=17%
|
|
0,030
|
0,78
|
-0,286
|
0,081796
|
|
|
 =1,066 =1,066
|
|
∑=0,58812
|
|
SD=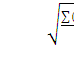 RSD=
RSD=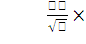 Xi=
Xi=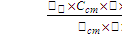
Aст(ГСО)=0,050
P=100 мл
Cст=0,0026

a=5 мл
V=5 мл
W1=25 мл
W2=10 мл
3.2.3 Вывод
По результатам экспериментов можно сделать
заключение о неподтверждении прецизионности методики «Количественное
определение» фотоколориметрическим методом Натрия ацетата, т. к. величина
относительного стандартного отклонения превышает предельное значение,
рекомендованное АОАС (RSD=2,7%
для 1% действующего вещества).
Методика «Количественное определение»
титриметрическим методом Натрия хлорида прецизионна, т. к. величина относительного
стандартного отклонения не превышает предельное значение, рекомендованное АОАС
(RSD=2,7% для 1%
действующего вещества)
3.3 Линейность
При определении линейности следует убедиться в
наличии прямой пропорциональной зависимости оптической плотности от
концентрации или количества определяемого вещества в анализируемой пробе.
3.3.1 Определение линейности
количественного определения Натрия хлорида титриметрическим методом в модельной
смеси 1
Для этого было приготовлено шесть опытных
образцов из шести разных навесок с точно известным количеством определяемого
вещества и проведено титрование. Навески были подобраны с таким расчетом, чтобы
на титрование было израсходовано не менее 1 мл и не более 10 мл титрованного
раствора.
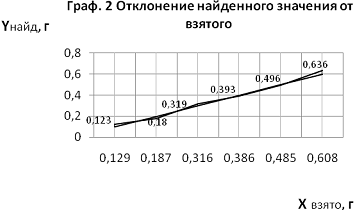
Результаты представлены в таблице 5. По данным
таблицы 5 был построен график 1 зависимости найденного содержания вещества от
объема титранта, пошедшего на титрование.
Табл. 5 Результаты определения линейности
титриметрического метода
|
X
навеска, г
|
Y найдено, г
|
|
0,123
|
1,1
|
0,129
|
|
0,18
|
1,6
|
0,187
|
|
0,319
|
2,7
|
0,316
|
|
0,393
|
3,3
|
0,386
|
|
0,496
|
4,15
|
0,485
|
|
0,636
|
5,2
|
0,608
|
|
∑=2,147
|
|
∑=2,111
|

Все экспериментальные точки находятся вблизи
линии тренда. Была составлена таблица и вычислен коэффициент корреляции.
Табл. 6 Вычисление коэффициента корреляции
|
Xi
|
Yi
|
Xi×Yi
|
Xi2
|
Yi2
|
|
|
0,123
|
1,10
|
0,1353
|
0,015129
|
1,21
|
r=0,999847
|
|
0,180
|
1,60
|
0,288
|
0,0324
|
2,56
|
|
|
0,319
|
2,70
|
0,8613
|
0,101761
|
7,29
|
|
|
0,393
|
3,30
|
1,2969
|
0,154449
|
10,89
|
|
|
0,496
|
4,15
|
2,0584
|
0,246016
|
17,2225
|
|
|
0,636
|
5,20
|
3,3072
|
0,404496
|
27,04
|
|
|
∑=2,147
|
∑=18,05
|
∑=7,9471
|
∑=0,954251
|
∑=66,2125
|
|
r=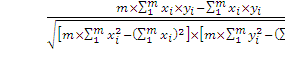
3.3.2 Определение линейности
количественного определения Натрия ацетата фотоколориметрическим методом в
модельной смеси 1
Данный опыт провести невозможно, т. к. это метод
не прошел тест на прецизионность.
3.3.3 Вывод
По результатам эксперимента можно сделать вывод
о линейности методики определения Натрия хлорида титриметрическим методом, т.
к. коэффициент корреляции больше критического значения (r=0,99).
3.4 Правильность
Данным тестом проверялось наличие или отсутствие
систематической погрешности.
3.4.1 Определение правильности
количественного определения Натрия хлорида титриметрическим методом.
Данные для обработки были взяты из табл. 5, по
которым был рассчитан t-критерий.
y=ax+b
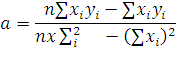
a= 0,935
b=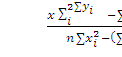
b= 0,017
 =0,15
=0,15
 =2,57
=2,57
3.4.2 Определение правильности
количественного определения Натрия ацетата фотоколориметрическим методом
Данный опыт провести невозможно, т. к. это метод
не прошел тест на прецизионность.
3.4.3 Вывод
Результаты расчетов показали, что  <
< .
Это говорит о минимальном (допустимом) влиянии систематической погрешности на
результаты эксперимента.
.
Это говорит о минимальном (допустимом) влиянии систематической погрешности на
результаты эксперимента.
Примечание.
В данной работе построение графиков и
математические расчеты были произведены с использованием программы Excel
(Microsoft
Office 2007).
Список литературы
1) Государственная фармакопея X
2) Государственная фармакопея XI
3) Качественный анализ
органических лекарственных средств: учебное пособие / [авт., ред.].-Пятигорск,
2007.
4) Муравьев И.А. Технология
лекарств. Изд. 3-е, перераб. и доп. Т. II,
М., «Медицина», 1980.
5) Руководство к
производственной практике по внутриаптечному контролю качества лекарственных
средств: учебное пособие / Е. В. Компанцева, Т. Т. Лихота, Г. И. Лукьянчикова,
Г.В. Сеньчукова / под редакцией Е.В. Компанцевой, - Пятигорск, 2006.
6) Фармацевтическая химия. В 2
ч.: Ч.1. Общая фармацевтическая химия; Ч. 2. Специальная фармацевтическая
химия: Учеб. для вузов.- Пятигорск, 2003.